Авторы заданий – Миссюль А.Б. (№ 1), Гусев И.М. (№ 2), Скрипкин М.Ю. (№ 3), Байгозин Д.В. (№№ 4-6), Ростовский Н.В. (№ 7)
№1
Работа литий-ионных аккумуляторов основана на обратимом переносе ионов лития между катодом и анодом. Типичная конструкция содержит в качестве анодного материала графит, в качестве катодного – LiCoO2.
Определите, какие вещества образуются при зарядке такого аккумулятора, если известно, что:
1. При взаимодействии 100 мг заряженного анодного материала с водой образуется 14,18 мл (н.у.) газа.
2. При обработке 100 мг заряженного катодного материала избытком соляной кислоты и пропускании полученного газа через водный раствор KI образуется раствор, на титрование которого расходуется 15,9 мл 0,1 н раствора Na2S2O3.
Емкость аккумулятора смартфона Samsung Galaxy SIII составляет 2100 мА·ч, а вес телефона 133 г. Какие массы графита и LiCoO2 необходимо взять, чтобы получить аккумулятор такой емкости? (Побочными процессами в аккумуляторе пренебречь.) Какую долю массы телефона составляют материалы аккумулятора?
№2
 Ниже приведена схема превращений элемента Е, соединения которого играют важнейшую роль в процессе фотосинтеза. Известно, что взаимодействием минерала Б с "морской" кислотой было впервые получено простое вещество, кислородсодержащие соединения которого широко используются в качестве отбеливателя. Соединение В кроме Е содержит 24,7 % массовых долей калия и 40,5% кислорода. Определите вещества А – З, напишите все уравнения реакций.
Ниже приведена схема превращений элемента Е, соединения которого играют важнейшую роль в процессе фотосинтеза. Известно, что взаимодействием минерала Б с "морской" кислотой было впервые получено простое вещество, кислородсодержащие соединения которого широко используются в качестве отбеливателя. Соединение В кроме Е содержит 24,7 % массовых долей калия и 40,5% кислорода. Определите вещества А – З, напишите все уравнения реакций.
№3
При определении состава газообразных соединений нередко реакцию проводят непосредственно в масс-спектрометре с последующей идентификацией присутствующих в газовой фазе молекулярных ионов по значениям m/z (отношение массы молекулярного иона (а.е.м.) к его заряду (в единицах е)). При этом прибор обычно калибруется таким образом, чтобы определять только положительные значения m/z при z=1.
В масс-спектрометр ввели пары двух простых веществ. При этом зарегистрировали две группы сигналов со значениями m/z 162 и 164, вторую – со значениями m/z 464, 466, 468, 470, 472, 474 и 476.
А) определите, какие вещества были введены в масс-спектрометр;
Б) определите, какие продукты образовались при взаимодействии этих веществ;
В) какова пространственная структура этих продуктов? Ответ аргументируйте;
Г) каково соотношение интенсивностей двух крайних сигналов внутри этих двух групп?
Д) Какие новые группы сигналов будут регистрироваться при повышении температуры в масс-спектрометре?
№4
В органическом синтезе важное значение имеют доступные высокоактивные реагенты. К ним относится вещество Х, легко получаемое при взаимодействии метилового эфира муравьиной кислоты и пентахлорида фосфора. Х вступает в реакции со многими органическими веществами. Некоторые реакции и свойства образующихся органических продуктов приведены в таблице:
| Реакция | Продукт | Массовая доля углерода в продукте, % | Температура кипения продукта, °С | Некоторые свойства продукта |
| HCOOCH3 + PCl5 при 20°С | Х | 20,89 | Положительная проба Бейльштейна | |
| CH3-COOH + X | A | 30,60 | Положительная проба Бейльштейна. Бурно реагирует с водой | |
| CH3-CO-CH3 + X | B | 31,89 | Положительная проба Бейльштейна | |
| C6H6 + X+ TiCl4, затем Н2О | C | 79,23 | Отрицательная проба Бейльштейна. Легко окисляется. | |
| CH3ONa + X | D | 45,27 | Отрицательная проба Бейльштейна. Легко гидролизуется водными растворами кислот, но не щелочей |
Примечание. Проба Бейльштейна: медная проволочка, смоченная веществом, вносится в пламя горелки. Проба положительна, если пламя окрашивается в голубовато-зеленый цвет.
1. Какой реагент обозначен буквой Х? Предложите еще один способ его синтеза.
2. Какие вещества обозначены буквами A–D? Напишите схемы соответствующих превращений.
3. Какова предположительная структура продукта взаимодействия Х с C6H6 до взаимодействия с Н2О?
4. Объясните химическую основу пробы Бейльштейна.
№5
Алкилсульфаты являются важными поверхностно-активными веществами, но их широкое использование приводит к загрязнению окружающей среды. Основным процессом их разрушения в природе является гидролиз, исследование которого представляет большой интерес. Для исследования зависимости кинетики гидролиза от рН среды был выбран неопентилсульфат калия, (CH3)3CCH2OSO3K (I). Результаты исследования оказались достаточно неожиданными.
Во-первых, если при гидролизе в кислой среде образовывался ожидаемый неопентиловый спирт, то в нейтральной или щелочной – изомерный продукт (II). При небольшом нагревании с водным раствором серной кислоты II образует газообразный продукт III, озонирование которого дает смесь IV и V, причем IV является популярным растворителем.
Во-вторых, наблюдаемая константа скорости реакции гидролиза I зависела от рН и имела значение kнабл = 2,3·10–1·сН+ + 2,7·10–6 с–1.
1. Определите строение продукта гидролиза Iв нейтральных и щелочных средах. Напишите уравнения всех упомянутых в задаче превращений.
2. Постройте график зависимости lgkнабл от рН в диапазоне от 2 до 10, объясните его вид.
3. Напишите кинетические уравнения для гидролиза I в неопентиловый спирт, соединение II и суммарное кинетическое уравнение гидролиза I. Определите соотношение неопентилового спирта и продукта II при рН 5.
4. Объясните, почему попадание некоторых бактерий в почву резко ускоряет разложение присутствующих в почве алкилсульфатов.
№6
В рамках программы поиска интересных для парфюмерной промышленности соединений был синтезирован о-эвгенол (F) – изомер природного эвгенола. Синтез был осуществлен по схеме:
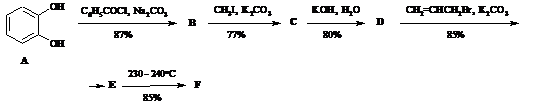
Вещества A, B, D, F дают характерное окрашивание при взаимодействии с раствором FeCl3, вещества С и Е – нет. Соединения Е и F являются изомерами с молекулярной формулой С10Н12О2. Для установления точной структурной формулы о-эвгенола его обработали сначала безводным хлористым водородом, а образовавшееся производное (G) – спиртовым раствором КОН. Образовавшийся продукт (H) имеет молекулярную формулу С10Н12О2 и не взаимодействует с раствором FeCl3.
1. Установите строение о-эвгенола и соединений В–Е и G–Н.
2. Рассчитайте общий выход о-эвгенола.
3. Почему при добавлении раствора FeCl3 к некоторым веществам образуются окрашенные растворы?
№7
Поиск и синтез пористых органических молекул является актуальной задачей для получения металл-органических пористых полимеров. Вещество Х – возможная основа для таких материалов. Синтез Х описывается следующей схемой:
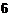
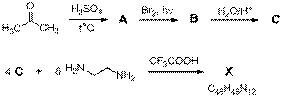
Соединение A (углеводород, содержащий 90 % углерода) имеет два, а вещество Х – три типа атомов водорода (по данным спектров ЯМР 1Н). Вещество В содержит 80.8 % брома.
Вопросы.
1.Расшифруйте схему синтеза Х и напишите структурные формулы соединений А, В, С и X.
2.Возможно ли использование на стадии B – C раствора щёлочи?
3.Какова роль СF3COOH на стадии получения Х?
