Расчет термодинамических констант равновесия
Термодинамическая константа равновесия может быть выражена как через активности веществ, участвующих в реакции, Ka, так и через фугитивности Kf:
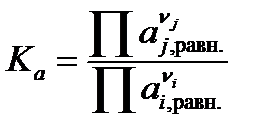
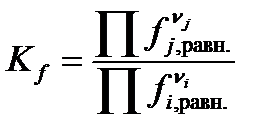 ,
,
Термодинамические константы равновесия являются безразмерными величинами.
Константа равновесия 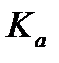 может быть рассчитана по частному уравнению изотермы химической реакции:
может быть рассчитана по частному уравнению изотермы химической реакции:
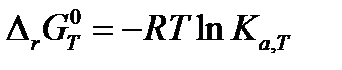 , , | (1.36) |
если известно значение изменения стандартной энергии Гиббса при данной температуре. Тогда термодинамическая константа равновесия 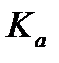 рассчитывается как экспонента:
рассчитывается как экспонента:
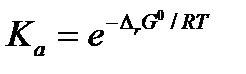 , , |
Термодинамическая константа равновесия зависит от природы реагирующих веществ и температуры, но не зависит от давления, поскольку изменение стандартной энергии Гиббса не зависит от давления по определению.
Величина константы равновесия может принимать значения от нуля до бесконечности: 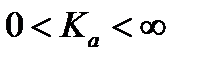
Пример: Рассчитаем термодинамическую константу равновесия реакции синтеза метанола при температурах 298 и 1000 К и давлении 101,325 кПа.
Решение:Рассчитаем изменение стандартной энергии Гиббса при температуре 298К, используя рассчитанные в предыдущих примерах значения 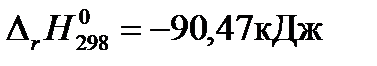 и
и 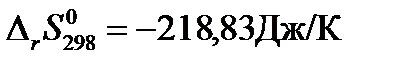 :
:
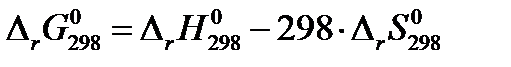 = – 90,47∙103 – 298∙( – 218,83) = – 25258,66 Дж
= – 90,47∙103 – 298∙( – 218,83) = – 25258,66 Дж
По частному уравнению изотермы химической реакции
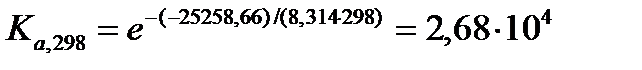
Для расчета константы равновесия при 1000 К воспользуемся рассчитанным в предыдущем примере значением стандартной энергии Гиббса при температуре 1000 К для реакции синтеза метанола 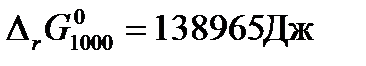 .
.
По частному уравнению изотермы химической реакции
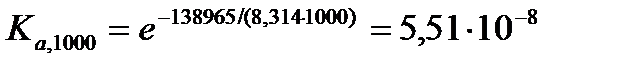
Если химическая реакция протекает при давлениях меньше ≤ 50 атм, то константа равновесия, выраженная через приведенные давления 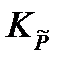 , равна термодинамической константе равновесия Kaи является безразмерной величиной.
, равна термодинамической константе равновесия Kaи является безразмерной величиной.
Практические константы равновесия
Химическое равновесие могут характеризовать практические константы равновесия. Практические константы равновесия могут быть рассчитаны, если при равновесии определить количества или концентрации веществ, участвующих в реакции тем или иным методом химического или физико-химического анализа. Они могут быть выражены
– через числа молей веществ ni,j в равновесии:
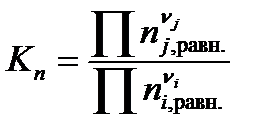 ; ; | (1.37) |
– через молярные концентрации веществ сi,j в равновесии:
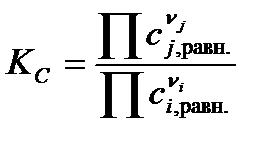 ; ; | (1.38) |
– через мольные доли веществ xi,j в равновесии:
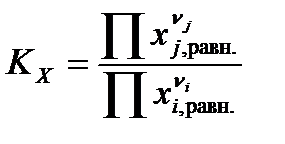 ; ; | (1.39) |
– через парциальные давления веществ pi,j в равновесии:
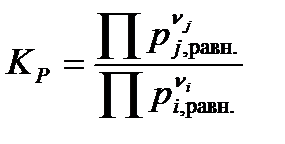 | (1.40) |
Практические константы равновесия являются размерными величинами.
Удобно использовать и безразмерные константы равновесия, например, константу, выраженную через приведенные давления 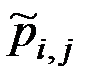 :
:
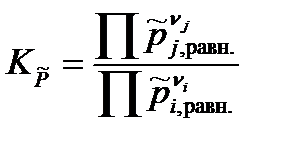 , , | (1.41) |
где 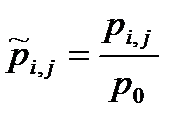 , а p0 – стандартное давление.
, а p0 – стандартное давление.
Между практическими константами равновесия существует определенная математическая связь. Например, легко показать, что константа 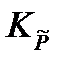 связана с практической константой равновесия, выраженной через моли Kn,следующим соотношением
связана с практической константой равновесия, выраженной через моли Kn,следующим соотношением
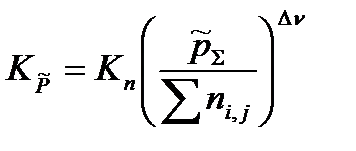 | (1.42) |
