Амперометрическое титрование
Под косвенным методом полярографирования понимают процесс титрования, в котором установление момента эквивалентности основано на контроле величины диффузионного тока, изменяющегося при взаимодействии исследуемого вещества с титрантом (амперометрическое титрование, разработано С. Березиску под руководством Я. Гейровского).
Для применения к такой реакции амперометрии необходимо, чтобы после наложения потенциала хотя бы одно из участвующих в ней веществ восстанавливалось или окислялось (рис.2.2) на микроэлектроде при соблюдении зависимости Iпред = f (C). Возможны следующие варианты амперометрического анализа (соответствующие им графические зависимости Iпред = f (Vст. р-ра), частично представленные на рис.3):
а) электроокисление (электровосстановление) титруемого вещества: снижение положительного (возрастание отрицательного) Iпред и выход на горизонталь вблизи момента эквивалентности (МЭ) параллельно оси Х (объем затраченного титранта);
б) электроактивное вещество – титрант: изменение постоянного значения Iпред на возрастающее вблизи МЭ;
в) электроактивные исследуемое вещество и титрант: снижение Iпред до значения, близкого к МЭ и последующий подъем;
г) последовательное титрование двух электроактивных веществ: снижение до первого МЭ и дальнейшее постоянное значение Iпред до второго МЭ. Далее – подъем при избыточном содержании титранта в системе;
д) электроокисление титруемого вещества и электровосстановление титранта: снижение Iпред до пересечения с осью Х (МЭ) и далее, как правило, под другим углом;
е) электроактивный продукт реакции: возрастание Iпред от точки пересечения осей под углом, зависящим от природы деполяризатора, до МЭ с последующим выходом на горизонталь;
ж) титрование с электроактивным индикатором: некоторое постоянное значение Iпред до МЭ с последующим снижением тока.
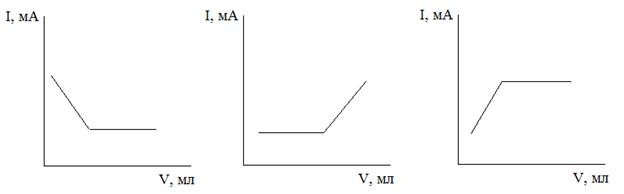
Рис.3. Кривые амперометрического титрования для случаев, когда электроактивны: 3.1. электроокисление титруемое вещество (электроокисление);
3.2. титрант;
3.3. продукт реакции.
Очевидно, что в ходе титрования объем жидкости в измерительной ячейке возрастает, например, при равенстве концентраций реагирующих веществ, в два раза. Полученные значения предельных токов необходимо корректировать, используя уравнение (9):
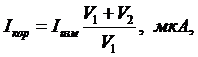 (9)
(9)
где Iкор – сила тока с учетом разбавления;
Iизм – измеряемая сила тока, мкА;
V1 – исходный объем исследуемого раствора, мл;
V2 – объем введенного титранта, мл.
В связи с прямолинейностью участков кривых титрования амперометрический анализ может быть значительно ускорен (по сравнению с другими методами электрометрии) сокращением точек определения предельного тока. В техническом анализе допускается измерение значений Iпред в 3-4 точках до и после момента эквивалентности с последующим определением последнего по пересечению пролонгированных прямых линий.
Другой, существенной для технического анализа особенностью амперометрии является зависимость возможности и интенсивности, заложенной в основу определения электродной реакции, от приложенного к индикаторному электроду напряжения. При обоснованном выборе величины последнего удается, как правило, достичь больших точности и селективности контроля смесей нескольких компонентов.
Лабораторные работы
Работа 2. Амперометрическое определение цинка
Гексацианоферроат (II) калия (ферроцианид калия К4[Fe (CN)6]) образует с цинком, кадмием и рядом других металлов труднорастворимые соединения, например:
3Zn 2+ + 2K4[Fe(CN)6] → K2Zn3[Fe(CN)6]2↓ + 6K+
5Cd2+ + 4K4[Fe(CN)6] → K6Cd5[Fe(CN)6]4↓ + 10K+
При взаимодействии с цинком возможно протекание реакции образования простой соли Zn[Fe(CN)6]2, также выпадающий в осадок.
Амперометрическое титрование проводят по уменьшению силы тока катодного восстановления определяемого металла до нулевого значения в точке эквивалентности по реакции:
Me+4 + 4e- → Me0
или по увеличению силы тока анодного окисления избытка титранта К4[Fe (CN)6] после достижения толчки эквивалентности:
[Fe (CN)6]4- - е- → [Fe (CN)6]5-
Применение платиновых электродов при определении цинка с использованием последней реакции позволяет достичь более высокой точности и селективности анализа.
Методика проведения анализа
Этап 1. Выбор потенциала электрохимического окисления стандарта К4[Fe (CN)6].
Очищают поверхность платинового анода (микроэлектрод) погружением в раствор азотной кислоты HNO3 (1:1), затем трижды обмывают рабочую поверхность электрода дистиллированной водой. В электролизер заливают цилиндром 1мл 0,1 М раствора титранта, добавляют 30 мл 0,5 М раствора сульфата калия K2SO4 (фон). В ячейку опускают электроды, доливают дистиллированной воды до полного погружения их рабочих поверхностей в раствор и перемешивают его на магнитной мешалке 1-2 минуты. Включают прибор и постепенно изменяют потенциал в интервале 0 ÷1,5 В через каждые 0,2 В регистрируют показания миллиамперметра.
По полученным данным строят вольтамперную зависимость I=f(E) и выбирают значение потенциала, соответствующее предельному току окисления ферроцианида К4[Fe(CN)6]. Ячейку и электроды ополаскивают дистиллированной водой.
Этап 2. Анализ исследуемого раствора хлорида цинка ZnCl2
Анализируемый раствор в мерной колбе на 100,00 мл доводят до метки дистиллированной водой и перемешивают. Аликвотную часть полученного раствора (10,00 мл) пипеткой переносят в электролизер, добавляют цилиндром 25 мл фонового раствора K2SO4 и 2-3 мл 2% аммиака при перемешивании на магнитной мешалке до растворения образовавшейся мути. Включают прибор и при выбранном на этапе 1 потенциале рабочего электрода (750-950 мВ) титруют из бюретки 0,1000 М стандартным раствором К4[Fe(CN)6].по 0,20 мл до возрастания тока, регистрируя показания миллиамперметра. Добавляют проверочные 3-4 порции стандарта, фиксируют значения увеличивающейся токовой величины. Аналогично проводят повторное (параллельное) титрование.
Обработка экспериментальных данных
По результатам титрования строят кривые в координатах I=f(Vст.р-ра).По излому на этих зависимостях определяют объемы стандартного раствора К4[Fe(CN)6], соответствующие точке эквивалентности и рассчитывают содержание цинка в анализируемом растворе, считая что аналитическая реакция идет по уравнению:
3ZnCl + 2K4[Fe(CN)6] → K2Zn3[Fe(CN)6]2↓ + 6KCl
В этом случае используется формула расчета количества цинка:
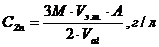
где М- молярная концентрация ферроцианида калия;
А – атомная масса цинка (65);
Vэ.т. – объем стандарта, пошедшего на титрование, мл;
Val – объем аликвоты.
Находят среднее значение Сср, г/л.
Работа 3. Биамперометрическое определение меди (титрование по замещению)
Титрование проводят с использованием двух индикаторных электродов. Определение основано на восстановлении в растворе двухвалентной меди йодидом калия и восстановлении образовавшегося молекулярного йода на платиновом электроде. Последующее титрование обратимой окислительно-восстановительной системы (I2/2I-) стандартным раствором тиосульфатом натрия (система S4O62-/2S2O32- необратима) обуславливает сложный характер изменения токовых значений (возрастание, прохождение через максимум и снижение до минимальной величины в точке эквивалентности).
Схема используемой для анализа установки аналогична представленной в работе 2 (рис. 5).
В анализируемом растворе протекает реакция замещения:
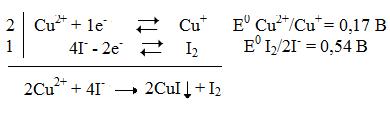
При введении избыточного количества йодид-ионов реальный потенциал пары окислителя (меди) возрастает до 0,70 В за счет снижения концентрации одновалентной меди связываемой в осадок CuI↓ согласно уравнению В. Нернста:
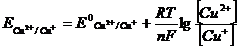
В ходе титрования идут процессы:
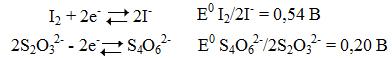
Методика проведения анализа
Анализируемый раствор двухвалентной меди доводят до метки в мерной колбе на 100,00 мл и перемешивают. В ячейку для титрования пипеткой вносят 20,00 мл приготовленного раствора, добавляют в качестве фона 20 мл 2 н Н2SO4 (мерным цилиндром) и, на кончике шпателя ~ 1,0 г йодида калия. Разбавляют исследуемую систему дистиллированной водой до середины высоты ячейки, помещают её на магнитную мешалку и перемешивают содержимое в течении 3 мин для завершения реакции замещения.
Погружают в раствор платиновые электроды и задают напряжение 20,0 мВ. Титруют исследуемую систему 0,1000 н тиосульфатом натрия по 0,10 мл, регистрируя показания тока после каждой порции стандарта. При достижении минимального значения тока (I, мВ) добавляют 3-4 проверочные порции титранта. Аналогично проводят повторное (параллельное) титрование.
Обработка экспериментальных данных
По результатам титрования строят кривые в координатах I=f(VNa2S2O3) (интегральная зависимость). Определяют среднее значение объема тиосульфата натрия (V), соответствующее точке эквивалентности и рассчитывают содержание меди в пробе:
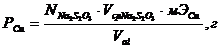
где 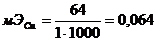 ; Val=20,00 мл.
; Val=20,00 мл.
Работа 4. Вольтамперометрическое определение тирозина
Схема определения. Тирозин является одной из немногих аминокислот, электроактивных при потенциалах, значительно превышающих окисление ртути. Поэтому его определение проводят на твердом (графит) электроде, а в качестве электрода сравнения применяют хлорсеребряный полуэлемент. Для создания ионной силы раствора, обеспечивающей достаточную электропроводность используют серную кислоту.
Электрод Электрод
индикаторный неполяризуемый
(графит) (хлорсеребряный)
 Ø Ø
Ø Ø
 С9Н11NO3 + H2SO4
С9Н11NO3 + H2SO4
Фон
Окисление тирозина на графите происходит по уравнению

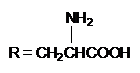
где
Методика проведения анализа. В пять мерных колб на 100,00 мл отбирают 0,00; 1,00; 2,00; 3,00; 4,00 мл исследуемого раствора тирозина и доводят (из бюретки) до меток 0,02 н серной кислотой. Растворы последовательно заливают в ячейку с электродами, помещают ее на магнитную мешалку и при интенсивном перемешивании снимают вольтамперные зависимости от 0,5 В до потенциала разряда чистого фона (Н2SO4). Перед снятием каждой вольтамперограммы зачищают до блеска рабочую поверхность графитового электрода (торец) фильтровальной бумагой и промывают оба электрода дистиллированной водой.
Обработка экспериментальных данных. После построения графиков зависимостей Ji =fEi измеряют высоты полярографических волн (предельных токов Jпр) и потенциалы полуволн (Е1/2). Определяют наличие необратимости окисления тирозина в данных условиях по влиянию разбавления на значение Е1/2. В случае непостоянства величин потенциалов полуволн или размытости полярографических волн снимают две дополнительные полярограммы с наибольшим содержанием тирозина при концентрации фона (Н2SO4) 0,04 и 0,06 н.
Концентрацию тирозина определяют по уравнению
С, моль/л = 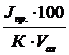 ,
,
где К - эмпирический коэффициент, определенный при анализе стандартных растворов тирозина;
Vал - объем аликвот исследуемого раствора;
100 - объемы мерных колб, используемых при приготовлении анализируемых растворов.
Вопросы для самоконтроля
1. Сущность полярографического анализа.
2. Методы качественного и количественного полярографического определения.
3. Взаимосвязь потенциала системы и диффузионного тока.
4. Зависимость аналитического сигнала от концентрации определяемого вещества.
5. Уравнение Д. Ильковича.
6. Классификация полярографических методов анализа.
7. Сущность амперометрического, биамперометрического титрования.
8. Влияние электроактивных компонентов на вид амперометрических зависимостей.
9. Принципиальные схемы полярографических (амперометрических) установок.
10. Электроды, применяемые в полярографии (амперометрии).
11. Обоснование величины потенциала индикаторных электродов.
12. Преимущества и недостатки полярографического (амперометрического) анализа.
Решение типовых задач
Задача 1. Навеску сплава 0,1000 г., содержащую кобальт растворили в смеси кислот и разбавили до 100,00 мл. Для полярографического анализа отобрали аликвоту 10,00 мл, разбавили фоном до 20,00 мл. Высота волны составила 35 мм.
Для построения калибровочного графика приготовили стандартный раствор соли кобальта (10-3М), аликвотные части которого разбавили до 20,00 мл тем же фоном и получили при полярографировании следующие данные:
| Val, мл | |||||
| h, мм |
Определить массовую долю кобальта в сплаве.
Решение. Строим график зависимости высоты волны h от объема раствора соли кобальта Val. По графику определяем, что высоте волны 35 мм соответствует объем соли кобальта, равный 3,5 мл.Содержание кобальта в анализируемой пробе равно:
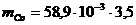 мг
мг
Это количество кобальта находится в 10,00 мл исследуемого раствора, тогда в 100,00 мл его содержится:
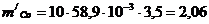 мг,
мг,
а массовая доля кобальта в сплаве равна:
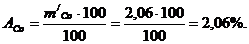
Задача 2. Высоты полярографических волн составили 74 мм для 3 см3 анализируемого раствора сульфата меди и 35 мм для 2 см3 стандартного раствора CuSO4, молярность которого 0,01 г-моль/л. Рассчитать молярность, нормальность, титр раствора CuSO4, а также содержание CuSO4 в нем (г).
Решение. Определим титр и нормальность стандартного раствора. Содержание CuSO4 в одном литре
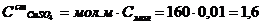 г/л
г/л
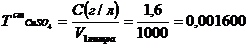 г/мл
г/мл
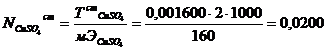 н.
н.
Концентрации исследуемого раствора (М, N, T, p) рассчитываем по методу стандартных растворов, используя уравнение (7):
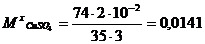 моль/л
моль/л 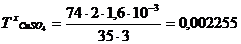 г/мл
г/мл
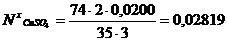 н
н
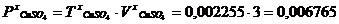 г в анализируемой пробе.
г в анализируемой пробе.
Задача 3. Рассчитать концентрацию раствора (N) кадмия, если при анализе 15 см3 исследуемого раствора высота полярографической волны кадмия (h1) составила 20,5 мм, а после добавления 2 см3 0,053 н стандартного раствора хролида кадмия высота волны увеличилась до 24,3 мм (h2).
Решение. Так как данный анализ проведен методом добавки раствора известной концентрации (стандарта), для определения нормальной концентрации воспользуемся уравнением (8):
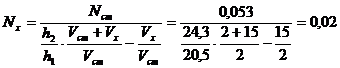 н.
н.
Задача 4. при амперометрическом титровании 10,00 мл исследуемого раствора стандартным раствором калия с титром по цинку 0,002440 г/мл получили следующие результаты:
| VK4Fe(CN)6, мл | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | |
| I, мкА |
Построить кривую титрования в координатах I=f(Vст) и определить концентрацию цинка (мг/л) в анализируемом растворе.
Решение. Построив зависимость I=f(Vст) находим объем затраченный до наступления момента эквивалентности (2,00 мл). Используя расчетные формулы, представленные в работе [7, стр. 71] определяем концентрацию цинка в растворе
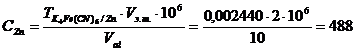 мг/л.
мг/л.
