Электронные формулы элементов и периодическая система Д.И. Менделеева
Рассмотрим связь между электронным строением элементов и их положением в периодической системе (ПС) (табл. 1.1).
Первый период (n = 1, ℓ= 0) прост. В нём всего два элемента: водород Н 1s1 и гелий He 1s2 и т.о. первый энергетический уровень завершён. ПС построена таким образом, что заселение нового энергетического уровня совпадает с началом нового периода.
| Таблица 1.1. Периодическая система элементов Д.И. Менделеева | |||||||||||
| группы | |||||||||||
| I | II | III | IV | V | VI | VII | VIII | ||||
| ПЕРИОДЫ | I | 1H | химические элементы | 2He | |||||||
| 1,00795 | 4,002602 | ||||||||||
| водород | гелий | ||||||||||
| II | 3Li | 4Be | 5B | 6С | 7N | 8O | 9F | 10Ne | |||
| 6,9412 | 9,01218 | 10,812 | 12,0108 | 14,0067 | 15,9994 | 18,9984 | 20,179 | ||||
| литий | бериллий | бор | углерод | азот | кислород | фтор | неон | ||||
| III | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar | |||
| 22,9898 | 24,305 | 26,98154 | 28,086 | 30,9738 | 32,06 | 35,453 | 39,948 | ||||
| натрий | магний | алюминий | кремний | фосфор | сера | хлор | аргон | ||||
| IV | 19K | 20Ca | 21Sc | 22Ti | 23V | 24Cr | 25Mn | 26Fe | 27Co | 28Ni | |
| 39,0983 | 40,08 | 44,9559 | 47,9 | 50,9415 | 51,996 | 54,938 | 55,847 | 58,9332 | 58,7 | ||
| калий | кальций | скандий | титан | ванадий | хром | марганец | железо | кобальт | никель | ||
| 29Cu | 30Zn | 31Ga | 32Ge | 33As | 34Se | 35Br | 36Kr | ||||
| 63,546 | 65,38 | 69,72 | 72,59 | 74,9216 | 78,96 | 79,904 | 83,8 | ||||
| медь | цинк | галлий | германий | мышьяк | селен | бром | криптон | ||||
| V | 37Rb | 38Sr | 39Y | 40Zr | 41Nb | 42Mo | 43Tc | 44Ru | 45Rh | 46Pd | |
| 85,4678 | 87,62 | 88,9059 | 91,22 | 92,9064 | 95,94 | 98,9062 | 101,07 | 102,906 | 106,4 | ||
| рубидий | стронций | иттрий | цирконий | ниобий | молибден | технеций | рутений | родий | палладий | ||
| 47Ag | 48Cd | 49In | 50Sn | 51Sb | 52Te | 53I | 54Xe | ||||
| 107,868 | 112,41 | 114,82 | 118,69 | 121,75 | 127,6 | 126,905 | 131,3 | ||||
| серебро | кадмий | индий | олово | сурьма | теллур | иод | ксенон | ||||
| VI | 55Cs | 56Ba | 57La | 72Hf | 73Ta | 74W | 75Re | 76Os | 77Ir | 78Pt | |
| 132,905 | 137,33 | 138,9 | 178,49 | 180,948 | 183,85 | 186,207 | 190,2 | 192,22 | 195,09 | ||
| цезий | барий | лантан × | гафний | тантал | вольфрам | рений | осмий | иридий | платина | ||
| 79Au | 80Hg | 81Tl | 82Pb | 83Bi | 84Po | 85At | 86Rn | ||||
| 196,967 | 200,59 | 204,37 | 207,2 | 208,9 | |||||||
| золото | ртуть | таллий | свинец | висмут | полоний | астат | радон | ||||
| VII | 87Fr | 88Ra | 89Ac** | 104Rf | 105Db | 106Sg | 107Bh | 108Hs | 109Mt | 110Ds | |
| франций | радий | актиний | резерфордий | дубний | сиборгий | борий | хассий | мейтнерий | дармштадтий |
ЛАНТАНОИДЫ* И АКТИНОИДЫ**
| 58Ce | 59Pr | 60Nd | 61Pm | 62Sm | 63Eu | 64Gd | 65Tb | 66Dy | 67Ho | 68Er | 69Tm | 70Yb | 71Lu |
| 140,9 | 150,4 | 151,9 | 157,3 | 158,9 | 162,5 | 164,9 | 167,3 | 168,9 | 174,9 | ||||
| церий | празеодим | неодим | прометий | самарий | европий | гадолиний | тербий | диспрозий | гольмий | эрбий | тулий | иттербий | лютеций |
| 90Th | 91Pa | 92U | 93Np | 94Pu | 95Am | 96Cm | 97Bk | 98Cf | 99Es | 100Fm | 101Md | 102No | 103Lr |
| торий | протактиний | уран | нептуний | плутоний | америций | кюрий | берклий | калифорний | эйнштейний | фермий | менделевий | нобелий | лоуренсий |
Во втором периоде (n = 2, ℓ = 0, 1) идёт заполнение
второго энергетического уровня: сначала более низких поэнергии s- орбиталей (s- элементы литий Li [He]2s1 и
бериллий Be 2s2), затем последовательно трёх p- орбиталей (р-элементы от бора до неона с общей электронной конфигурацией [He]2s22р1-6).
Число элементов во втором периоде – 8 − соответствует максимально возможному числу электронов во втором слое (два s- + шесть р-).
В третьем периоде заполняется третий слой (n = 3, l = 0, 1`, 2)), состоящий из 3s-, 3p- и 3d- подуровней. Однако, в нём всего восемь элементов − электронных аналогов второго периода: два s- (Na [Ne]3s1 и Mg 3s2) и шесть р- элементов от алюминия Al до аргона Ar, 13 - 18Э[Ne]3s23р1-6 ). Благородный газ аргон 18Аr [Ne]3s2 3p6 завершает третий период, при этом пять d– орбиталей (ℓ = 2) третьего энергетического уровня остаются незаселёнными.
Следующие за аргоном калий и кальций попадают в четвёртый период. У них электроны заселяют 4s- орбиталь. Появление 4s- электронов при наличии свободных 3d- орбиталей обусловлено экранированием ядра плотным 3s23p6 электронным слоем с малым радиусом (Аr 3s23p6). В связи с отталкиванием от этого слоя внешних электронов для калия и кальция реализуются 19К[18Ar]3d04s¹ - и 20Ca[Ar]3d04s²- состояния. Сходство К и Са с Na и Mg соответственно, являясь чисто «химическим» обоснованием, подтверждается также электронными спектрами.
При дальнейшем увеличении заряда ядра у следующих после кальция элементов от Sc до Zn 3d- состояние энергетически более выгодно, чем 4р, и это определяет заселение 3d- подуровня (рис. 1.3).
Из анализа зависимости энергии электрона от порядкового номера элемента В.М. Клечковский сформулировал правило, согласно которому, сначала заполняются орбитали с меньшей суммой (n + ℓ). При равенстве сумм сначала заполняется подуровень с меньшим n. Так, у К и Са заполняется 4s – орбиталь (n + l = 4 + 0 =4), а у Sc один электрон занимает 3d – орбиталь (n + l = 3 + 2 = 5), а не 4р (n + l = 4 + 1 = 5).
В ПС появляется первый d-элемент Sc [Ar] 3d14s², таким образом, d-орбиталь, отвечающая 3му энергетическому слою, начинает заселятьсялишьв IV периоде, т.е. с отставанием на 1 период. Соответственно 4d-орбиталь будет заселяться в 5 периоде, 5d- в шестом, 6d- в седьмом.
Элементы, у которых заполняются внутренние d- оболочки, образуют вставные декады и называются d- элементами.
С. 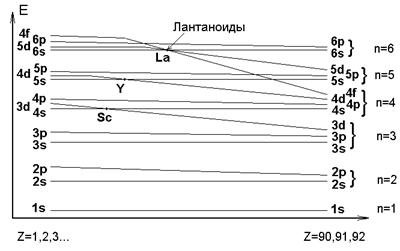 Рис. 1.3. Приближенные энергетические уровни в зависимости от атомных номеров элементов
Рис. 1.3. Приближенные энергетические уровни в зависимости от атомных номеров элементов
Относительная энергия и заселение подуровней определяется их взаимным влиянием и зависит от заряда ядра Z. Так, для всех элементов с Z ≥ 21 энергия 3d- подуровня становится ниже, чем 4s- (рис.1.3), и, несмотря на превосходящую проникающую способность 4s- электронов, большая часть плотности вероятности для 4s- орбитали оказывается в среднем дальше от ядра, чем у 3d- орбитали. Другими словами энергия заселённой 3d- орбитали, в соответствии с её положением, в общем случае ниже энергии 4s- орбиталии существенно ниже энергии 4р- орбитали.
Однако у Sc 3d- и 4s- орбитали имеют ≈ равную энергию и Sc проявляет единственно устойчивую степеньокисления +3: Sc+3 [Ar]3d04s0.
От скандия до цинка идёт постепенное заселение 3d- подуровня, сопровождающееся понижением энергии и, как следствие, уменьшением химической активности 3d-электронов.
Во внешем слое у всех d- элементов заполнен 4s - подуровень. Поэтому в четвертом периоде в ряду Sс − Ζn все десять 3d- элементов – металлы с низшей степенью окисления, как правило, 2 за счет внешних 4s- электронов. Общая электронная формула этих элементов Э[18Ar]3d1–10 4s1–2]. Для хрома и меди наблюдается проскок (или провал) одного 4s- электрона на 3d – подуровень: 24Cr [18Ar]3d54s1, 29Сu [18Ar]3d104s1, что объясняется стабильностью наполовину и полностью заполненного 3d- подуровня.
Образование катионов d- элементов связано с потерей прежде всего внешних ns- электронов с более высокой энергией (рис. 1.3.) и только затем (n–1)d- электронов. Например:
– 2ē – 1 ē
22Ti [18Ar]3d24s2 → Ti2+ 3d2 → Ti 3+ 3d1
– 2 ē – 2 ē
25Mn [18Ar]3d54s2 → Mn2+ 3d5 → Mn4+ 3d3
Далее в четвертом периоде после десяти d- элементов появляются 4р- элементы от 31Gа [18Ar]3d10 4s24р1 до 36Кr [18Ar]3d104s24p6. Заполненный десятью электронами предшествующий 3d- подуровень у них невалентен. Благородный газ криптон завершает четвёртый период. Незаселёнными остаются 4d- и 4f- подуровни. Всего в четвёртом периоде восемнадцать элементов.
В пятом периоде расположены также 18 элементов − электронных аналогов элементов 4 периода: два − 5s-, десять − 4d- (39 -48 Э [36Kr] 4d1-10 (4f 0) 5s1-2) и шесть − 5р- (49 -54 Э [36Kr] 4d10 5s25р1-6) элементов.
Однако, в электронных конфигурациях, проявляемых степенях окисления и свойствах 3d- и 4d- элементов наряду со сходством наблюдаются некоторые различия из-за наличия у последних вакантного 4f- подуровня. Это ослабляет межэлектронное взаимодействие на 4d- подуровне и приводит к провалу на него электронов с 5s- орбитали у всех (кроме технеция, 43Тс[36Kr]4d54f05s2]) d- элементов 5 периода, начиная с ниобия. При этом у Nb, Mo, Ru, Ro, Ag с 5s- на 4d- орбиталь переходит один из s- электронов, а у палладия сразу оба: 46Pd [36Kr]4d104f05s0. Таким образом, палладий является единственным элементом ПС, у которого отсутствуют электроны, отвечающие за свой период. Палладий относится к редкоземельным металлам и, подобно никелю, чаще проявляет степень окисления +2.
Следующее за палладием серебро 47Ag [36Kr]4d10 (4f 0)5s1 также испытывает влияние 4f 0- подуровня, которое проявляется в особой устойчивости для серебра степени окисления +1 → Ag+1 [36Kr]4d10 (4f0)5s0.
Кадмий 48Сd[36Kr]4d105s2 ─ последний из 4d- элементов.
Пятый период завершается шестью р-элементами 49-54Э [36Kr]4d10 5s25p1-6. Вакантными остаются 4f-, 5d-, и 5f- подуровни.
Шестой период также начинается с двух s- элементов: цезия 55Cs [54Xe]6s1 и бария 56Ва [54Xe]6s2. В нём с отставанием на два периоданачинает заселяться f- орбиталь четвёртого слоя. Однако, в лантане 57La[54Xe]5d16s2, стоящем в ПС после бария, 4f- орбиталь энергетически менее выгодна, чем 5d (влияние экранирования и межэлектронного взаимодействия), и первый f- электрон появляется только у церия: 58Се[54Xe]4f1 5d16s2, причём 4f- и 5d- орбитали атома церия имеют приблизительно равную энергию. После церия возросший заряд ядра стабилизирует 4f- орбиталь и празиодиму соответствует электронная конфигурация 59Pr [54Xe]
4f 35d06s2. У последующих элементов продолжается заполнение 4f-орбиталей. У атома гадолиния 64Gd[54Xe]4f 7 5d16s2 один электрон заселяет 5d- орбиталь, т.к. при этом сохраняется устойчивая конфигурация f 7.
Элементы ПС, у которых наблюдается заполнение электронами f- орбиталей, называют f- элементами. В шестом периоде мы имеем 14 f- элементов от церия до лютеция 71Lu[54Xe] 4f145d16s2, хотя последний правильнее относить к d- элементам, так как он не содержит на f- орбитали валентных электронов.
Все 4f- элементы, включая лютеций, по своим свойствам сходны с лантаном и поэтому получили название лантаноидов(подобные лантану) или лантанидов(следующие за лантаном). Поскольку идет заполнение глубоколежащего невалентного (n‑2)f- подуровня, свойства этих элементов очень близки. Электронная конфигурация атомов лантаноидов может быть выражена общей формулой 58-71Э[54Xe]4f 1-145d0-16s2. В короткопериодном варианте таблицы они отнесены к 3 группе (подгруппа скандия) и помещены в низу таблицы. Это металлы с устойчивой степенью окисления +3.. В некоторых случаях, в основном, когда на 4f- орбитали образуется устойчивая электронная конфигурация 4f 0, 4f 7, 4f 14, лантаноиды могут проявлять степени окисления +2 и +4.
При образовании катионов 4f – элементов электроны снимаются сначала с внешнего 6s-, затем с предвнешнего 5d- и только потом с более глубокого 4f- подуровня, что согласуется с их энергиями (см. с.19, рис. 1.3).
65Tb [54Xe] 4f 95d06s2 → Tb+3 4f 85d06s0 → Tb+4 4f 75d06s0
После лютеция в шестом периоде от гафния 72Hf [54Xe] 4f 145d2 6s2 до ртути 80Hg [54Xe] 4f 145d10 6s2 продолжается заполнение 5d- орбиталей. У d- элементов шестого периода наблюдается большое сходство с соответствующими d- элементами пятого периода из-за близости орбитальных радиусов под влиянием 4f- сжатия. В то же время следует отметить некоторые особенности в электронных конфигурациях и свойствах 5d- элементов, объясняющиея влиянием полностью заселённого электронами 4f- подуровня. Так, в отличие от 4d- элементов, у 5d- элементов практически отсутствуют провалы электронов с внешнего s- на предвнешний d- подуровень. Их нет у W, Os, Ir. Исключение составляют платина 78Pt [54Xe] 4f 145d9 6s1 и золото Au[54Xe] 4f 145d106s1.
Влиянием заполненного 4f- подуровня и близостью энергий 5d- и 6s- орбиталей в результате проникновения последних во внутренние слои можно объяснить, например, что для Hf, Ta, W, Re высшая степень окисления − единственно устойчивая (Hf+4, Ta+5, W+6, Re+7).
Устойчивость высших и нестабильность низших степеней окисления переходных металлов возрастает в группе: 3d < 4d < 5d.
Завершают шестой период шесть р-элементов: талий, свинец, висмут, полоний, астат, радон с общей электронной конфигурацией 81-86Э[54Xe] 4f 145d106s2р1-6. В шестом периоде – 32 элемента.
В седьмом периоде расположены два s- (Fr, Ra), четырнадцать f- (Th – Lr), десять d-(89Ac и 104Rf -109Mt, 110-112Э) элементов.
f-Элементы 7 периода объединены в семейство актиноидов Th – Lr. В отличие от лантаноидов для элементов от тория 90Th до кюрия 96Cm невозможно однозначно определить электронную конфигурацию из-за энергетической близости 5f- и 6d- подуровней. В атомах этих актиноидов происходит своеобразное «соревнование» в заполнении 5f- и 6d- орбиталей. Они поливалентны. Их можно отнести как к f-,так и к d- элементам.
Все элементы седьмого периода радиоактивны. Время полураспада d- элементов измеряется секундами. Они получены искусственным путём на ядерных установках.
В настоящее время известны шесть р- элементов с номерами 113-118, пока ещё не признанные официально. Седьмой период считается незавершённым.
Таким образом, в Периодической системе Д.И. Менделеева элементы расположены в порядке возрастания заряда ядра (порядкового номера) атома. Заселение электронами атомных орбиталей происходит в порядке возрастания их энергий. В некотором приближении можно составить следующую последовательность заполнения подуровней:
Период I │ II │ III │ IV │V
Орбитали 1s │< 2s < 2p │ < 3s < 3p │< 4s ≈ 3d < 4p│‹5s ≈ 4d < 5p ‹
К-во эл. (2s)│(2s +6p)=8│ 8 │ (8+10d)=18 │ 18
Период │ VI │ VII
Орбитали │< 6s ≈ 4f ≈ 5d < 6p│< 7s ≈ 5f ≈ 6d < 7p
К-во эл-тов (18+14f)=32 не завершён
Представленный ряд легко разбить на отдельные секции (периоды), в результате чего получим упрощенную схему Периодической системы. Анализируя её, можно подвести некоторые итоги:
1. Номер периода совпадает со значением главного квантового числа внешнего энергетического уровня.
2. Начало каждого периода совпадает с началом нового энергетического уровня.
3. Каждый период начинается с двух s- элементов.
4. Каждый период (кроме первого) завершается шестью р- элементами.
5. Заполнение s- и p- орбиталей происходит во внешнем валентном слое, совпадающем с № периода.
6. d- Подуровень заполняется с отставанием на 1 период (3d- в 4-м периоде, 4d – в пятом, 5d – в шестом и т.д.).
7. d-Элементы в ПС всегда предшествуют р-элементам.
8. f- Подуровень заполняется с отставанием на 2 периода (4f- в шестом, 5f- в седьмом периоде).
9. f- Элементы в ПС располагаются перед d- элементами.
10. Энергии (n-2)f-, (n-1)d- и ns-подуровней примерно равны и всегда меньше энергии р- подуровня.
11. В первом периоде расположены два элемента.
Во втором – 8 элементов (два s- и шесть р-элементов, №/№ 3 – 10)
В третьем – 8 элементов (два s- и шесть р-элементов, №/№ 11 – 18)
В четвёртом – 18 элементов (два s-, шесть р- и десять d- элементов, №/№ 19 – 36).
В пятом - 18 элементов (два s-, шесть р- и десять d- элементов, №/№ 37 – 54).
В шестом - 32 элемента (два s-, шесть р-, десять d- и 14 f- элементов, №/№ 55 – 86).
Седьмой период не завершён.
Данная схема ПС (ряд орбиталей) согласуется с эмпирическим правилом Клечковского. Правило Клечковского не является строгим и применять его следует с большой осторожностью.
Электронные формулы атомов и ионов элементов подтверждены спектроскопическими исследованиями (ИК-, ЭПР-, ЭСР-, ЯГР- и др.).
