Геометрические и энергетические характеристики атомов
Атомный радиус.Атом не имеет строго определенных границ. За его радиус принимается расстояние от ядра до главного максимума плотности внешних электронных оболочек. С увеличением заряда ядра в периодах атомный радиус немонотонно уменьшается, а в группах увеличивается.
Энергия ионизации Еi –это энергия, необходимая для отрыва наиболее слабо связанного электрона от атома, количественно выражается в кДж/моль или эВ. Чем меньше энергия ионизации, тем легче атом отдает электрон при образовании химической связи, т.е. элемент является более сильным восстановителем. Поэтому восстановительная способность нейтральных атомов с ростом заряда ядра в периоде уменьшается, в главных подгруппах растет.
Энергия сродства к электрону Еср –энергия, выделяющаяся при присоединении электрона к нейтральному атому, количественно выражается в кДж/моль или эВ. Она определяет окислительные свойства несвязанных атомов. Чем больше электронное сродство, тем более сильным окислителем является данный элемент. Окислительной способностью не обладают нейтральные атомы с устойчивыми конфигурациями s2, s2р6. У остальных элементов в таблице Д.И. Менделеева окислительная способность нейтральных атомов повышается слева направо и снизу вверх.
Электроотрицательностью элемента (ЭО)называют меру относительной способности атомов оттягивать на себя электроны при образовании химической связи. Она пропорциональна как энергии ионизации, так и энергии сродства к электрону. Имеется несколько шкал электроотрицательности. Согласно Р. Малликену, абсолютная электроотрицательность равна полусумме энергии ионизации и сродства к электрону:
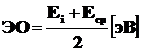 ,
,
Л. Полинг ввел относительную шкалу электроотрицательности (ОЭОR):
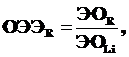
С ростом заряда в периодах электроотрицательность в общем растет, а в подгруппах падает.
Химическая связь.
Под химической связью понимают результат взаимодействия двух и более атомов, приводящий к образованию устойчивой многоатомной системы.
Важнейшими видами химической связи являются: ковалентная, ионная водородная, металлическая, межмолекулярная.
При образовании ковалентной связи между атомами их электроны обобщаются и локализуются между ними.
Число общих электронных пар,соединяющих два атома,определяет кратность химической связи.
Длина химической связи характеризует межъядерное расстояние в молекуле. Чем больше кратность связи, тем меньше ее длина при прочих равных условиях.
Прочность химической связи (энергия разрыва или диссоциации) – это количество энергии, необходимой для ее разрыва. Чем короче связь, тем больше энергия ее разрыва в том случае, если сравниваются однотипные связи.
Химическая связь, образованная при перекрывании атомных орбиталей (АО), расположенных вдоль прямой линии, проведенной через ядра взаимодействующих атомов, называется σ (сигма)-связью. Между двумя атомами в молекуле возможна только одна σ–связь. Углы между σ–связями называются валентными углами.
При перекрывании АО, расположенных перпендикулярно или под иными углами к σ-связи и параллельно друг к другу происходит образование π (пи) и δ (дельта)-связей. Перекрывание АО при этом меньше, чем при σ, поэтому π- и δ-связи, как правило, слабееσ-связи.
Под направленностью химической связи понимают валентные углы, которые образуются между химическими связями в молекулах, состоящих из трех и более атомов. Для предсказания геометрического строения молекул типа АВn, где n>1, и значений валентных углов применяют идею гибридизации атомных орбиталей.
Подполярностью химической связипонимают асимметрию в распределении электронной плотности между атомами, образующими химическую связь.
В двухатомных молекулах простых веществ (таких, как Н2, О2, Cl2 и др.) электронная плотность около обоих атомов одинакова, а сама связь является неполярной.
Если связь образована атомами разных элементов, то один из них, как правило, притягивает общую электронную пару сильнее. Тогда симметрия распределения зарядов нарушается и полюс отрицательных зарядов не совпадает с положительным полюсом. Вследствие этого связь становится полярной.
С увеличением разности электроотрицательностей (Δ ЭО), участвующих в образовании связи атомов, возрастает эффективный заряд на атомах, т.е. возрастает степень ионности связи. Для 100% степени ионности связи ΔЭО, рассчитанная по относительной шкале электроотрицательностей элементов, должна быть равной 3,5. При ΔЭО>1,9, когда эффективный заряд атомов становится больше ±0,5, вполне допустимо рассматривать атомы как ионы с целочисленными зарядами, а связь между ними считать ионной.
Химическая связь считается локализованной (ограниченной определенным местом), если осуществляющие ее электроны принадлежат только двум связываемым атомам. Связь является нелокализованной,если электрон или электроны осуществляют связь более, чем между двумя атомами. Типичным примером нелокализованной связи является металлическая химическая связь,т.к. электроны, осуществляющие связь, обобществлены («электронный газ») и перемещаются по всему объему металла, в целом электронейтральному.
Водородная связь характерна для атома водорода, связанного непосредственно с наиболее электроотрицательными элементами F, N, O и другими. Она может быть межмолекулярной и внутримолекулярной. В первом случае связь возникает между водородом и электроотрицательным элементом другой молекулы, а внутримолекулярная – между атомами этих элементов в одной молекуле.
Пример 3. Определите тип химической связи в молекулах Cl2, НCl, КCl, ЅО2, Н2Ѕ.
Решение.Молекула Cl2 – двухатомная молекула простого вещества. Такие молекулы являются неполярными и химические связи в них также неполярные.
Для определения типа внутримолекулярной химической связи в других веществах находим разности относительных электроотрицательностей входящих в них элементов, используя прил. 2, и сравниваем полученный результат с нормируемым значением для ионной связи ΔЭО>1,9.
НCl: Δ ЭО = 3,0-2,1=0,9 (результат меньше 1,9, следовательно для данного соединения характерна ковалентная полярная связь);
КCl: Δ ЭО = 3,0-0,8=2,2 (>1,9, связь ионная);
ЅО2: Δ ЭО =3,5-2,5 =1,0 (<1,9, ковалентная полярная связь)
Н2Ѕ: Δ ЭО =2,5-2,1=0,4 (<1,9, ковалентная полярная связь)
Задачи к главе 2
Й уровень
41-45. Составьте электронную формулу атома элемента с порядковым номером Z. К какому электронному семейству принадлежит этот элемент? Составьте уравнение β--распада ядра изотопа этого элемента с массовым числом А. Учесть, что в задаче 42 изотоп распадается с выделением двух β-частиц:
| Задачи | |||||
| Z | |||||
| А |
46-50. Укажите в периодической системе элемент, валентные электроны которого имеют конфигурацию Z. Напишите полную электронную формулу этого элемента. Составьте уравнение β+-распада ядра изотопа этого элемента с массовым числом А:
| Задачи | |||||
| Z | 3s23p1 | 3d54s2 | 5s2 | 3d14s2 | 4s24p2 |
| А |
51-55. Какие значения квантовых чисел n, l, m1, ms, имеют валентные электроны элемента А? Напишите электронную формулу элемента:
| Задачи | |||||
| A | 37Rb | 4Be | 31Ga | 20Ca | 3Li |
56-60. Составьте уравнение реакции ядерного обмена согласно схеме 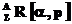 для изотопа элемента, содержащего Z протонов с массовым числом А.
для изотопа элемента, содержащего Z протонов с массовым числом А.
| Задачи | |||||
| Z | |||||
| А |
Й уровень
61-65. Определите тип химической связи в молекуле вещества А, изобразите ее структурную формулу:
| Задачи | |||||
| A | Аl2О3 | СS2 | СBr4 | РН3 | СаF2 |
66-70. Руководствуясь периодической системой, укажите символ химического элемента, иону которого с зарядом А соответствует электронная конфигурация валентных электронов Б. Для найденного элемента приведите его электронную формулу:
| Задачи | |||||
| А | 2+ | 1- | 3+ | 3- | 2+ |
| Б | 3d5 | 2s22p6 | 3d5 | 4s24p6 | 3d2 |
71. По значениям энергии ионизации атомов (эВ) определите, какой из приведенных элементов имеет наиболее ярко выраженные восстановительные свойства: К (4,34), Са (6,11), Rb (4,18), Sr (5,69).
72. Энергия ионизации атомов I, Cl, Br, F имеет значения (эВ): 11,84; 12,97; 10,45; 17,42. Атому какого элемента соответствует значение энергии ионизации 10,45 эВ?
73. По значению энергии сродства к электрону (эВ) выберите элемент, у которого наиболее ярко выражены окислительные свойства: Br (3,37), О (1,47), С (1,27), Cl (3,61).
74. Энергия ионизации атомов Mg, Al, Na, Cl имеет значения (эВ): 5,99; 5,14; 12,97; 7,65. Атому какого элемента соответствует значение энергии ионизации 12,97 эВ?
75. По значениям энергии ионизации атомов (эВ) определите, какой из приведенных элементов имеет наиболее ярко выраженные восстановительные свойства: К (4,34), Al (5,99), Ni(7,64), Sс (6,56).
3-й уровень
76-80. Определите число связей и их характер в соединении А:
| Задачи | |||||
| А | SiH4 | SiO2 | K2SiF6 | С2Н6 | СCl4 |
81.Как и почему изменяется длина связи в ряду: CF4, CCl4, CBr4?
82. Сколько σ- и π-связей имеется в молекулах С2Н2 и РН3?
83. Составьте электронную формулу хрома, содержащегося в соединении Cr2(SO4)3.
84.Определите тип гибридизации орбиталей атома металла в молекуле хлорида кальция и изобразите геометрическую форму молекулы.
85. Определите тип гибридизации орбиталей атома азота в ионе аммония и изобразите геометрическую форму частицы.
86. При бомбардировке некоторого изотопа нейтронами происходит поглощение одного нейтрона и, впоследствии, испускание двух высокоэнергетических электронов. При этом образуется изотоп 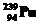 . Какие материнские ядра участвуют в обменной реакции? Составить полное и краткое уравнения этой реакции.
. Какие материнские ядра участвуют в обменной реакции? Составить полное и краткое уравнения этой реакции.
87. Какую ускоренную частицу поглощает материнское ядро 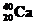 , если при этом образуется дочернее ядро
, если при этом образуется дочернее ядро 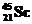 и два высокоэнергетических протона? Составить полное и краткое уравнения этой реакции.
и два высокоэнергетических протона? Составить полное и краткое уравнения этой реакции.
88. Сколько и каких высокоэнергетических частиц выбрасывает ядро 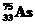 , поглотившее четыре нейтрона, образуя стабильный изотоп
, поглотившее четыре нейтрона, образуя стабильный изотоп 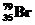 ? Составить полное и краткое уравнения этой реакции.
? Составить полное и краткое уравнения этой реакции.
89. Изотоп 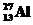 , подвергаясь α-облучению, участвует в обменной реакции:
, подвергаясь α-облучению, участвует в обменной реакции: 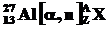 . Образующиеся при этом ядра
. Образующиеся при этом ядра 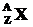 являются радиоактивными (искусственная радиация) и подвергаются β+-распаду, выбрасывая один высокоэнергетический позитрон. Изотоп какого элемента образуется из алюминия в конечном итоге? Составить уравнения всех описанных реакций.
являются радиоактивными (искусственная радиация) и подвергаются β+-распаду, выбрасывая один высокоэнергетический позитрон. Изотоп какого элемента образуется из алюминия в конечном итоге? Составить уравнения всех описанных реакций.
90. Изотоп ртути 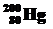 участвует в двух обменных ядерных реакциях:
участвует в двух обменных ядерных реакциях:
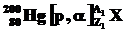 и
и 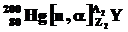 . В какой их этих реакций образуется β-радиоактивный изотоп? Составить уравнения обменных реакций и схему β--распада образующегося в одной из них изотопа, обладающего искусственной радиоактивностью.
. В какой их этих реакций образуется β-радиоактивный изотоп? Составить уравнения обменных реакций и схему β--распада образующегося в одной из них изотопа, обладающего искусственной радиоактивностью.
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
Для прогнозирования физико-химических процессов очень важно заранее знать, возможна ли реакция между теми или иными веществами, приведенными в химический контакт. В случае, если реакция в данных условиях невозможна, то какие для ее протекания необходимы температура и давление, каков при этом окажется состав равновесной смеси и давление. Не менее важны сведения о тепловых эффектах химических реакций, особенно для оценки теплотворной способности различных видов топлива. Или, например, почему одновременно могут протекать два противоположных процесса – фотосинтез и горение? Ответы на все эти вопросы позволяет найти химическая термодинамика.
Термодинамика – наука о превращениях энергии. Химическая термодинамика применяет законы термодинамики к свойствам и поведению веществ в химических реакциях. Они определяются через изменение соответствующих термодинамических параметров состояния системы, к которым относятся:
- внутренняя энергия U – полная энергия частиц, составляющих данное вещество; она слагается из кинетической энергии поступательного, колебательного и вращательного движения частиц, а также потенциальной энергии сил притяжения и отталкивания, действующих между частицами;
- энтальпия системы Н – термодинамическая функция, характеризующая систему, находящуюся при постоянном давлении, Н=U+pV, где p и V – соответственно давление и объем системы;
- энтропия S и ее изменение DS, являющиеся мерой структурной неупорядоченности системы, Дж/(моль×К);
- свободная энергия Гельмгольца (F) и ее изменение D F, которые являются рой химического сродства и критерием самопроизвольного протекания изохорно-изотермических процессов, кДж/моль;
- свободная энергия Гиббса G и ее изменение DG, которые являются мерой химического сродства и критерием самопроизвольного протекания изобарно-изотермических процессов, кДж/моль.
Соотношения между перечисленными параметрами можно выразить следующей схемой:


H (ΔH)

U (∆U) РV (Р∆V)


ТS (Т∆S) G (∆G)


ТS (Т∆S)F(∆F)РV (Р∆V)




Из данной схемы можно легко построить любое термодинамическое уравнение, например:
∆F = ∆Н - Т∆S - Р∆V.
Термохимия
Термохимия изучает тепловые эффекты химических процессов. Протекание химических реакций всегда связано с выделением или поглощением теплоты. Химические реакции, в результате которых выделяется теплота, называются экзотермическими, химические реакции, протекающие с поглощением теплоты, называются эндотермическими. При химических процессах может выделяться или поглощаться не только тепловая, но и другие виды энергии: электрическая, световая, механическая и др. Различные виды энергии, выделяемой или поглощаемой в ходе процесса, пересчитывают на тепловую энергию, выражая ее количество в килоджоулях (кДж).
Количество энергии относят к такому числу молей вещества, которое указано в уравнении реакции, и называют его тепловым эффектом (теплотой) Q реакции. Уравнения реакций, в которых указываются тепловые эффекты, называются термохимическими. Так как тепловой эффект зависит от состояния вещества, то в термохимических уравнениях указывают их фазовое состояние.
Для реакций, протекающих при постоянном давлении и постоянной температуре, тепловой эффект равен изменению энтальпии с противоположным знаком: Qр =-DН, кДж/моль, а при постоянном объеме он равен изменению внутренней энергии с противоположным знаком: QV =-D U.
Тепловой эффект реакции образования одного моля вещества из простых веществ называется теплотой образования DН данного вещества. Энтальпию образования 1 моля сложного вещества из простых веществ, измеренную при температуре 298 К и давлении 101,325 кПа, называют стандартной энтальпией образования 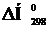 , кДж/моль. Энтальпии простых веществ (О2, Н2, S и т.п.) условно принимают равными нулю.
, кДж/моль. Энтальпии простых веществ (О2, Н2, S и т.п.) условно принимают равными нулю.
Термохимические расчеты осуществляют, применяя следствие из закона Гесса: тепловой эффект химической реакции DНх.р равен сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ, с учетом коэффициентов перед формулами этих веществ в реакции:
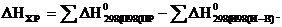 .
.
Пример 1. Вычислить тепловой эффект, написать термохимическое уравнение горения 1 моля метана и рассчитать количество теплоты, которое выделится при сгорании 10 л CH4.
Решение.Составим термохимическое уравнение реакции
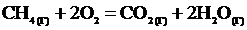
Выпишем стандартные теплоты образования 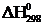 веществ (прил. 3):
веществ (прил. 3):
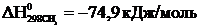 ,
,
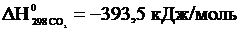 ,
,
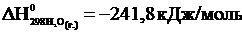 .
.
Тепловой эффект реакции вычислим, используя следствие закона Гесса:
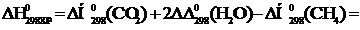
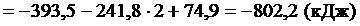
При сжигании 22,4 л выделяется 802,2 кДж, при сжигании 10 л выделяется х кДж. Составим и решим пропорцию:
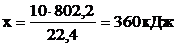 .
.
Ответ: 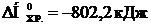 , при сжигании 10 л метана выделяется 360 кДж.
, при сжигании 10 л метана выделяется 360 кДж.
Химическое сродство
Чтобы понимать химические процессы и управлять ими, необходимо знать ответ на вопрос: каковы движущие силы и критерии самопроизвольных химических процессов. Одной из движущих сил химической реакции является уменьшение энтальпии системы, т. е. экзотермический тепловой эффект реакции. Как показывает опыт, большинство экзотермических (DН<0) реакций протекают самопроизвольно. Но кроме энтальпийного фактора имеется другая движущая сила самопроизвольного процесса. Это стремление системы к переходу от более упорядоченного состояния к менее упорядоченному. Мерой неупорядоченности состояния системы служит термодинамическая функция, получившая название энтропии. Состояние системы можно характеризовать микросостояниями составляющих ее частиц. Число микросостояний системы называется термодинамической вероятностью системы W. Величина, равная RlnW= S, называется энтропией системы, отнесенной к одному молю вещества. Как и молярная постоянная R, энтропия имеет единицу измерения Дж/(моль×К). Энтропия вещества в стандартном состоянии называется стандартной энтропией 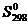 .
.
Т.к. энтропия является функцией состояния системы, то для вычислений изменения стандартной энтропии химической реакции DSх.р применяют следствие из закона Гесса (с учетом стехиометрических коэффициентов):
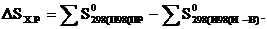 .
.
Таким образом, в химических процессах проявляются две тенденции: а) стремление к образованию прочных связей между частицами, к возникновению более сложных веществ, сопровождающееся понижением энергии системы (энтальпийный фактор); б) стремление к разъединению частиц, к беспорядку, характеризуемое возрастанием энтропии (энтропийный фактор).
Для изохорно-изотермических процессов возможность самопроизвольного протекания определяется через объединяющий эти два фактора изохорно-изотермический потенциал или энергию Гельмгольца:
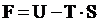 ,
,
изменение этой величины ΔF равно
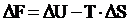 .
.
В системах, находящихся при постоянной температуре, самопроизвольно могут протекать только те процессы, которые сопровождаются уменьшением величины F при постоянном объеме.
Для изобарно-изотермических процессов энтальпийный и энтропийный факторы объединены функцией, называемой свободной энергией Гиббса или химическим сродством G. Ее рассчитывают как равнодействующую вышеупомянутых факторов реакции:
 |
Свободная энергия Гиббса связана с энтальпией и энтропией следующим соотношением:
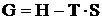 .
.
Изменение свободной энергии Гиббса ΔG является движущей силой реакции (разностью химических потенциалов) подобно ЭДС в электрических процессах (ΔЕ) или перепаду давлений в гидравлических процессах (ΔР):
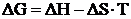
и может быть рассчитано по следствию из закона Гесса:

В системах, находящихся при постоянной температуре, самопроизвольно могут протекать только те процессы, которые сопровождаются уменьшением величины G при постоянном давлении.
Найдя величину ΔG0х.р, можно вычислить константу химического равновесия реакции Kp, являющуюся количественной характеристикой положения равновесия (предел протекания реакции):
ΔG = -RTlnKp.
Для окислительно-восстановительных реакций (в том числе и лежащих в основе работы гальванических элементов) через свободную энергию Гиббса можно определить разность окислительно-восстановительных потенциалов или ЭДС элемента (ΔЕ):
ΔG = -nFΔЕ,
где n – число принятых или отданных электронов в окислительно-восстановительном процессе; F – число Фарадея, F = 96483 Кл/моль; ΔЕ – разность окислительно-восстановительных потенциалов или ЭДС элемента, В.
Пример 2.Может ли реакция I2(K) +H2S (Г)=2HI(Г)+S(K) при стандартных условиях протекать самопроизвольно в прямом направлении. Как скажется повышение температуры на направлении протекания этой реакции?
Решение. Выпишем значения 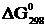 для веществ, участвующих в реакции (прил. 3):
для веществ, участвующих в реакции (прил. 3):
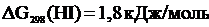 ;
;
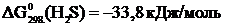 ,
,
тогда 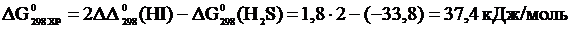 .
.
Положительный знак 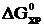 означает, что эта реакция при Т=298 К и р=101,325 кПа самопроизвольно протекать не может. В этой реакции число молей веществ в газообразном состоянии возрастает,
означает, что эта реакция при Т=298 К и р=101,325 кПа самопроизвольно протекать не может. В этой реакции число молей веществ в газообразном состоянии возрастает, 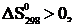 т.е. в уравнении
т.е. в уравнении 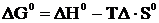 член ТDS-отрицателен. Следовательно, с повышением температуры значение
член ТDS-отрицателен. Следовательно, с повышением температуры значение 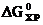 будет уменьшаться. Это означает, что повышение температуры будет благоприятствовать протеканию реакции в прямом направлении.
будет уменьшаться. Это означает, что повышение температуры будет благоприятствовать протеканию реакции в прямом направлении.
Задачи к главе 3
Й уровень
91-95. Рассчитайтестандартный тепловой эффект реакции, предварительно подобрав коэффициенты в уравнении, и установите, является ли реакция экзо- или эндотермической. Стандартные энтальпии образования реагентов А, В и продуктов С и D взять из прил.3:
Задачи Реакции
A B C D
 91 CuCl2(т) + H2O(г) CuO(т) + HCl(г)
91 CuCl2(т) + H2O(г) CuO(т) + HCl(г)
 92 Al2(SO4)3(т) Al2O3(т) + SO3(г)
92 Al2(SO4)3(т) Al2O3(т) + SO3(г)
 93 CS2(ж) + O2(г) CO2(г) + SO2(г)
93 CS2(ж) + O2(г) CO2(г) + SO2(г)
 94 HF(г) +N2(г) NF3(г) + H2(г)
94 HF(г) +N2(г) NF3(г) + H2(г)
 95Na2SO3(т)Na2SO4(т) + Na2S(т)
95Na2SO3(т)Na2SO4(т) + Na2S(т)
96-100По термохимическому уравнению взаимодействия реагентов А и В, рассчитайте стандартную энтальпию образования продукта D. Известны (прил. 3) стандартный тепловой эффект химической реакции 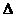 Н°х.р. и стандартные энтальпии образования реагентов
Н°х.р. и стандартные энтальпии образования реагентов 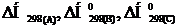 :
:
| Задачи | Реакции | |||||
| А | В | С | D | 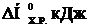 | ||
 96 96 | Na2O(т) | + SO3(т) | + H2O(ж) | NaHSO4(т) | -650 | |
 97 97 | Na2O(т) | + SO2(г) | + S(т) | Na2 S2O3(т) | -402 | |
 98 98 | CuO(т) | + NO2(г) | + O2(г) | Cu(NO3)2(т) | -440 | |
 99 99 | H2O(г) | + CO2(г) | + CuO(т) | Cu2(OH)2CO3(т) | -101 | |
 100 100 | MgO(т) | + NO2(г) | + O2(г) | Mg(NO3)2(т) | -510 |
101-105. По термохимическому уравнению рассчитайте стандартную энтальпию образования реагента А, если известны стандартные энтальпии образования веществ В, С и D (прил. 3).
ЗадачиРеакции
A B C D 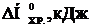
 101KClO4(т) KClO3(т) + KCl(т) + O2(г) +60
101KClO4(т) KClO3(т) + KCl(т) + O2(г) +60
 102Mg(NO3)2(т) MgO(т) + NO2(г) + O2(г) +510
102Mg(NO3)2(т) MgO(т) + NO2(г) + O2(г) +510
 103Na2CO3×10H2O(т) NaOH(т) + CO2(г) + H2O(г) +662
103Na2CO3×10H2O(т) NaOH(т) + CO2(г) + H2O(г) +662
 104KH2PO4(т) KOH(т) +P4O10(т) + H2O(ж) +1020
104KH2PO4(т) KOH(т) +P4O10(т) + H2O(ж) +1020
 105NaHCO3(т) Na2O(т) +CO2(г) + H2O(ж) +338
105NaHCO3(т) Na2O(т) +CO2(г) + H2O(ж) +338
106-110. Рассчитайтестандартное изменение энтропии реакции, предварительно подобрав коэффициенты в уравнении, и установите, будет ли она протекать самопроизвольно в изолированной системе при стандартных условиях. Необходимые данные взять из прил. 3:
Задачи Реакции
106NiO(т)+Al(т)=Ni(т)+Al2O3(т)
107V(т) +CaO(т) =V2O5(т) +Ca(т)
108SO2(г) +H2S(г) =S(т) +H2O(ж)
109N2H4(г) +O2(г) =N2(г) +H2O(г)
110PbS(т) +O2(г) =PbO(т) +SO2(г)
111-115. Рассчитайте при температуре 25оС стандартное изменение свободной энергии Гиббса образования оксида из соответствующих простых веществ, если известны стандартные энтальпии образования ( 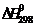 ,кДж/моль) и стандартные энтропии образования(Δ
,кДж/моль) и стандартные энтропии образования(Δ 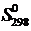 ,Дж/(моль·К)) данного оксида. Может ли данная реакция протекать самопроизвольно?
,Дж/(моль·К)) данного оксида. Может ли данная реакция протекать самопроизвольно?
| Задачи | |||||
| Оксид | Fе2О3 | РbО2 | ZnО | Аl2О3 | ВаО |
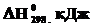 | -824 | -277 | -581 | -1675 | -538 |
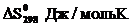 ,ДЖ/мольК ,ДЖ/мольК |
116-120. Поприведенным стандартным значениям изменения энтальпии и энтропии для химической реакции рассчитайте температуру, при которой равновероятны прямое и обратное направления данной реакции. В каком направлении, прямом или обратном, данная реакция будет протекать самопроизвольно при более высоких температурах?
| Задачи | Реакция | 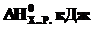 | 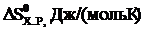 |
| СО2(г)+С(г)=2СО(г) | + 173 | +176 | |
| N2(г)+3Н2(г)=2NH3(г) | -92 | -201 | |
| 2NO(г)+О2(г)=2NO2(г) | -116 | -147 | |
| SО2(г)+Сl2(г)=SС12О2(г) | -67 | -159 | |
| Сl2(г)+5F2(г)=2СlF5(г) | -478 | -616 |
Й уровень
121-125. Вычислите количество теплоты, выделившееся при сгорании углеродсодержащего топлива А массой m, в котором также содержится негорючий компонент с массовой долей Сm. Считать, что горючим компонентом в топливе является углерод С(т):
| Задачи | |||||
| А | Антрацит | Бурый уголь | Каменный уголь | Горючий сланец | Кокс |
| m, кг | |||||
| Cm, % ^т. /о |
126-130. Вычислите, какое количество теплоты выделится при восстановлении оксида А металлом Б, если было получено m, г, восстановленного металла:
| Задачи | |||||
| A | Fе2О3 | ТiO2 | Сr2О3 | СdО | РbО |
| Б | Аl | Са | Mg | Аl | Zn |
| m, г |
131-135. Оцените при стандартных условиях возможность самопроизвольного протекания реакции восстановления металла из его оксида с помощью восстановителей А и В:
| Задачи | |||||
| Оксид | Sb2O5 | Fе3О4 | Вi2О3 | WO3 | ZrO2 |
| А, В | С, Н2 | Са, Н2 | С, Н2 | С, Н2 | Са, Н2 |
136-140. Определите знаки при D Н° и D S° для реакции, протекающей при стандартных условиях в прямом направлении. Как будет изменяться DG° (возрастать или убывать), если температура будет изменяться так, как указано в условии?
| Задачи | Реакция | Температура | |
| 2АВ(т)+В2(г)=2АВ2(т) | возрастает | ||
| АВ5(т) =АВ3(т) +В2(г) | уменьшается | ||
| 2А(ж)+ВС(г)=А2ВС(ж) | уменьшается | ||
| АВ(т)+В(ж)=АВ2(т) | возрастает | ||
| А2В3(г)=2А2В(ж) + В2(г) | возрастает | ||
141-145. Для данной реакции оцените возможность самопроизвольного ее протекания при температуре 298 К.
| Задачи | Реакция |
| H2(г) + Cl2(г) + O2(г) = HСlO4(ж) | |
| Ca(т) + P(т) + O2(г) = Ca3(PO4)2(т) | |
| H2(г) + N2(г) + O2(г) = HNO3(ж) | |
| N2(г) +2 H2(г) = N2H4(г) | |
| Ca(т) + C(т) + O2(г) = CaCO3(т) |
146-150. Рассчитайте температуру, при которой возможно протекание данной реакции в прямом направлении:
| Задачи | Реакция | |
| СН4(г)= С(т) + 2Н2(г) | ||
| Са3(РO4)2(т) = СаО(т) + Р2O5(т) | ||
| Mg(NO3)2(т) = MgO(т) + N2O5(г) | ||
| 2Н2О(г) = 2 H2(г) + O2(г) | ||
| Nа2SО3(т) = Nа2О(т) + SО2(г) | ||
Й уровень
151.Раствор ацетата натрия, содержащий фенолфталеин, при Т =298 К обесцвечивается, а при нагревании становится розовым. На основании этого определите знаки при 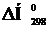 и
и 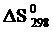 наблюдаемого процесса, напишите его уравнение.
наблюдаемого процесса, напишите его уравнение.
152. Почему при растворении в воде кристаллического хлорида калия энтропия увеличивается, а при растворении газообразного диоксида углерода – уменьшается?
153. Каков знак изменения энергии Гиббса процесса таяния льда при 273 К?
154. Стандартные энтальпии образования (кДж/моль) гидридов азота (III) и фосфора (III) равны соответственно -46,2 и 5,4. Сделайте вывод об относительной устойчивости этих веществ.
155. Предварительно подобрав коэффициенты в уравнении, рассчитайте энтальпию образования реагента Fe3O4 при стандартных условиях, если известны стандартные энтальпии остальных реагентов и продуктов реакции, а также стандартный тепловой эффект реакции ∆Н0х.р= 37 кДж:
СО(г) + Fe3O4(т) → FeO(т) + СO2(г)
156-160. Постандартному изменению энтропии в реакциях (I) и (II) рассчитайте стандартную энтропию образования указанного вещества из простых веществ. Напишите уравнение реакции образования этого вещества из простых веществ:
| Задачи | Реакции | ΔS°, Дж/(мольК) | Вещество |
| (I) 2С(т)+O2(г)=2СО(г) (II) СO(г)+F2(г)= СОF2(г) | + 179 -143 | СОF2 | |
| (I) 2Сr(т)+3F2(г)=2СrF3(т) (II) 2СrF2(т)=2СrF2(т)+F2(г) | -469 -40; | СгF2 | |
