Схема электролиза с нерастворимым анодом
Электролиз водного раствора иодида натрия NaI. Схема электролизера.
(-) Cграфит | Раствор NaI | Cграфит (+)
1. В водном растворе иодида натрия присутствует три вида частиц, способных участвовать в электродных реакциях: молекулы воды Н2О, ионы Na+ и I-. Анодный графит считается инертным (нерастворимым) электродом.
2.3. Возможные анодные реакции:
(+) An: 2I- - 2 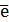 = I2 E0 = + 0,536 B (1)
= I2 E0 = + 0,536 B (1)
2 Н2О - 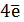 = O2 + 4H+ E0 = + 1,23 B (2)
= O2 + 4H+ E0 = + 1,23 B (2)
Возможные катодные реакции:
(-)KatNa+ + 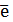 = Na0 E0 = - 2,714 B (1)
= Na0 E0 = - 2,714 B (1)
2Н2О + 2 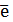 = H2 + 2OH- E0 = - 0,82 B (2)
= H2 + 2OH- E0 = - 0,82 B (2)
4.Сравнив потенциалы реакций, делаем вывод, что на аноде будет протекать реакция №1, так как ее потенциал наименьший, а на катоде - реакция №2,так как ее потенциал наибольший.
5.Сложив эти уравнения, получим суммарную реакцию электролиза
ИМУ 2I- + 2Н2О = I2 + H2 + 2OH-
МУ 2NaI + 2Н2О = I2 + H2 + 2NaOH
В результате электролиза водного раствора иодида натрия с нерастворимым графитовым анодом получают в анодном пространстве электролизера молекулярный иод, а в прикатодном пространстве - раствор гидроксида натрия и выделяющийся газообразный водород.
Следует отметить, что приведенные примеры электролиза рассмотрены в упрощенном варианте. В реальных процессах необходимо учитывать специфическое (адсорбционное) взаимодействие ионов и материала электродов.
Энергия этого взаимодействия может быть настолько велика, что некоторые анионы (An-) могут восстанавливаться на отрицательном катоде, а положительные катионы окисляться на положительном аноде. Использование термодинамических стандартных потенциалов для определения последовательности электродных реакций тоже условно, так как прохождение тока через электролизер сопровождается поляризацией электродов. Результатом поляризации является смещение электродных потенциалов у анода - в положительную сторону, а у катода - в отрицательную. Кроме того, степень смещения этих потенциалов зависит от материала электродов. Это объясняется тем, что нерастворимые электроды являются не только токоподводами, но и выполняют роль катализаторов электродных реакций. Очевидно, что каталитическая активность различных материалов по отношению к конкретной реакции является различной. Степень затрудненности электродных реакций на электродах из различных материалов оценивается параметром, называемым «перенапряжение» (h,В).
Детализация перечисленных явлений не входит в программу настоящего пособия и требует работы с дополнительной литературой.
КОРРОЗИОННЫЕ ПРОЦЕССЫ
Коррозия – это процесс самопроизвольного разрушения металлов при их химическом, электрохимическом или биохимическом взаимодействии с частицами окружающей среды. Коррозионные процессы относятся к разряду окислительно - восстановительных реакций, в которых металл всегда является восстановителем, а частицы окружающей среды выступают в роли окислителя. Процесс коррозии становится возможным, если потенциал металла будет меньше, чем потенциал окислителя. Наиболее распространенным окислителем является атмосферный кислород.
Различают химическую, электрохимическую и биохимическую коррозию. Химическая коррозия металлов –это разрушение металлов под действием агрессивных газов при высоких температурах (газовая коррозия), а также
разрушение металлов в растворах неэлектролитов, т.е. в непроводящих средах.
Биохимическая коррозиявызывается жизнедеятельностью различных микроорганизмов, использующих металл в качестве питательной среды. Биокоррозия обычно сочетается с другими видами коррозии. Для ее развития наиболее благоприятны почвы определенного состава, застойные воды и некоторые органические продукты.
Электрохимическая коррозиявстречается чаще других видов коррозионного разрушения и наиболее опасна для металлов. Она может протекать в газовой атмосфере, когда на поверхности металла возможна конденсация влаги (атмосферная коррозия), в почве (почвенная коррозия), в соленой и пресной воде.
В зависимости от характера разрушений при электрохимической коррозии различают сплошную коррозию, захватывающую всю поверхность металла и местную коррозию, локализующуюся на определенных участках. Очаги местной коррозии могут иметь вид пятен (пятнистая коррозия) или точек (питтинговая коррозия), которые могут захватывать зерна только одного из компонентов сплава (избирательная или селективная коррозия ), проходить через все зерна в виде узких трещин (транскристаллитная коррозия) или сосредоточиться на границах зерен (межкристаллитная коррозия).
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ
Окислителем при электрохимической коррозии металлов может быть растворенный в воде кислород. В этом случае говорят, что коррозия протекает с кислородной деполяризацией:
О2 + 4Н+ + 4е = 2Н2О ( рН=0) Ео= +1,228 В
О2 + 2Н2О + 4е = 4ОН- (рН=7) Ео= +0,81 В
О2 + 2Н2О + 4е = 4ОН- (рН=14) Ео= +0,401 В
Таким образом, в кислой среде подвергаться коррозии с кислородной деполяризацией могут металлы, стандартный электродный потенциал которых отрицательнее +1,23 В, в нейтральной +0,81 и щелочной – отрицательнее + 0,4В.
Активные металлы в кислой среде корродируют с водородной деполяризацией, т.е в качестве окислителя выступают свободные ионы водорода:
2Н+ + 2е = Н2 (рН =0) Ео = 0 В
Наиболее простой моделью коррозионного процесса, идущего по электрохимическому механизму, является модель коррозионного гальванического элемента (микрогальванопар). Возникновение катодных и анодных участков на поверхности металла связано: с химической и геометрической неоднородностью поверхности; механическими напряжениями; неоднородностью коррозионной среды; температурным градиентом поверхности; контактом с другими металлами и многими другими факторами. Рассмотрим некоторые из этих факторов более подробно.
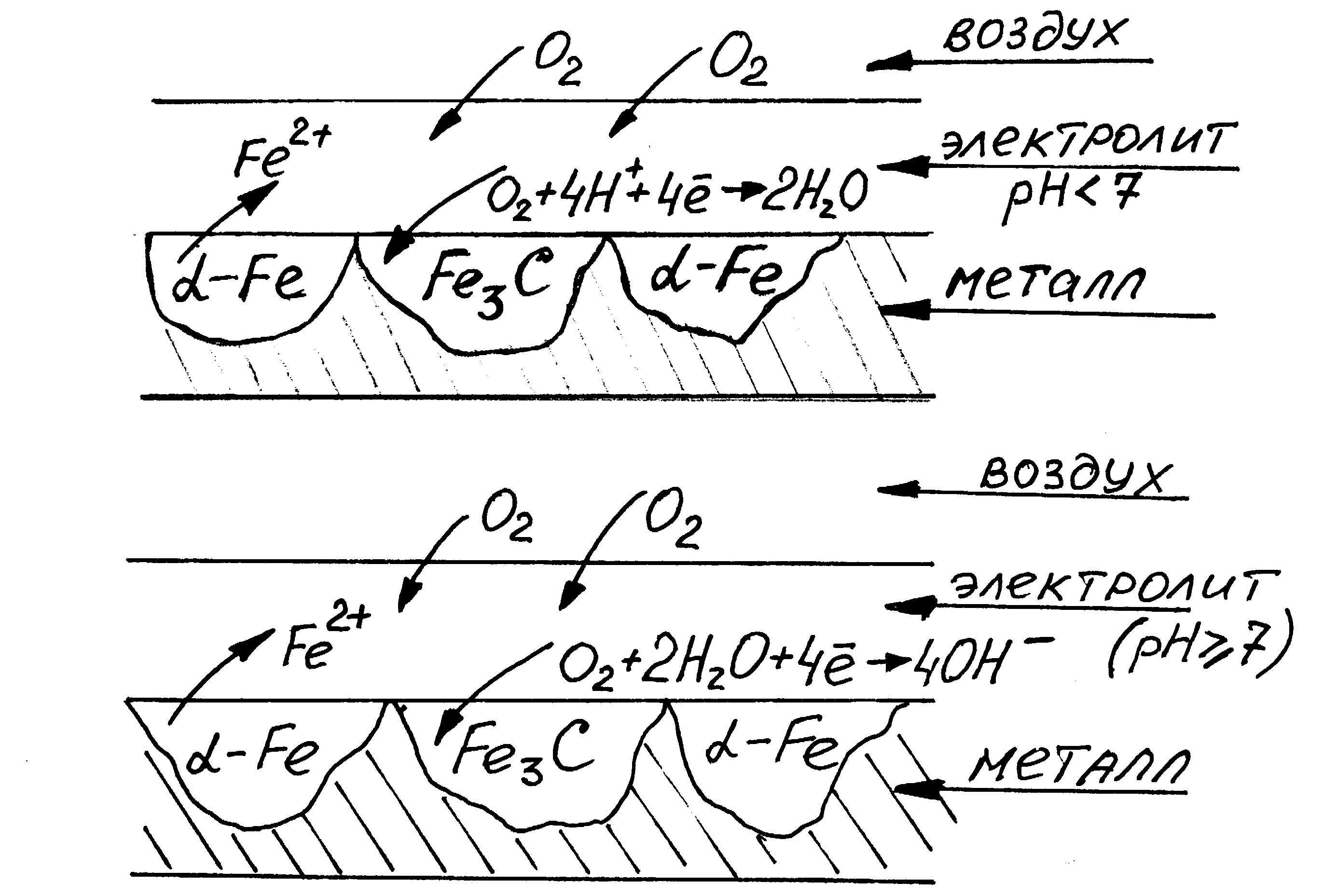
Химическая неоднородность поверхности.Ниже приведены схемы коррозии углеродистой стали для различных сред, в которых пассивными (катодными) участками являются зерна карбида железа (Fe3C).
| Коррозионные процессы: Fe - 2e = Fe2+ 2 О2 + 4Н+ + 4е = 2Н2О1 ___________________________________ 2Fe + O2 +4H+ = 2Fe2+ + 2 H2O |
| Коррозионные процессы: Fe - 2e = Fe2+ 2 О2 + 2Н2O + 4е = 4OН-1 2Fe + O2 +2H2O = 2Fe2+ + 4OH- 2Fe2+ + 4OH- = 2Fe(OH)2 |
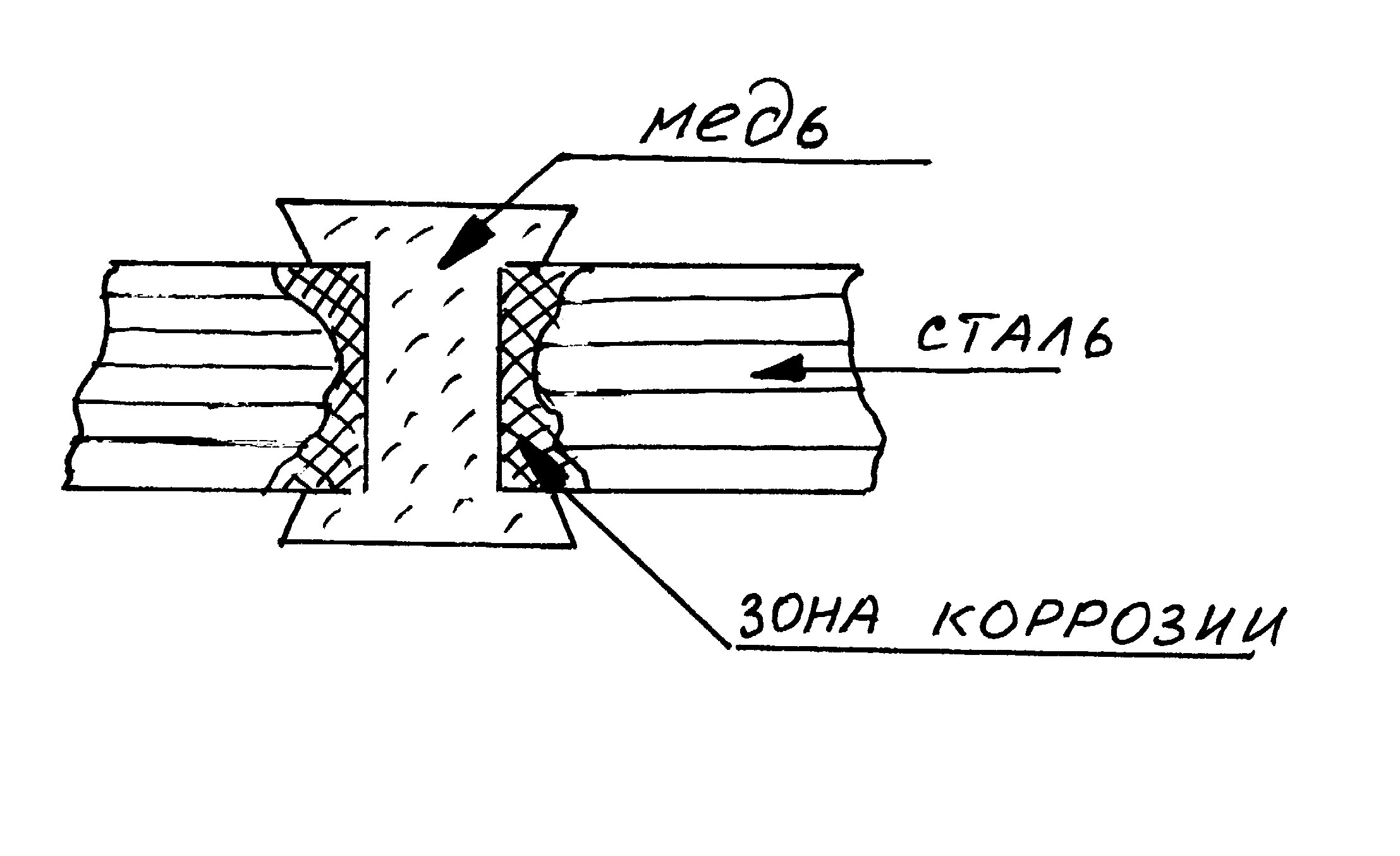
В данном примере рассматривается работа коррозионной микрогальванопары  металл и его соединение. При коррозии эвтектического сплава возможен процесс
металл и его соединение. При коррозии эвтектического сплава возможен процесс
селективного вытравливания зерен одного из компонентов (более активного металла).
| Коррозионные процессы: (кислая среда) Fe - 2e = Fe2+ 2Н+ +2е = Н2 Fe + 2H+ = Fe2+ + H2 |
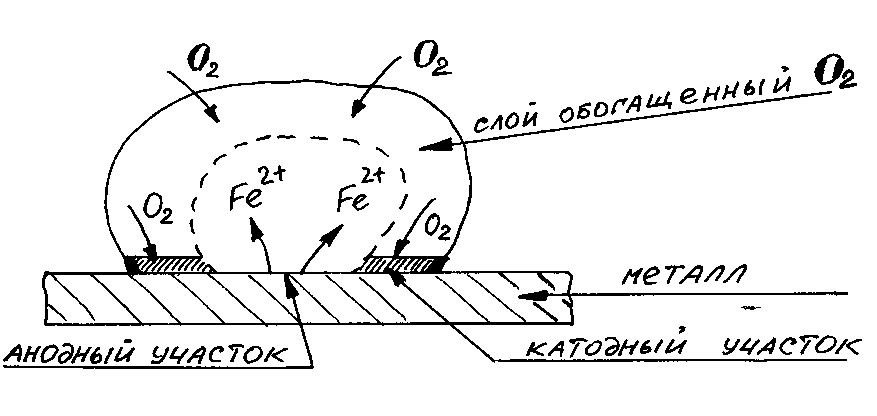
Влияние неоднородности состава коррозионной среды. Неоднородность состава среды может приводить к образованию микрогальванопар даже на поверхности одного и того же металла. Примером может служить коррозия металла под каплей воды. Так как поверхностные слои воды содержат больше растворенного кислорода, чем внутренние, поверхность металла в центре под каплей оказывается более активной (анодный участок). После высыхания капли в центре металлической пластинки появляется довольно глубокое пятно ржавчины. Такие процессы наиболее часто наблюдаются при атмосферной и почвенной коррозии. В общем случае неоднородность состава среды приводит к неравенству электродных потенциалов на различных участках поверхности металла, что и способствует образованию микрогальванопар.
Механические напряжения. Коррозионные микрогальванопары могут
возникать при действии внешних и внутренних механических напряжений (например, остаточные напряжения после сварки). Коррозия при действии внешних
и внутренних напряжений приводит к межкристаллитному растрескиванию, или так называемой «ножевой» коррозии.
