Опишите способы получения средних солей

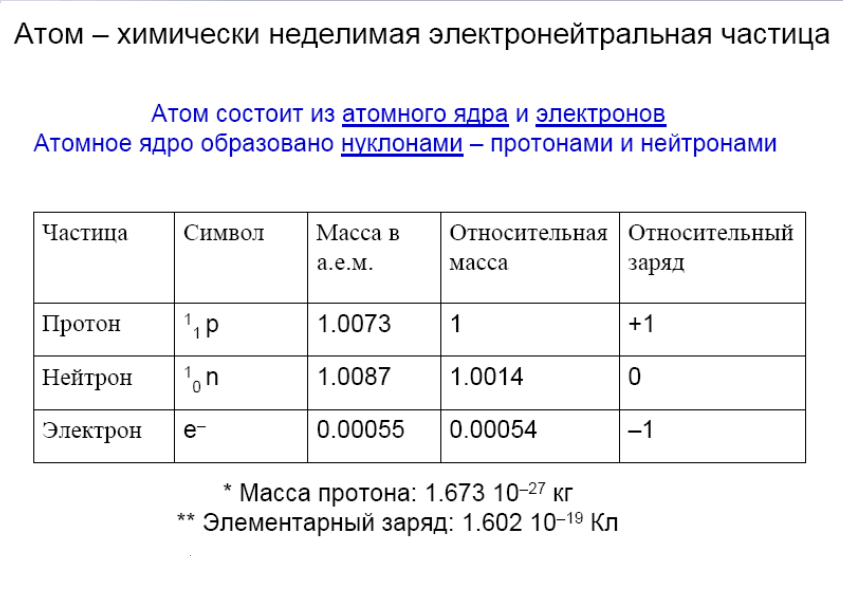
Опишите строение атома, охарактеризуйте частицы, находящиеся в составе атома
Сформулируйте постулаты Бора
Первый постулат Бора. Электроны могут вращаться вокруг ядра по строго определенным стационарным орбитам, при этом они не излучают и не поглощают энергию.
Второй постулат Бора. При переходе с одной орбиты на другую электрон поглощает или испускает квант энергии.
Опишите квантовые числа, тукажите их физический смысл, приведите формулы для расчета



15)СТРУКТУРА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ Менделеева (короткая форма)
Современная периодическая система включает 109 хим элементов
В периодической системе существуют горизонтальные и вертикальные ряды химических элементов:
Период – это горизонтальный ряд химических элементов, расположенные в порядке возрастания заряда атомного ядра. У химических элементов находящихся в одном периоде атомы имеют одинаковое количество энергетических уровней. Всего существует семь периодов. Различают малые и большие периоды химических элементов.Каждый период начинается со щелочного металла и заканчивается инертным газом.
Группа – вертикальные ряды, химические элементы в которых имеют одинаковое количества электронов на внешнем энергетическом уровне. Нахождение элемента в подгруппе определяется сходством конфигурации внешнего энергетического уровня. От порядка заполнения атомныхорбиталей все элементы делятся на s,p,d и f семейства.
16) 1. Номер периода = числу энергетических уровней в атоме
2. Порядковый номер элемента = количеству электронов = заряду ядра атома
3. Длина периода определяется числом электронов, необходимых для завершения соответствующих энергетических подуровней
4. В коротких периодах, начале и конце длинных периодов наблюдается увеличение числа электронов на внешнем уровне
5. В длинных периодах происходит заполнение внутренних электронных оболочек в атомах переходных металлов
6. Электронных конфигурации элементов в группе аналогичны, что приводит к сходству физических и химических свойств
АТОМНЫЙ РАДИУС
· Орбитальный радиус (rорб) – расстояние от ядра до максимума радиальной электронной плотности последнего энергетического уровня ( наибольшие rорб – щелочные и щелочно-земельные металлы, наименьшие rорб – галогены и инертные газы)
· Ковалентный радиус (rk) – половина длины одинарной ковалентной связи между атомами данного элемента ( в том числе для атомов, образующих кратные связи)
· Металлический радиус (rм ) –половина межъядерного расстояния соседних атомов в плотноупакованной кристаллической решетке металла
· Ионный радиус (r+, r-) – считают, что расстояние между ядрами соседних катиона и аниона равно сумме их ионных радиусов
· Ван-дер-ваальсов радиус (rв) – кратчайшее расстояние между атомами, не образующими химической связи
18)Потенциал ионизации атома - минимальная разность потенциалов U, которую должен пройти электрон в ускоряющем электрическом поле, чтобы приобрести кинетическую энергию, достаточную для ионизации атома.
Чаще употребляемое понятие - энергия ионизации E. Это минимальная энергия, которую надо затратить для удаления электрона из атома.
Потенциал ионизации U тесно связан с энергией ионизации соотношением:
E=Ue,
где е-элементарный электрический заряд.
Энергия ионизации атома является внутренним свойством частицы и не зависит от способа ионизации, тогда как потенциал ионизации, можно сказать,- характеристика исторически первого метода ионизации.
Энергия ионизации атома, выраженная в эВ (электроновольтах), численно совпадает с потенциалом ионизации атома, выраженным вВ (вольтах)
Энергии ионизации возрастает в периоде по мере увеличения порядкового номера элемента. Наименьшее ее значение имеют щелочные металлы, находящиеся в начале периода. Наибольшее значение энергии ионизации характерно для инертных газов, находящихся в конце периода.
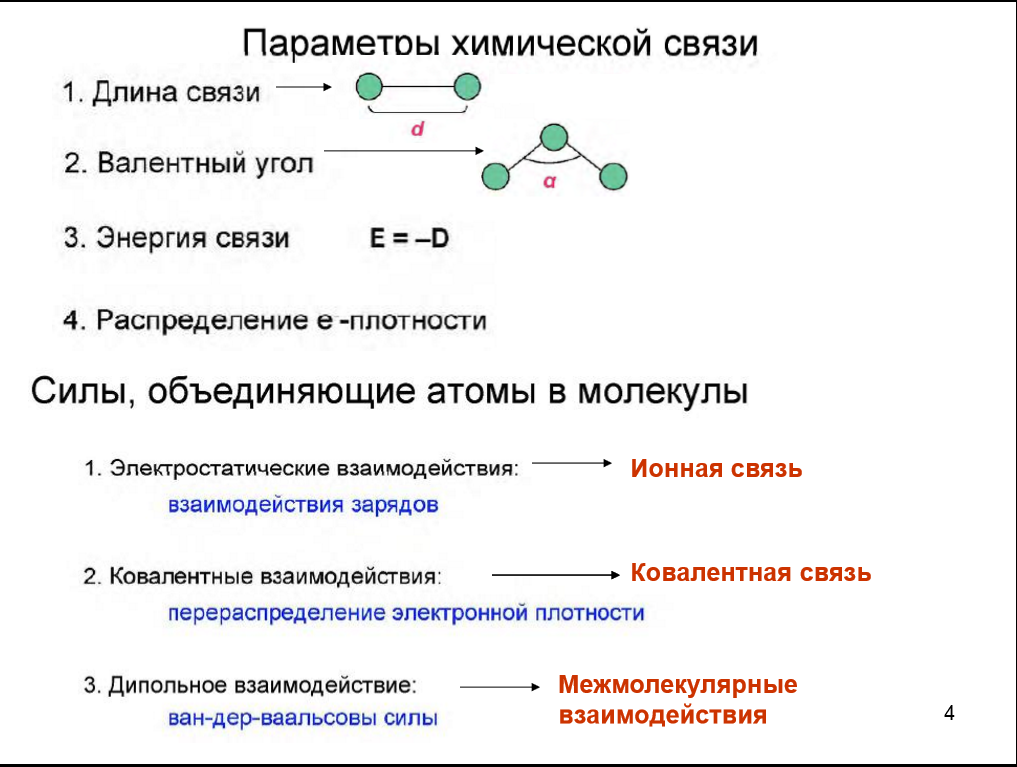
ПАРАМЕТРЫ ХИМИЧЕСКОЙ СВЯЗИ