Относительная элетроотрицательность
СПРАВОЧНЫЕ МАТЕРИАЛЫ
ПО КУРСУ ОБЩЕЙ И НЕОРГАНИЧЕСКОЙ ХИМИИ
Нижний Новгород 1998
Составители: Л.Н. Четырбок, Г.А. Паничева, А.Д. Самсонова
УДК 54(07)
Справочные материалы по курсу общей химии / НГТУ; Сост.: Л.Н. Четырбок, Г.А. Паничева, А.Д. Самсонова. Н.Новгород, 1998. – 35с.
Приведены справочные материалы для практических и лабораторных занятий по курсу общей и неорганической химии.
Научный редактор Ю.М. Тюрин
Редактор И.И. Морозова
Подп. к печ. 5.10.98. Формат 60х84 1/16. Бумага газетная. Печать офсетная. Печ.л. 2,25.
Уч.-изд.л. 2,2. Тираж 2500 экз. Заказ 414.
Нижегородский государственный технический университет.
Типография НГТУ. 603600. Н.Новгород, ул. Минина, 24.
© Нижегородский государственный технический университет, 1998
ЭНЕРГИЯ ИОНИЗАЦИИ И СРОДСТВО К ЭЛЕКТРОНУ НЕКОТОРЫХ АТОМОВ (эВ)
| периоды | Группы элементов | |||||||||||||||||
| IА | IIA | IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |||
| H 13,60 0,75 | He 24,59 -0,22 | |||||||||||||||||
| Li 5,39 0,59 | Be 9,32 -0,19 |
- энергия ионизации (I), Э+I=Э+е - сродство к электрону (F), Э+е=Э±F +F – атом присоединяет е с выигрышем энергии -F – атом не присоединяет электрон (е) | B 8,30 0,30 | C 11,26 1,27 | N 14,53 -0,21 | O 13,62 1,47 | F 17,42 3,45 | Ne 21,56 -0,22 | ||||||||||
| Na 5,14 0,34 | Mg 7,65 -0,22 | Al 5,99 0,5 | Si 8,15 1,37 | P 10,49 0,8 | S 10,36 2,08 | Cl 12,97 3,61 | Ar 15,76 -0,37 | |||||||||||
| K 4,34 0,47 | Ca 6,11 -1,93 | Sc 6,56 -0,73 | Ti 6,82 0,39 | V 6,74 0,63 | Cr 6,76 0,98 | Mn 7,44 -0,97 | Fe 7,89 0,58 | Co 7,87 0,94 | Ni 7,63 1,28 | Cu 7,73 1,8 | Zn 9,39 0,09 | Ga 6,00 0,39 | Ge 7,90 1,74 | As 9,82 1,07 | Se 9,75 2,02 | Br 11,84 3,37 | Kr 14,0 -0,42 | |
| Rb 4,18 0,42 | Sr 5,69 -1,51 | Y 6,22 -0,4 | Zr 6,84 0,45 | Nb 6,88 1,13 | Mo 7,10 1,18 | Tc 7,28 0,99 | Ru 7,37 1,51 | Rh 7,46 1,68 | Pd 8,34 1,02 | Ag 7,58 1,30 | Cd 8,99 -0,27 | In 5,79 0,2 | Sn 7,34 1,03 | Sb 8,64 0,94 | Te 9,01 1,96 | I 10,45 3,08 | Xe 12,13 -0,45 | |
| Cs 3,89 0,39 | Ba 5,21 -0,48 | La 5,58 0,55 | Hf 7,5 -0,63 | Ta 7,89 0,15 | W 7,98 1,23 | Re 7,88 0,38 | Os 8,50 1,44 | Ir 9,1 1,97 | Pt 8,9 2,13 | Au 9,23 2,31 | Hg 10,44 -0,19 | Tl 6,11 0,32 | Pb 7,42 1,03 | Bi 12,25 0,95 | Po 8,43 1,32 | At 9,20 2,80 | Rn 10,75 - |
ОТНОСИТЕЛЬНАЯ ЭЛЕТРООТРИЦАТЕЛЬНОСТЬ
| Период | IA | IIA | IIIA | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | ||
| H 2,1 | |||||||||||||||||
| Li 1,0 | Be 1,5 | B 2,0 | C 2,5 | N 3,0 | O 3,5 | F 4,0 | |||||||||||
| Na 0,9 | Mg 1,2 | Al 1,5 | Si 1,8 | P 2,1 | S 2,5 | Cl 3,0 | |||||||||||
| K 0,8 | Ca 1,0 | Sc 1,3 | Ti 1,6 | V 1,6 | Cr 1,6 | Mn 1,5 | Fe 1,8 | Co 1,8 | Ni 1,8 | Cu 1,9 | Zn 1,6 | Ga 1,6 | Ge 1,7 | As 2,0 | Se 2,4 | Br 2,8 | |
| Rb 0,8 | Sr 1,0 | Y 1,3 | Zr 1,6 | Nb 1,6 | Mo 1,8 | Tc 1,9 | Ru 2,2 | Rh 2,2 | Pd 2,2 | Ag 1,9 | Cd 1,7 | In 1,7 | Sn 1,7 | Sb 1,8 | Te 2,1 | I 2,6 | |
| Cs 0,7 | Ba 0,9 | La 1,1 | Hf 1,3 | Ta 1,5 | W 1,7 | Re 1,9 | Os 2,2 | Ir 2,2 | Pt 2,2 | Au 2,4 | Hg 1,9 | Tl 1,8 | Pb 1,7 | Bi 1,8 | Po 2,0 | At 2,2 | |
| Fr 0,7 | Ra 0,9 | Ac 1,1 |
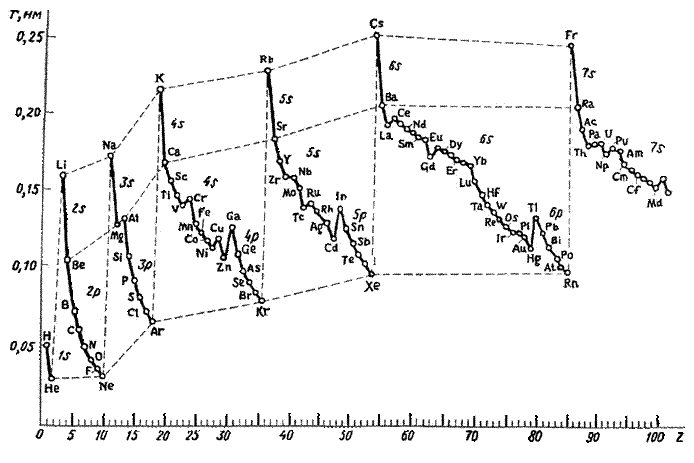
4. Зависимость орбитальных радиусов атомов от атомного номера элемента
5. ПЕРИОДИЧЕСКАЯ ЗАВИСИМОСТЬ СРОДСТВА К ЭЛЕКТРОНУ (F1) И ПЕРВОЙ ЭНЕРГИИ ИОНИЗАЦИИ (I1) АТОМОВ ОТ АТОМНОГО НОМЕРА ЭЛЕМЕНТА
Сродство к электрону взято с обратным знаком, т.е. приведены первые энергии ионизации отрицательно заряженных ионов Э-

ПАРАМЕТРЫ ХИМИЧЕСКОЙ СВЯЗИ ДВУХАТОМНЫХ МОЛЕКУЛ
| Молекула | Энергия связи, кДж/моль | Длина связи, нм | Энергия ионизации, эВ | Сродство к электрону, эВ | |
| I | H2 | 435,8 | 0,074 | 15,46 | |
| N2 | 946,9 | 0,110 | 15,63 | ||
| CO | 1076,8 | 0,113 | 14,02 | ||
| II | He2 | 0,042 | 0,292 | 22,45 | |
| O2 | 498,6 | 0,121 | 12,11 | 0,497 | |
| F2 | 159,2 | 0,142 | 16,50 | 3,08 | |
| Cl2 | 243,0 | 0,199 | 11,51 | 2,40 | |
| Br2 | 192,7 | 0,228 | 10,64 | 2.59 | |
| J2 | 150,8 | 0,267 | 9,29 | 2.49 | |
| NO | 632,7 | 0,115 | 9,29 | ||
| III | HCl | 431,6 | 0,127 | 12,76 | |
| HBr | 368,7 | 0,141 | 11,68 | ||
| HJ | 297,5 | 0,161 | 10,42 |
Молекулы группы I при ионизации теряют связывающие электроны, молекулы группы II – теряют разрыхляющие электроны, а молекулы группы III теряют несвязывающие электроны.
ТИПЫ МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ
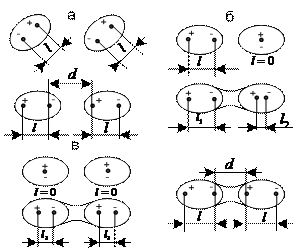
а – ориентационное; б – индукционное; в – дисперсионное; 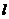 - длина диполя;
- длина диполя; 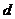 - межмолекулярное расстояние
- межмолекулярное расстояние
ВКЛАД ОТДЕЛЬНЫХ СОСТАВЛЯЮЩИХ В ПОЛНУЮ ЭНЕРГИЮ
МЕЖМОЛЕКУЛЯРНОГО ВЗАИМОДЕЙСТВИЯ
| Вещество | Электрический момент диполя молекулы *1029, Кл*м | Поляри-зуемость | Эффект, кДж/моль | Суммарная энергия, кДж/моль | Температура кипения, К | ||
| ориента-ционный | индук-ционный | диспер-сионный | |||||
| H2 | 0,20 | 0,17 | 0,17 | 20,21 | |||
| Ar | 1,63 | 8,48 | 8,48 | ||||
| Xe | 4,00 | 18,4 | 18,4 | ||||
| CO | 0,39 | 1,99 | 8,79 | 8,79 | |||
| HCl | 3,4 | 2,63 | 3,34 | 1,003 | 16,72 | 21,05 | |
| HBr | 2,57 | 3,58 | 1,09 | 0,71 | 28,42 | 30,22 | |
| HI | 1,25 | 5,4 | 0,58 | 0,295 | 60,47 | 61,36 | |
| NH3 | 4,95 | 2,21 | 13,28 | 1,55 | 14,72 | 29,55 | 239,6 |
| H2O | 6,07 | 1,48 | 36,32 | 1,92 | 8,98 | 47,22 |
СПРАВОЧНЫЕ МАТЕРИАЛЫ
ПО КУРСУ ОБЩЕЙ И НЕОРГАНИЧЕСКОЙ ХИМИИ
Нижний Новгород 1998
Составители: Л.Н. Четырбок, Г.А. Паничева, А.Д. Самсонова
УДК 54(07)
Справочные материалы по курсу общей химии / НГТУ; Сост.: Л.Н. Четырбок, Г.А. Паничева, А.Д. Самсонова. Н.Новгород, 1998. – 35с.
Приведены справочные материалы для практических и лабораторных занятий по курсу общей и неорганической химии.
Научный редактор Ю.М. Тюрин
Редактор И.И. Морозова
Подп. к печ. 5.10.98. Формат 60х84 1/16. Бумага газетная. Печать офсетная. Печ.л. 2,25.
Уч.-изд.л. 2,2. Тираж 2500 экз. Заказ 414.
Нижегородский государственный технический университет.
Типография НГТУ. 603600. Н.Новгород, ул. Минина, 24.
© Нижегородский государственный технический университет, 1998
ЭНЕРГИЯ ИОНИЗАЦИИ И СРОДСТВО К ЭЛЕКТРОНУ НЕКОТОРЫХ АТОМОВ (эВ)
| периоды | Группы элементов | |||||||||||||||||
| IА | IIA | IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | |||
| H 13,60 0,75 | He 24,59 -0,22 | |||||||||||||||||
| Li 5,39 0,59 | Be 9,32 -0,19 |
- энергия ионизации (I), Э+I=Э+е - сродство к электрону (F), Э+е=Э±F +F – атом присоединяет е с выигрышем энергии -F – атом не присоединяет электрон (е) | B 8,30 0,30 | C 11,26 1,27 | N 14,53 -0,21 | O 13,62 1,47 | F 17,42 3,45 | Ne 21,56 -0,22 | ||||||||||
| Na 5,14 0,34 | Mg 7,65 -0,22 | Al 5,99 0,5 | Si 8,15 1,37 | P 10,49 0,8 | S 10,36 2,08 | Cl 12,97 3,61 | Ar 15,76 -0,37 | |||||||||||
| K 4,34 0,47 | Ca 6,11 -1,93 | Sc 6,56 -0,73 | Ti 6,82 0,39 | V 6,74 0,63 | Cr 6,76 0,98 | Mn 7,44 -0,97 | Fe 7,89 0,58 | Co 7,87 0,94 | Ni 7,63 1,28 | Cu 7,73 1,8 | Zn 9,39 0,09 | Ga 6,00 0,39 | Ge 7,90 1,74 | As 9,82 1,07 | Se 9,75 2,02 | Br 11,84 3,37 | Kr 14,0 -0,42 | |
| Rb 4,18 0,42 | Sr 5,69 -1,51 | Y 6,22 -0,4 | Zr 6,84 0,45 | Nb 6,88 1,13 | Mo 7,10 1,18 | Tc 7,28 0,99 | Ru 7,37 1,51 | Rh 7,46 1,68 | Pd 8,34 1,02 | Ag 7,58 1,30 | Cd 8,99 -0,27 | In 5,79 0,2 | Sn 7,34 1,03 | Sb 8,64 0,94 | Te 9,01 1,96 | I 10,45 3,08 | Xe 12,13 -0,45 | |
| Cs 3,89 0,39 | Ba 5,21 -0,48 | La 5,58 0,55 | Hf 7,5 -0,63 | Ta 7,89 0,15 | W 7,98 1,23 | Re 7,88 0,38 | Os 8,50 1,44 | Ir 9,1 1,97 | Pt 8,9 2,13 | Au 9,23 2,31 | Hg 10,44 -0,19 | Tl 6,11 0,32 | Pb 7,42 1,03 | Bi 12,25 0,95 | Po 8,43 1,32 | At 9,20 2,80 | Rn 10,75 - |
ОТНОСИТЕЛЬНАЯ ЭЛЕТРООТРИЦАТЕЛЬНОСТЬ
| Период | IA | IIA | IIIA | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | ||
| H 2,1 | |||||||||||||||||
| Li 1,0 | Be 1,5 | B 2,0 | C 2,5 | N 3,0 | O 3,5 | F 4,0 | |||||||||||
| Na 0,9 | Mg 1,2 | Al 1,5 | Si 1,8 | P 2,1 | S 2,5 | Cl 3,0 | |||||||||||
| K 0,8 | Ca 1,0 | Sc 1,3 | Ti 1,6 | V 1,6 | Cr 1,6 | Mn 1,5 | Fe 1,8 | Co 1,8 | Ni 1,8 | Cu 1,9 | Zn 1,6 | Ga 1,6 | Ge 1,7 | As 2,0 | Se 2,4 | Br 2,8 | |
| Rb 0,8 | Sr 1,0 | Y 1,3 | Zr 1,6 | Nb 1,6 | Mo 1,8 | Tc 1,9 | Ru 2,2 | Rh 2,2 | Pd 2,2 | Ag 1,9 | Cd 1,7 | In 1,7 | Sn 1,7 | Sb 1,8 | Te 2,1 | I 2,6 | |
| Cs 0,7 | Ba 0,9 | La 1,1 | Hf 1,3 | Ta 1,5 | W 1,7 | Re 1,9 | Os 2,2 | Ir 2,2 | Pt 2,2 | Au 2,4 | Hg 1,9 | Tl 1,8 | Pb 1,7 | Bi 1,8 | Po 2,0 | At 2,2 | |
| Fr 0,7 | Ra 0,9 | Ac 1,1 |
4. Зависимость орбитальных радиусов атомов от атомного номера элемента

5. ПЕРИОДИЧЕСКАЯ ЗАВИСИМОСТЬ СРОДСТВА К ЭЛЕКТРОНУ (F1) И ПЕРВОЙ ЭНЕРГИИ ИОНИЗАЦИИ (I1) АТОМОВ ОТ АТОМНОГО НОМЕРА ЭЛЕМЕНТА
Сродство к электрону взято с обратным знаком, т.е. приведены первые энергии ионизации отрицательно заряженных ионов Э-

