Цель урока: изучение аномальных свойств воды.
Задачи урока:
Обучающая:
- формировать у обучающихся понятий аномалий воды: температуры кипения и замерзания, поверхностное натяжение; удельная теплоемкость.
Развивающая:
- создать условия для развития у обучающегося ключевых компетенций: информационной, коммуникативной;
- продолжить развитие экспериментальных навыков;
- формировать умение анализировать полученную информацию.
Воспитывающая:
- воспитание положительной мотивации учения, правильной самооценки и чувства ответственности; умение работать в коллективе.
Технология критического мышления.
Тип урока: применение знаний по теме.
Форма занятия:
- Групповая и индивидуальная работы, лабораторный опыт и демонстрация.
Оборудование:
- Ноутбук, мультимедийный проектор, экран
- Химические реактивы и оборудование: стакан с водой; стакан с соленой водой; соль; яйцо (сырое); ложка, игла.
Схема урока:
I. Стадия «Вызов».
Учитель предлагает отгадать, что содержится в черном ящике.
Лао-Цзы утверждал, что это «самое мягкое и слабое существо в мире, но в преодолении твердого и крепкого она непобедима и нет ей на свете равного в этом». Отгадайте, ребята, что в черном ящике?
( В черном ящике – стакан с водой)
Итак, ребята, я думаю, вы догадались, что сегодня речь пойдет об обыкновенной воде. Учитель достает из «черного ящика» стакан с водой.
Эпиграф урока (записан на слайде):
Вода благоволила литься! Она блистала столь чиста,
что - ни напиться, ни умыться, и это было неспроста.
Ей не хватало ивы, тала и горечи цветущих лоз.
Ей водорослей не хватало и рыбы, жирной от стрекоз.
Ей не хватало быть волнистой, ей не хватало течь везде.
Ей жизни не хватало - чистой, дистиллированной воде!
Леонид МАРТЫНОВ (1946 г.)
Итак, сегодня мы с вами говорим о вечном веществе – воде. Давайте вспомним, что мы знаем об этом веществе. Учитель просит учащихся расчертить таблицу ЗХУ и заполнить 1 колонку «что знаю» (учащиеся перечисляют физические свойства воды: агрегатное состояние, вкус, цвет, запах, температуры кипения и замерзания, некоторые обучающиеся делятся информацией, полученной на уроке биологии о содержании воды в организме человека и различных растениях и др.).
Занятие по теме «Вода благоволила литься…»
| что знаю | что хочу узнать | что узнал (а) |
2 колонку учащиеся заполняют по окончании блеф-игры «Верите ли вы…» Последнюю графу «что узнал» - заполняют после просмотра документального фильма «Тайна воды».
Блеф-игра «Верите ли вы…»
- Верите ли вы, что в соленой воде не утонет яйцо? (Плотность соленой воды больше, чем пресной, следовательно, выше выталкивающая сила.) ЛО. Одному из учеников предлагается опустить по 1 сырому яйцу в 2 стакана с соленой и пресной водой. Учащиеся на практике могут убедиться в разной плотности соленой и пресной воды.
- Верите ли вы, что на морозе белье высыхает быстрее. (Нет скорость высыхания зависит от температуры. Лед испаряется, поэтому белье высыхает)
- Верите ли вы, что сухой воздух легче (На самом деле легче влажный воздух, т.к. масса воды меньше массы воздуха).
- Верите ли вы, что ржаной хлеб черствеет медленнее, чем белый (В ржаном хлебе больше клейковины и микроэлементов, они активнее связывают и удерживают воду).
- Верите ли вы, что стальная игла, аккуратно опущенная на поверхность чистой воды, не тонет? (Ее удерживают силы поверхностного натяжения). Демонстрация поверхностного натяжения воды (Приложение 1).
- Верите ли вы, что существует 8 наименований состояния воды в метеорологии? (Пар, лед, снег, туман, иней, град, облака, тучи).
- Верите ли вы, что при снегопаде наблюдается потепление? (У льда высокая теплота плавления).
- Верите ли вы, что слово «гигиена» произошло от имени древнегреческой богини, которую принято обозначать в виде молодой женщины с чашей воды в руке? (Да, это Богиня здоровья Гигея).
- Как понятие «малая родина» связано с водой? (Структура воды в человеческом организме идентична структуре воды той местности, в которой он родился). /2/.
- Верно ли, что вода обладает текучестью? (Под действием внешних сил жидкость не сохраняет форму и поэтому принимает форму сосуда, в котором находится. В отличии от пластичных твердых тел, жидкость не имеет предела текучести: достаточно приложить сколь угодно малую внешнюю силу, чтобы жидкость потекла).
- Верите ли вы, что вода бывает сухой? (Нет, не бывает. То, что называют «сухой водой» на самом деле водой не является. «Сухая вода» - Noves 1230. Формула вещества CF3CF2C(O)CF(CF3)2
Демонстрация видеофрагмента передачи «Галилео» о свойствах «сухой воды» /4/.
Стадия «Осмысление»
Учащимся предлагается чтение информационного текста об аномалиях воды и составление маркированной таблицы («Инсерт»). Вся работа (индивидуальная и групповая) рассчитана на 20 минут.
Работа выполняется индивидуально. Для чего каждый ученик получает текст «Аномалии воды» (Приложение 2) /5/. Количество граф в таблице соответствует значкам маркировки: «V» - уже знал; «+» - новое; «-» - думал иначе; «?» - не понял, есть вопросы.
| V | + | - | ? |
Сначала учащиеся самостоятельно заполняют маркировочную таблицу. Затем объединившись в группы, совместно обсуждают заполнение этой таблицы. Спустя означенное время группа представляет свой вариант работы над текстом. При заполнении таблицы учащиеся неоднократно обращаются к тексту, т.е. чтение в этом случае будет внимательным, осмысленным.
Стадия «Рефлексия»
На стадии «Рефлексия» я применяю рисунок, отображающий аномалии воды (Приложение 3) /6/. Задача обучающихся – по рисунку составить синквейн.
Синквейн – это стихотворение, состоящее из пяти строк, в которых человек высказывает свое отношение к проблеме.
Порядок написания синквейна:
Первая строка – одно ключевое слово, определяющее содержание синквейна.
Вторая строка – два прилагательных, характеризующих данное предложение.
Третья строка – три глагола, показывающие действие понятия.
Четвертая строка – отношение автора к проблеме одним предложением.
Пятая строка – одно слово, обычно существительное, через которое человек выражает свои чувства, ассоциации, связанные с понятием /1/.
Возможный вариант синквейна по теме «Вода благоволила литься…»:
Вода,
Обыкновенная, загадочная,
Лечит, таит секреты, замерзая расширяется,
В тебе зародилась жизнь,
Аномалия.
Закончить занятие я предлагаю «научной шуткой», которая доказывает важность знаний химии для обыкновенного человека.
Недавно исследователи открыли факт загрязнения наших водопроводных систем опасным химикатом. Этот химикат бесцветный, безвкусный и не имеет запаха. Он убивает бесчисленное множество людей каждый год. Правительство не предприняло никаких попыток регулирования этого опасного заражения. Данный химикат называется «дигидрогенамонооксид» (Dihydrogenmonoxide).
У этого вещества негативные для человека свойства:
· Длительный контакт с химикатом в его твёрдой форме приводит к серьёзным повреждениям кожи человека;
· Контакт с газообразной формой химиката приводит к сильным ожогам;
· Вдыхание даже небольшого количества химиката грозит смертельным исходом;
· Ни один известный очиститель не способен полностью очистить воду от этого химиката!
Несмотря на эти опасности, химикат активно и безнаказанно используется в индустрии. Многие корпорации ежедневно получают тонны химиката через специально проложенные подземные трубопроводы. Люди, работающие с химикатом, как правило, не получают спецодежды и инструктажа. Отработанный химикат тоннами выливается в реки и моря. Некоторые люди призывают население проявить сознательность и протестовать против дальнейшего использования этого опасного химиката /3/.
Все что я сейчас о дигидрогенемонооксиде сказала, не более чем шутка. Предназначена она для иллюстрации того, каким образом отсутствие научных знаний и предвзятый анализ могут привести к панике. Надеюсь, что вы не будете бояться этого вещества, тем более, как всем известно, «что без воды и не туды, и не сюды».
Домашнее задание: просмотр документального фильма «Великая тайна воды» и заполнение 3 колонки таблицы ЗХУ – «что узнал». Для желающих – составление презентации по теме: «Вода – простое, но удивительное вещество».
Литература:
1. Маркина И.В. Современный урок химии. Технологии, приемы, разработки учебных занятий/ Ярославль: Академия развития, 2008. – 288 с.; стр. 40.
2. Вода в нашей жизни. Дополнительные материалы к учебникам О.С. Габриеляна «Химия. 8 класс» и «Химия. 9 класс»: учебно-метод. пособие / О.С. Габриелян, Т.Н. Попкова, Г.А. Сивкова, С.А. Сладков. – М. : Дрофа, 2011. – 224 с. : с. 84.
3. http://ru.wikipedia.org/wiki/%D0%94%D0%B8%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%B3%D0%B5%D0%BD%D0%B0_%D0%BC%D0%BE%D0%BD%D0%BE%D0%BE%D0%BA%D1%81%D0%B8%D0%B4. Загадка в начале урока.
4. Телевизионная передача «Галилео» о «сухой воде»: http://www.youtube.com/watch?feature=endscreen&v=unfbSxDLYi4&NR=1 и http://www.youtube.com/watch?v=bt2X4lRxPy0&feature=related
5. Аномалии воды. http://kfs-centr.com/production/55-kfs-20.html
6. Картинка(для рефлексии) аномалия воды http://схемо.рф/shemy/himija/kovalevskaja-n-b-himija-v-tablicah-i-shemah-2009-g/6123.html#down
Дополнительные источники информации (для любознательных учащихся):
1. http://www.youtube.com/watch?v=bt2X4lRxPy0&feature=related – вода и низкая частота звука.
2. Виды воды. http://info-voda.ru/?p=111
3. Сколько нужно воды человеку http://ewater.ru/o-vode-i-eyo-znachanii/
4. О феномене "памяти" воды к.х.н. О.В. Мосин http://kfs-gav2raza.ru/pamyat.htm
5. Пацукова Л.В., Семенькова Н.И. Слушается дело об аномалиях воды. // «Химия в школе» №8, 2002 с.82.
6. Золотова Н.А. Известная и неизвестная вода. // «Химия в школе» №8, 2002 с.85.
ПРИЛОЖЕНИЯ.
Приложение 1.
«Поверхностное натяжение воды»
Опыт 1.Осторожно положите на поверхность воды небольшую швейную иголку. Если у вас один конец иглы был под наклоном, она окажется на дне. Выньте ее из воды, протрите сухой тряпкой и повторите опыт.
Опыт 2. Проделайте аналогичные действия, используя воду, в которой предварительно растворили небольшую порцию стирального порошка.
Опыт 3.На поверхность стекла нанесите по одной капле водопроводной и мыльной воды, рассмотрите, различаются ли они по форме.
Учащимся предлагается объяснить наблюдаемые факты.
ПРИЛОЖЕНИЯ.
Приложение 2.
АНОМАЛЬНЫЕ СВОЙСТВА ВОДЫ
Аномальные свойства воды были открыты учеными в результате длительных и трудоемких исследований. Эти свойства свидетельствуют о том, что молекулы Н2О довольно прочно связаны между собой и образуют характерную молекулярную конструкцию, которая сопротивляется любым разрушающим воздействиям, например, тепловым, механическим, электрическим. По этой причине, например, необходимо затратить много тепла, чтобы превратить воду в пар.
В настоящее время известно большое число гипотез и моделей структуры воды. Согласно одной из них - вода представляет собой иерархию правильных объемных структур из 57 ее молекул (квантов), которые взаимодействуют друг с другом за счет свободных водородных связей, формой напоминающую тетраэдр.
Простые тетраэдры могут объединяться между собой вершинами, ребрами или гранями, образуя различные кластеры со сложной структурой, например, в виде додекаэдра.
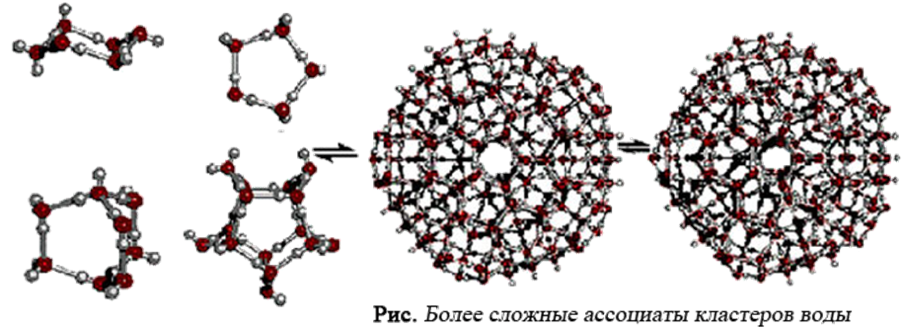 Кластерная модель воды объясняет её многие аномальные свойства.
Кластерная модель воды объясняет её многие аномальные свойства.
Первое аномальное свойство воды – аномалия точек кипения и замерзания. Если бы вода - гидрид кислорода – Н2О была бы нормальным мономолекулярным соединением, таким, например, как ее аналоги по шестой группе Периодической системы элементов Д.И. Менделеева - гидрид серы Н2S, гидрид селена Н2Se, гидрид теллура Н2Те, то в жидком состоянии вода существовала бы в диапазоне от минус 90°C до минус 70°C. При таких свойствах воды жизни на Земле не существовало бы.
Второе аномальное свойство воды - способность при замерзании увеличивать, а не уменьшать свой объем, т.е. уменьшать плотность. На это особое свойство воды впервые обратил внимание еще Г. Галилей. При переходе любой жидкости (кроме галлия и висмута) в твердое состояние молекулы располагаются теснее, а само вещество, уменьшаясь в объеме, становится плотнее. Вода и здесь представляет собой исключение. При охлаждении вода сначала ведет себя, как и другие жидкости: постепенно уплотняясь, она уменьшает свой объем. Такое явление можно наблюдать до +4°С (точнее до +3,98°С).Именно при температуре +3,98° С вода имеет наибольшую плотность и наименьший объем. Дальнейшее охлаждение воды постепенно приводит уже не к уменьшению, а к увеличению объема. Плавность этого процесса вдруг прерывается и при 0° С происходит резкий скачок увеличения объема почти на 10%! В это мгновение вода превращается в лед. Именно эта особенность воды предохраняет от сплошного промерзания в зимний период все водоемы земли - реки, озера, моря и тем самым спасает жизнь.
В отличие от пресной воды морская вода при охлаждении ведет себя иначе. Замерзает она не при 0°С, а при минус 1,8-2,1°С - в зависимости от концентрации растворенных в ней солей. Имеет максимальную плотность не при + 4°С, а при -3,5°С. Таким образом она превращается в лед, не достигая наибольшей плотности. Процесс обмена между верхними и нижними слоями идет непрерывно, создавая благоприятные условия для развития животных и растительных организмов.
Аномалия теплоёмкости заключается в следующем: при нагревании любого вещества теплоемкость неизменно повышается. Вода - исключение: с повышением температуры изменение теплоемкости воды аномально; от 0 до 37°С она понижается и только от 37 до 100°С теплоемкость все время растет.
В пределах температур, близких к 37°С, теплоемкость воды минимальна. Именно эти температуры - область температур человеческого тела. Физика воды в области температур 35-41°С (пределы возможных, нормально протекающих физиологических процессов в организме человека) констатирует вероятность достижения уникального состояния воды, когда массы квазикристаллической и объемной воды равны друг другу и способность одной структуры переходить в другую - максимальная. Это замечательное свойство воды предопределяет равную вероятность течения обратимых и необратимых биохимических реакций в организме человека и обеспечивает "легкое управление" ими.
Аномалии диэлектрической постоянной воды. Это связано с тем, что ее диэлектрическая проницаемость очень велика и составляет 81, в то время как для других жидкостей она не превышает 10. В соответствии с законом Кулона сила взаимодействия двух заряженных частиц в воде будет в 81 раз меньше, чем, например, в воздухе, где эта характеристика равна единице. В этом случае прочность внутримолекулярных связей уменьшается в 81 раз и под действием теплового движения молекулы диссоциируют с образованием ионов. Необходимо отметить, что из-за исключительной способности растворять другие вещества вода никогда не бывает идеально чистой.
Аномалия пятая - поверхностное натяжение. Из всех известных жидкостей только ртуть имеет более высокое поверхностное натяжение. Это свойство проявляется в том, что вода всегда стремится сократить свою поверхность.
Нескомпенсированные межмолекулярные силы наружного (поверхностного) слоя воды, создают внешнюю упругую пленку. Благодаря пленке многие предметы, будучи тяжелее воды, не погружаются в воду. Если, например, стальную иголку осторожно положить на поверхность воды, то иголка не тонет. А ведь удельный вес стали почти в восемь раз больше удельного веса воды. Всем известна форма капли воды. Высокое поверхностное натяжение позволяет воде иметь шарообразную форму при свободном падении.
Поверхностное натяжение и смачивание являются основой особого свойств воды и водных растворов, названного капиллярностью. Капиллярность имеет огромное значение для жизни растительного, животного мира, формирования структур природных минералов и плодородия земли. В каналах, которые во много раз уже человеческого волоса, вода приобретает удивительные свойства. Она становится более вязкой, уплотняется в 1,5 раза, а замерзает при минус 80-70°С.
Приложение 3.

Методическая разработка
Занятие 11.«Золотистого мёдаструя из бутылки текла…»
О. Мандельштам
