Определение содержания белковых веществ
Белки – высокомолекулярные азотсодержащие органические соединения. В природе существует примерно от 1010 до 1012 различных белков, содержание которых в биологических объектах зависит от ряда факторов: климатических условий, урожайности, биологических особенностей.
По своему строению белки являются высокомолекулярными соединениями, состоящими из аминокислот. Соединенные амидной (пептидной) связью аминокислоты образуют полипептиды простого (протеина) и сложного (протеида) строения. В состав протеидов дополнительно входят небелковые вещества (липиды, углеводыит. д.).
Всреднем белковые молекулы содержат: 50–54 % углерода; 15–18 % азота; 20–23 % кислорода; 6–8 % водорода и 0,3–2,5 % серы.
При проведении производственного анализа содержание белковых веществ подсчитывают не по белковому, а по общему азоту, входящему в состав всех органических и неорганических веществ. Такое отклонение в точности определения содержания белков вполне допустимо.
Обычно содержание общего азота в пищевых продуктах определяют с использованием метода Кьельдаля. В целях упрощенияи сокращения длительности анализа этот метод неоднократно подвергался модификации. В настоящее время разработаны высокопроизводительные автоматические анализаторы типа «Кьельфос».
Минерализацию (сжигание) производят нагреванием навески продукта с концентрированной серной кислотой в присутствии катализаторов (сернокислой меди или пероксида водорода), а также веществ, повышающих температуру кипения смеси (сульфата натрия или калия). Минерализация органических веществ протекает в четыре стадии по нижеприведенной схеме.
1. Гидролитический распад:
| R' | CH2 | CH | COOH | H2SO4 | COOH + R" | CH2 | CH | COOH | ||||||||||||||||
| HN | C | CH | CH2 | R" + H2O | R' | CH2 | CH | |||||||||||||||||
| O | NH | NH | NH | |||||||||||||||||||||





2. Декарбоксилирование:
| R | CH | CH |  COOH COOH | R | CH | CH | + | CO | ||||||
| NH2 | NH2 |
3. Окисление:
| CH3CH2CH2NH2 + 9 H2SO4 | NH3 + 3 CO2 + 9 SO2 + 12 H2O |
4. Связываниекислотой:
 2 NH3 + H2SO4 (NH4)2SO4
2 NH3 + H2SO4 (NH4)2SO4
Из образовавшегося сернокислого аммония аммиак вытесняют концентрированной щелочью:
 (NH4)2SO4 + 2 NaOH 2 NH4OH + Na2SO4.
(NH4)2SO4 + 2 NaOH 2 NH4OH + Na2SO4.
Выделяющийся аммиак отгоняют и улавливают титрованным раствором серной кислоты, которую берут в избытке:

 2 NH4OH 2 NH3 + H2O 2 NH3 + H2SO4 (NH4)2SO4
2 NH4OH 2 NH3 + H2O 2 NH3 + H2SO4 (NH4)2SO4
Содержание общего азота (в процентах) рассчитывают по формуле:
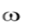 (V- (V- | V1) K 0,0014 100 | |
| m |
где V – объем 0,1 М раствора гидроксида натрия, израсходованного на титрование серной кислоты в контрольной пробе, см3; V1 – объем 0,1 М раствора гидроксида натрия, израсходованного на титрование избытка серной кислоты в рабочей пробе, см3; K – коэффициент пересчета на точный титр 0,1 М раствора гидроксида натрия, г; 0,0014 – количество азота, эквивалентное 1 см3 0,1 М раствора гидроксида натрия, г; m – масса навески образца, г.
За окончательный результат принимают среднее арифметическое значение двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,2 %. Вычисление проводят до второго знака после запятой.
Для определения азота истинных белков исследуемый образец смешивают с водой и прибавляют к смеси соответствующий реактив, осаждающий белок. Выпавший осадок белка отфильтровывают, затем проводят определение азота в осадке и фильтрате. Азот осадка соответствует белковому азоту, а азот фильтрата – небелковому. Зная содержание общего азота в образце, можно ограничиться определением азота только в осадке или в фильтрате. По разности между общим азотом и азотом, найденным в осадке или фильтрате, судят о количестве белкового и небелкового азота.
Колориметрический метод определения содержания белка (метод Лоури) основан на цветной реакции белков с реактивом Фолина.
Интенсивность окраски определяют на фотоэлектроколориметре с красным светофильтром или на спектрофотометре при длине волны 750 нм. Количество белка в растворе находят по калибровочной кривой. Метод применяют для определения содержания белка в растворах с концентрацией от 10 до 100 мкг.
В основе биуретового метода определения содержания белка лежит биуретовая реакция.
Имеются различные методы определения содержания азота, например метод Дюма. Метод заключается в разложении органического соединения в атмосфере оксида углерода до газообразного состояния с последующим измерением объема азота N2.
Широкое распространение получил метод инфракрасной спектроскопии, в основе которого лежит поглощение молекулами белков света с определенной длиной волны. Приборы калибруют по образцам с известным содержанием белка (эталонам), определяемым по методу Кьельдаля.
Известны методы количественного определения белка, основанные на различной степени помутнения (нефелометрический метод) и способности белков адсорбировать красители (кумасси синий R-250, амидочерный и др.). Данные методы характеризуются высокой точностью и простотой определения, хотя имеют ряд ограничений.
Массовую долю белка в пищевых продуктах определяют также колориметрическим методом, основанным на способности белков при рН ниже изоэлектрической точки связывать кислотные красители с образованием нерастворимых комплексов. При этом интенсивность окраски раствора уменьшается обратно пропорционально количеству белка. После удаления нерастворимого комплекса измеряют оптическую плотность раствора и по градуировочному графику определяют массовую долю белка.
Определение массовой доли белков методом формольного титрования применяют для контроля массовой доли белка в молоке кислотностью не более 22оС. Он основан на реакции щелочных аминогрупп белка с формалином, в результате которой высвобождаются карбоксильные группы белка. При этом повышается титруемая кислотность молока, по приросту которой и определяют массовую долю белка.
Для определения массовой доли белка в молоке применяют также рефрактометрический метод, основанный на изменении показателей преломления молока и безбелковой молочной сыворотки, полученной из того же образца молока, разность между которыми пропорциональна массовой доле белка в молоке.
