Молярная концентрация эквивалентов вещества в объёмном анализе. Титрование.
Молярная концентрация эквивалентов вещества Х (эвивалентная концентрация) – величина, равная отношению химического количества эквивалентов вещества Х к объёму раствора:
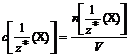 ; Или
; Или 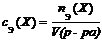
Она показывает, какое химическое количество эквивалентов вещества Х содержится в растворе объёмом 1 дм3. Например, запись  = 0,2 моль/дм3 обозначает, что в данном растворе объёмом 1 дм3 количество эквивалентов серной кислоты равно 0,2 моль. Часто молярную концентрацию эквивалента называют эквивалентной концентрацией и обозначают символом «сэ». Раньше её называли нормальной концентрацией (или нормальностью) и обозначили символами «н» или «N».
= 0,2 моль/дм3 обозначает, что в данном растворе объёмом 1 дм3 количество эквивалентов серной кислоты равно 0,2 моль. Часто молярную концентрацию эквивалента называют эквивалентной концентрацией и обозначают символом «сэ». Раньше её называли нормальной концентрацией (или нормальностью) и обозначили символами «н» или «N».
Согласно закону эквивалентов, вещества X и Y реагируют в таком соотношении, что количество эквивалентов вещества Х всегда равно количеству эквивалентов вещества Y, т. е.:
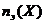 =
= 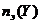 .
.
Поскольку 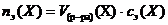 , а
, а 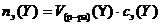 ,
,
то можно записать: Vр-ра(Х) × сэ(Х) = Vр-ра(Y) × сэ(Y)
Из этого уравнения видно, что при одинаковых концентрациях эквивалентов реагирующих веществ X и Y объёмы их растворов будут также одинаковыми. Так, например, для нейтрализации серной кислоты, содержащейся в растворе объёмом 50 см3 с концентрацией её эквивалентов, равной 0,1 моль/дм3, требуется такой же объём раствора гидроксида натрия с концентрацией его эквивалентов, равной 0,1 моль/дм3. Если же молярные концентрации эквивалентов веществ X и Y не равны между собой, то их отношение обратно пропорционально отношению объёмов растворов этих веществ:
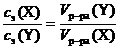 |
Это уравнение позволяет рассчитать значение эквивалентной концентрации вещества Х, если известно значение концентрации реагирующего с ним вещества Y. Данный тип расчетов очень широко используется в аналитической химии и лежит в основе метода объёмного анализа, основанного на измерении объёмов растворов реагирующих веществ.
На практике для определения эквивалентной концентрации веществ используют метод титровáния (от франц. «titre» – количество). Он заключается в том, что к определённому объёму раствора с неизвестной эквивалентной концентрацией вещества Х постепенно добавляют раствор с известной концентрацией вещества Y до момента окончания реакции, которому соответствует изменение окраски индикатора. Определив таким образом точный объём добавленного раствора вещества Y, рассчитывают эквивалентную концентрацию вещества Х в исходном растворе.
Пример 1.
На титрование раствора гидроксида калия объемом 10,0 см3 израсходован раствор объемом 12,8 см3 с эквивалентной концентрацией серной кислоты, равной 0,1200 моль/дм3. Вычислить эквивалентную концентрацию щёлочи в исходном растворе.
Решение:
Из уравнения V(кисл) × сэ(кисл) = V(щёл) × сэ(щёл)
выразим искомую концентрацию и найдем её значение:
сэ(щёл) = 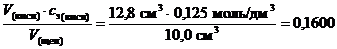 моль/дм3.
моль/дм3.
При приготовлении растворов с заданными значениями молярной концентрации эквивалентов необходимо помнить, что молярная масса эквивалента одного и того же вещества может иметь разные значения в зависимости от того, в какой реакции это вещество будет участвовать. Например, для реакции H2SO4 + NaOH ® NaHSO4 + H2O эквивалентом кислоты является её молекула и молярная масса эквивалентов равна 98 г/моль. В случае же другой реакции: H2SO4 + 2NaOH ® Na2SO4 + 2H2O эквивалентом кислоты является половина её молекулы и молярная масса эквивалентов в этом случае составляет:
M 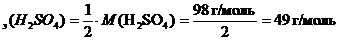 .
.
