Химия биологически активных веществ
Методические указания к лабораторным работам для студентов
Очной формы обучения по специальности 070100 – «Биотехнология»
Пермь 2006
Составитель Л.В. Аникина
УДК 547.9
Химия биологически активных веществ: метод. указания к лаборат. работам / сост. Л.В. Аникина; Перм. гос. техн. ун-т. – Пермь, 2006. – 32 с.
Дан порядок выполнения лабораторных работ по программе курса «Химия биологически активных веществ».
Предназначены для студентов очной формы обучения по направлению 550800 – «Химическая технология и биотехнология», специальность 070100 «Биотехнология».
Рецензент: канд. хим. наук В.А.Глушков
© Пермский государственный
технический университет, 2006
«Химия биологически активных веществ» является частью общего курса «Органическая химия». В течение данного курса студенты занимаются изучением элементов биоорганической химии – структурой и пространственной организацией белков, нуклеиновых кислот, углеводов, липидов, низкомолекулярных биорегуляторов.
Лабораторные работы проводятся с целью приобретения навыков и умений выделения биомолекул из биологического материала и исследования их химической структуры и химических свойств с использованием необходимых реактивов и оборудования. Проведение лабораторных работ по химии БАВ позволяет подтвердить теоретические положения и выводы по отдельным вопросам биоорганической химии и тем самым закрепить теоретические знания о строении, пространственной структуре, биологических функциях и основах функционирования белков, нуклеиновых кислот, углеводов, липидов, низкомолекулярных регуляторных молекул и продуктов жизнедеятельности клеток.
Лабораторные работы оформляются каждым студентом согласно следующему плану:
1. Дата.
2. Название лабораторной работы.
3. Цель и значение работы.
4. Принцип выделения, идентификации и количественного определения биомолекул, формулы и химизм реакций.
5. Техника выполнения работы.
6. Наблюдаемые явления и расчеты.
7. Выводы по работе.
В конце каждой работы даются контрольные вопросы, которые помогут при подготовке лабораторной работы к защите.
Лабораторная работа №1
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ УГЛЕВОДОВ В ЯБЛОКЕ
Цель работы – закрепить знания по теме «Углеводы» и овладеть методами количественного определения содержания углеводов в растительном сырье.
В различных сортах яблок содержится от 600 до 14800 мг% углеводов с преобладанием отдельных моносахаридов, а также сахарозы.
Исследуемый материал: яблоки нескольких сортов.
Реактивы:
1. 0,1 н раствор йода.
2. 0,1 н раствор натрия гидроксида.
3. 10% раствор серной кислоты.
4. 0,1 н раствор натрия тиосульфата.
5. 1% раствор крахмала.
6. 10% раствор соляной кислоты.
7. Сода.
Оборудование:
1. Плоскодонные колбы на 50 мл.
2. Водяная баня с термометром.
3. Воронки.
4. Фильтры бумажные.
5. Мерные колбы на 100 мл.
6. Пипетка на 5 мл.
7. Индикаторная бумага.
8. Мерные колбы на 50 мл.
Ход работы. Берут навеску 5 г одного из сортов яблок, прибавляют 50 мл дистиллированной воды и экстрагируют на водяной бане при температуре 70оС в течение 30 минут. Температуру бани не доводят до 100оС, чтобы избежать гидролиза сахарозы, который может идти под влиянием имеющихся в яблоках кислот. По истечении времени нагревания вытяжку отфильтровывают через складчатый фильтр в мерную колбу на 100 мл. Остаток на фильтре несколько раз промывают горячей водой. Охлажденную до комнатной температуры вытяжку с промывными водами доводят водой до метки. Отбирают пипеткой 5 мл вытяжки и определяют в ней содержание глюкозы по Вильштеттеру. Метод определения основан на свойствах окисления альдегидной группы глюкозы йодом до карбоксильной группы в присутствии фруктозы и сахарозы, которые остаются неизменными.
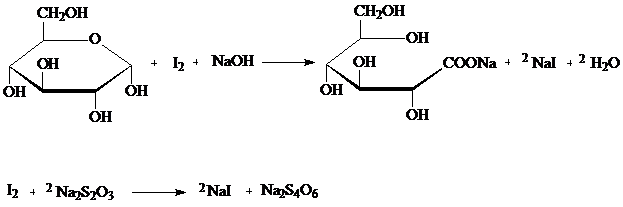
Для определения глюкозы по Вильштеттеру к 5 мл исследуемого раствора прибавляют 7 мл 0,1 н раствора йода. Через 2 минуты при энергичном перемешивании медленно добавляют 10 мл 0,1 н раствора натрия гидроксида и оставляют стоять на 20 минут. После этого раствор подкисляют 10% раствором серной кислоты до кислой рН и остаток йода титруют 0,1 н раствором натрия тиосульфата в присутствии индикатора – раствора крахмала.
Далее 25 мл вытяжки из яблок помещают в коническую колбу, прибавляют 2 мл 10% соляной кислоты и смесь выдерживают на кипящей водяной бане в течение 30 мин, затем раствор охлаждают, доводят до нейтральной рН с помощью соды, переливают в мерную колбу на 50 мл и доводят водой до метки. Далее снова определяют глюкозу по методу Вильштеттера. В этом случае будет определена свободная глюкоза + глюкоза, образовавшаяся при расщеплении сахарозы.
Указания к составлению отчета. Содержание глюкозы рассчитывают по формуле
Q=Tглюкозы × (Vйод – Vтиосульфат),
где Тглюкозы = 9 мг/мл.
Результат определения содержания глюкозы и сахарозы необходимо выразить в г/кг яблок (количество г глюкозы или сахарозы в 1 кг яблок), или в мг% (количество мг глюкозы или сахарозы в 100 г яблока). Молекулярная масса глюкозы – 180, сахарозы – 342. Написать уравнение реакции гидролиза сахарозы.
Контрольные вопросы:
1. Какие свойства глюкозы положены в основу метода ее определения?
2. Почему для определения сахарозы необходим ее гидролиз?
3. Какие органические соединения, кроме углеводов, находятся в яблоке?
4. Как вы полагаете, какое яблоко будет слаще на вкус, в котором больше глюкозы или сахарозы?
Лабораторная работа №2
РАЗДЕЛЕНИЕ ЛИПИДОВ СЫВОРОТКИ КРОВИ МЕТОДОМ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ
Цель работы – закрепить знания по теме «Липиды» и определить методом тонкослойной хроматографии отдельные фракции липидов сыворотки или плазмы крови, характеризующие липидный обмен организма и функцию печени.
Метод основан на различной скорости перемещения липидных фракций сыворотки крови (фосфолипиды, свободные жирные кислоты, холестерин, триацилглицериды) в тонком слое адсорбента при движении через него органического растворителя. Скорость разделения фракций зависит от их относительной полярности, и для их обнаружения полученные хроматограммы обрабатывают парами йода.
Исследуемый материал: сыворотка или плазма крови.
Реактивы:
1. Этанол – диэтиловый эфир (3:1).
2. Хлороформ.
3. Растворитель для хроматографии: н-гексан – диэтиловый эфир – уксусная кислота (73:25:2).
4. Йод металлический.
Оборудование:
1. Пластинки хроматографические Силуфол УФ254.
2. Камера для хроматографии.
3. Водяная баня.
4. Мерная колба на 25 мл.
5. Выпарительная чашка.
6. Пипетка на 10 мкл.
7. Камера для проявления хроматограмм.
8. Хроматоскоп.
Ход работы. В мерной колбе на 25 мл смешивают 1 мл исследуемой сыворотки крови с 10 мл приготовленной спиртово-эфирной смеси. Колбу с содержимым помещают на 30 с в кипящую водяную баню, охлаждают под струей холодной воды и доводят объем спиртово-эфирной смесью до 25 мл. Полученный липидный экстракт отфильтровывают через обезжиренный бумажный фильтр в выпарительную чашку, выпаривают досуха в кипящей водяной бане, а осадок растворяют в 0,2 мл хлороформа.
В хроматографическую камеру наливают 3 мл растворителя для хроматографии. На хроматографическую пластинку, отступая 1 см от края, пипеткой наносят 10 мкл хлороформного экстракта, помещают пластинку в камеру этим концом вниз, погрузив его на 3-5 мм в растворитель. Камеру закрывают крышкой для поддержания равномерной концентрации паров. Хроматографию проводят при комнатной температуре до тех пор, пока фронт растворителя не приблизится к верхнему краю, не доходя до него 0,5 см.
Полученную хроматограмму извлекают из камеры, высушивают на воздухе и вносят для проявления в камеру, на дно которой предварительно насыпают кристаллы металлического йода. Сосуд закрывают и подогревают на водяной бане при 60оС. Возгоняющийся йод вступает в реакцию с липидными фракциями.
Через 1 мин хроматограмму извлекают и просматривают в ультрафиолетовом свете на хроматоскопе. Фракции липидов обнаруживают в виде коричневых пятен. Ближе к линии старта расположены фосфолипиды, затем неидентифицированные соединения, холестерин, моноацилглицериды, диацилглицериды, свободные жирные кислоты, триацилглицериды и эфиры холестерина.
Указания к составлению отчета. Зарисовать полученную хроматограмму, указав в ней соответствующие липидные фракции сыворотки крови. Написать формулы представителей каждой липидной фракции в порядке убывания их относительной полярности.
Контрольные вопросы:
1. Повторите классификацию липидов.
2. Вспомните строение холестерина и его эфиров.
3. От чего зависит скорость перемещения липидов в слое сорбента при использовании органического растворителя?
4. Как возможно количественно определить липидные компоненты после разделения их методом ТСХ?
Лабораторная работа №3
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ И АМИНОКИСЛОТЫ
Цель работы – закрепить знания по аминокислотному составу белков и приобрести навыки проведения цветных реакций на белки и отдельные аминокислоты.
При взаимодействии белка с отдельными химическими веществами возникают окрашенные продукты реакции. Образование их обусловлено присутствием в молекуле белка той или иной аминокислоты, имеющей в боковом радикале определенную химическую группировку. Некоторые реакции присущи не только белкам, но и другим веществам, содержащим те же химические группировки, поэтому для установления наличия белка недостаточно проведения одной какой-нибудь реакции.
Значение цветных реакций состоит в том, что они дают возможность установить белковую природу вещества и доказать присутствие некоторых аминокислот в различных природных белках. На основании цветных реакций разработаны методы количественного определения белков и аминокислот.
Исследуемый материал: сыворотка или плазма крови, 1% раствор яичного белка (белок одного куриного яйца растворяют в 20-кратном объеме дистиллированной воды, фильтруют через марлю).
Реактивы:
1. 10% раствор NaOH.
2. 1% раствор CuSO4.
3. 0,1% водный раствор нингидрина.
4. Концентрированная азотная кислота.
5. Ледяная уксусная кислота.
6. Концентрированная серная кислота.
7. 5% раствор ацетата свинца.
Оборудование:
1. Штатив с пробирками.
2. Пипетки.
3. Песчаная баня или спиртовка.
Ход работы:
