Опыт 6. Получение и свойства средних солей
Напишите уравнения реакций средних солей:
1.___________________________________________________________________________________
2.___________________________________________________________________________________
3.___________________________________________________________________________________.
Запишите наблюдения:
1.___________________________________________________________________________________
2.___________________________________________________________________________________
3.__________________________________________________________________________________.
Напишите названия полученных солей:
1.___________________________________________________________________________________
2.___________________________________________________________________________________
3.__________________________________________________________________________________.
Вывод: (какие свойства солей наблюдали, почему реакции идут до конца?)______________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
Опыт 8.Получение основных солей
Напишите уравнения реакций получения основной соли (назовите ее) и её взаимодействие с щёлочью и кислотой:
1.___________________________________________________________________________________
2.___________________________________________________________________________________
3.___________________________________________________________________________________.
Запишите наблюдения:
1.___________________________________________________________________________________
2.___________________________________________________________________________________
3.___________________________________________________________________________________
Вывод: (какой способ получения основной соли использовали, какие свойства основных солей наблюдали)____________________________________________________________________________
_____________________________________________________________________________________
______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ФГБОУ ВПО «Уфимский государственный нефтяной технический университет»
Кафедра «Прикладная химия и физика»
Дисциплина «Химия»
ОТЧЕТ
по лабораторной работе №___
На тему: «Определение молекулярной массы эквивалента карбоната кальция»
Выполнил
студент группы__________ ______________ И.О. Фамилия
(Подпись, дата)
Принял
преподаватель кафедры ПХиФ ______________ И.О. Фамилия
(Подпись, дата)
Цель работы:
- определить молекулярную массу эквивалента карбоната кальция весовым методом на основе закона эквивалентов.
Теоретическая часть
Абсолютная атомная масса – _____________________________________________________
____________________________________________________________________________________.
Моль - ________________________________________________________________________
____________________________________________________________________________________.
Число Авогадро Na показывает____________________________________________________
____________________________________________________________________________________.
Относительная атомная масса -___________________________________________________
____________________________________________________________________________________.
Молекулярная масса - ___________________________________________________________
____________________________________________________________________________________.
Молярная масса - _______________________________________________________________
____________________________________________________________________________________.
К фундаментальным (стехиометрическим) относятся законы химии:____________________
_____________________________________________________________________________________
____________________________________________________________________________________.
Эквивалентом называется некая реальная или условная частица ________________________
____________________________________________________________________________________.
Число эквивалентности равно_____________________________________________________
____________________________________________________________________________________.
Единицей измерения количества эквивалентов является______________________________.
Величина, обратная числу эквивалентности, называется ______________________________,
которая показывает___________________________________________________________________.
Например, масса эквивалента кислорода равна ___________ г/моль.
Для газообразных веществ молярный объём эквивалента вещества называется _____________________________________так, молярный объём эквивалента кислорода равен ________ л/моль.
Закон эквивалентов:_____________________________________________________________
_____________________________________________________________________________________
____________________________________________________________________________________.
Для реакции А+В=С+Д закон эквивалентов записывается так:
____________________________________________________________________________________.
Экспериментальная часть
Определение молярной массы эквивалента карбоната кальция проводится по реакции:
________________________________________________________________________________
Записи в ходе эксперимента:
1. Вес пустой фарфоровой чашки - m1, г (________)
2. Вес фарфоровой чашки с мрамором до реакции - m2, г (_________)
3. Вес фарфоровой чашки с мрамором после реакции (после сушки) - m3, г (_________)
4. Объём соляной кислоты - 5 мл
5. Концентрация соляной кислоты - 2 н, моль/л
Обработка результатов:
1. Рассчитайте вес мрамора до реакции
m4 = m2 – m1, г
________________________________________________________________________________.
2. Рассчитайте вес мрамора после реакции
m5 = m3 – m1, г
________________________________________________________________________________.
3. Рассчитайте вес прореагировавшего мрамора
m6 = m4 – m5, г
________________________________________________________________________________.
4. Найдите массу соляной кислоты, вступившей в реакцию m(HCl) (по уравнению), г:
______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
5. Найдите молекулярную массу эквивалента карбоната кальция:
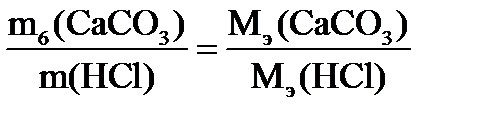 ;
;
МЭ (СaCO3) =
_________________________________________
6. Рассчитайте абсолютную и относительную ошибки опыта:
Δ MЭ = ׀Мтеор. – Мэксперим.׀
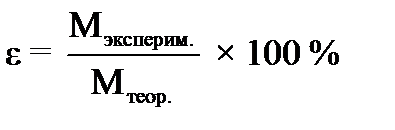
Вывод:(каким методом определили молярную массу эквивалента карбоната кальция, о чем говорят результаты расчета ошибок)________________________________________________________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
Нарисуйте схематично химическую посуду, используемую в лаборатории.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ФГБОУ ВПО «Уфимский государственный нефтяной технический университет»
Кафедра «Прикладная химия и физика»
Дисциплина «Химия»
ОТЧЕТ
по лабораторной работе №___
На тему: «Химическая кинетика. Катализ»
Выполнил
студент группы__________ ______________ И.О. Фамилия
(Подпись, дата)
Принял
преподаватель кафедры ПХиФ ______________ И.О. Фамилия
(Подпись, дата)
Цель работы:
- изучить влияние концентрации, поверхности реагирующих веществ, присутствия катализаторов на скорость химической реакции;
- оценить каталитическую активность катализатора.
Теоретическая часть
Химическая кинетика – это раздел химии, изучающий ____________________________ ______________________________________. Скоростью химической реакции называют ___________________________________________________________________________________ ____________________________________________________________________________________.Скорость гомогенной реакции выражается формулой:
Vгомог.=
_____________________
Скорость реакции зависит от различных факторов.
Зависимость скорости химической реакции от концентрации выражается законом действия масс: ________________________________________________________________________________ _______________________________________________________________________________________________________________________________________________________________________.
Например, для реакции 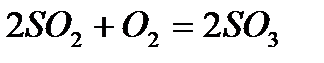 закон действия масс может быть записан:
закон действия масс может быть записан:
___________________________________________________________________________________
где 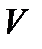 - ___________________;
- ___________________; 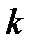 - __________________________; [ ] - _____ ___________________________________________________________________________________.
- __________________________; [ ] - _____ ___________________________________________________________________________________.
Данная система является гомогенной, так как _______________________________________ ___________________________________________________________________________________. Особенность гетерогенных процессов заключается в том, что они____________________________ ____________________________________________________________________. Поэтому скорость химических реакций в гетерогенных системах при постоянной температуре зависит и от _______________________________________________________. Скорость гетерогенной реакции выражается формулой:
Vгетер.=
_____________________
С ростом температуры скорость химической реакции резко возрастает. Зависимость скорости реакции от температуры выражается правилом ____________________________: _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________ и выражается формулой:
______________________________
где V(T1), V(Т2) - ____________________________________________; 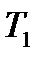 и
и 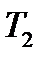 - __________ _________________________________________;
- __________ _________________________________________; 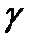 - _______________________________________, показывающий на сколько _________________________________________при повышении температуры на 10°С.
- _______________________________________, показывающий на сколько _________________________________________при повышении температуры на 10°С.
Лишь определенная часть общего числа соударений молекул реагирующих веществ приводит к химическому взаимодействию. Такие соударения называются _____________________.
Энергия активации – это _________________________________________________________ _______________________________________________________________________________________________________________________________________________________________________.
Одним из методов ускорения химической реакции является катализ, который, осуществляется при помощи катализаторов – веществ, ________________________________ _____________________________________________. Механизм действия катализатора сводится к _________________________________________________________________________________.
Вещества, снижающие скорость химической реакции, называются _____________________.
Автокатализ – это ______________________________________________________________ _______________________________________________________________________________________________________________________________________________________________________.
Экспериментальная часть
