Основные положения молекулярно-кинетической теории и их опытное обоснование
Основные положения молекулярно-кинетической теории и их опытное обоснование
Основные положения молекулярно-кинетической теории (МКТ) вещества состоят в следующем:
1)Все вещества состоят из мельчайших частиц: молекул, атомов, ионов и др.
Молекула — мельчайшая частица вещества, способная к самостоятельному существованию и сохраняющая некоторые его свойства. Молекулы, образующие данное вещество, совершенно одинаковы; различные вещества состоят из различных молекул. В природе существует чрезвычайно большое количество различных молекул. Молекулы состоят из более мелких частиц - атомов.
Атомы — мельчайшие частицы химического элемента, сохраняющие его химические свойства. Число различных атомов сравнительно невелико и равно числу химических элементов (105) и их изотопов (около 1500). Атомы представляют собой весьма сложные образования, но классическая МКТ рассматривает их как твердые неделимые частички сферической формы, взаимодействующие между собой по законам механики.
Доказательством молекулярного строения вещества является диффузия, распространение запахов, при котором отдельные молекулы раздражают центры обоняния, а также фотографии молекул, полученные с помощью электронного микроскопа и ионного проектора.
2)Молекулы находятся на определенных расстояниях друг от друга.
Доказательством этого является возможность сжатия твердых тел и растворения одних веществ в других.
Величина этих расстояний зависит от степени нагретости тела и агрегатного состояния вещества.
3)Молекулы связаны друг с другом силами молекулярного взаимодействия - притяжения и отталкивания.
Эти силы зависят от расстояния между частицами (см.ниже, 6.4).
Опытным доказательством этого положения является трудность сжатия и растяжения твердых и жидких тел.
4)Молекулы находятся в непрерывном беспорядочном (тепловом) движении.
Характер теплового движения (поступательное, колебательное, вращательное) молекул зависит от характера их взаимодействия и изменяется при переходе вещества из одного агрегатного состояния в другое. Интенсивность теплового движения зависит от степени нагретости тела, характеризуемой абсолютной температурой. Доказательством этого положения является броуновское движение, диффузия, распространение запахов, испарение веществ и др. В настоящее время МКТ обоснована не какими-то отдельными экспериментами, а успешным развитием и применением на практике больших разделов физики и химии, использующих основные представления МКТ.
Диффузия
Диффузия — самопроизвольное взаимное проникновение молекул соприкасающихся веществ. При диффузии молекулы одного тела, находясь в непрерывном движении, проникают в промежутки между молекулами другого соприкасающегося с ним тела и распределяются между ними. В одном и том же неоднородном веществе вследствие движения молекул концентрация вещества выравнивается — вещество становится однородным.
Диффузия проявляется во всех телах — в газах, жидкостях и твердых телах, — но в разной степени. Диффузию в газах можно наблюдать, если, например, сосуд с пахучим газом открыть в помещении. Через некоторое время газ распространится по всему помещению.
Диффузия в жидкостях происходит значительно медленнее, чем в газах. Например, если в стакан налить сначала слой раствора медного купороса, а затем очень осторожно добавить слой воды и оставить стакан в помещении с неизменной температурой, где бы он не подвергался никаким сотрясением, то через некоторое время исчезнет резкая граница между купоросом и водой, а через несколько дней жидкости перемешиваются, несмотря на то, что плотность купороса больше плотности воды.
Диффузия в твердых телах происходит еще медленнее, чем в жидкостях (от нескольких, часов до нескольких лет). Она может наблюдаться только в хорошо отшлифованных телах, когда расстояние между поверхностями отшлифованных тел близки к расстоянию между молекулами (10~8 см). При этом скорость диффузии увеличивается при повышении температуры и давления.
Броуновское движение
Броуновское движение открыто в 1827 г. английским ботаником Р.Броуном, теоретическое обоснование с точки зрения МКТ дано в 1905 г. Эйнштейном и Смолуховским.
Броуновское движение — это беспорядочное движение мельчайших твердых частиц "взвешенных" в жидкостях (газах).
"Взвешенные" частицы — это частицы, распределенные по объему жидкости, не оседающие на дно и не всплывающие на поверхность жидкости.
Для броуновского движения характерно:
1) броуновские частицы совершают непрерывное хаотическое движение, интенсивность которого зависит от температуры и от размеров броуновской частицы;
2) траектория движения броуновской частицы очень сложная, не зависит от природы частиц и внешних условий.
3) Броуновское движение наблюдается в жидкостях и газах. Причинами броуновского движения являются:
1) хаотическое движение молекул среды 2)Нескомпенсированость ударов малекул на данную частичу Броуновское движение свидетельствует, что молекулы действительно существуют и что они непрерывно и хаотически движутся.
Масса молекул
Измерить массу молекулы обычным путем, т.е. взвешиванием, конечно, невозможно. Она для этого слишком мала. В настоящее время существует много методов определения масс молекул, в частности - с помощью масс-спектрографа. С их помощью определены массы то всех атомов таблицы Менделеева.
Так, для изотопа углерода 12/6*С т0= 1,995 ■ 10~26 кг.
Поскольку массы атомов и молекул чрезвычайно малы, то при расчетах обычно используют не абсолютные, а относительные значения масс, получаемые путем сравнения масс атомов и молекул с атомной единицей массы, в качестве которой выбрана 1/12 часть массы атома углерода 1 а.е.м. = 1/12 *т0C= 1,660 • 10'27 кг .
Относительной молекулярной (или атомной) массой Мr
называют величину, показывающую, во сколько раз масса молекулы (или атома) больше атомной единицы массы. Относительная молекулярная (атомная) масса является безразмерной величиной.
Относительные атомные массы всех химических элементов указаны в таблице. Относительная молекулярная масса данного вещества равна сумме относительных атомных масс элементов, входящих в состав данного вещества. Ее рассчитывают, пользуясь таблицей Менделеева и химической формулой вещества.
Так, для воды (Н2О ) Мr= 1*2 + 16 = 18.
Размеры молекул
Размер молекулы является величиной условной. Между молекулами наряду с силами притяжения действуют и силы отталкивания, поэтому молекулы могут сближаться лишь до некоторого расстояния.
Расстояние предельного сближения центров двух молекул называют эффективным диаметром молекулы d (при этом считают, что молекулы имеют сферическую форму).
Метод определения размеров малек:
В твердых и жидких телах молекулы расположены очень близко одна к другой, почти вплотную. Поэтому можно считать, что V, занимаемый телом некоторой массы т, приблизительно = сумме объемов всех его молекул.V1=V/N; N=m/M*Na;V1=VM/mNa;
ρ=m/V-плотность тела. малекула—шар, то d=2r; V1=4/3πr^3=πd^3/6;
d= 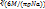 ; Размеры молекул очень малы.
; Размеры молекул очень малы.
Идеальный газ
Форму и объем тела определяет совместное действие двух факторов: 1) взаимодействие молекул, которое стремится удержать молекулы на определенных расстояниях друг от друга; 2) хаотическое движение молекул, которое разбрасывает их по всему объему.
Молекулы газа разлетаются по всему предоставленному для него объему. Следовательно, главную роль в поведении газа играет хаотическое движение молекул, а силы взаимодействия малы, и ими можно пренебречь. Это означает, что молекулы газа движутся равномерно и прямолинейно, пока не столкнутся с другими молекулами. При столкновении изменяется величина и направление скорости движения молекулы, и она снова движется равномерно прямолинейно до следующего столкновения. Длина свободного пробега (расстояние между двумя последовательными столкновениями молекулы) X ~ 10~7 м. При такой длине свободного пробега только 0,04% пространства, занятого газом, приходится на собственный объем его молекул. Это дает право воспользоваться моделью идеального газа.
Идеальный газ — это газ с достаточно простыми свойствами:
1) молекулы его исчезающе малы и их собственным объемом можно пренебречь, по сравнению с объемом сосуда, в котором находится газ;
2) между молекулами идеального газа нет сил взаимодействия;
3) молекулы идеального газа ведут себя при столкновениях как абсолютно упругие шарики.
При небольших давлениях и не очень низких температурах реальные газы близки к идеальному газу.При высоких давлениях молекулы газа сближаются, что пренебречь их собственным объемом нельзя и между ними возникают заметные силы притяжения.При низких температурах кинетическая энергия уменьшается и становится сравнимой с потенциальной энергией и пренебречь последней нельзя.
Для описания свойств газов можно пользоваться:1)микроскопическими параметрами (скорость, масса молекулы, ее энергия и др.), которые являются индивидуальными характеристиками молекул и численные значения которых находятся только расчетным путем; 2) макроскопическими параметрами (давление, температура, объем газа), значение которых определяется совместным действием огромного числа молекул. Макропараметры — это параметры газа как физического тела. Численные значения их находят простым измерением с помощью приборов.
Давление газа — это средняя сила ударов молекул о тело (например, о стенки сосуда), отнесенная к единице его поверхности.
Абсолютная температура Т— мера средней кинетической энергии хаотического движения молекул (см. раздел 6.11).
Под объемом газа понимают объем сосуда, в котором находится газ.
Скорости молекул газов
Движение молекул газа подчиняется законам статистической физики. В каждый момент времени скорости отдельных молекул могут значительно отличаться друг от друга, но их средние значения одинаковы и при расчетах используются не мгновенные скорости отдельных молекул, а некоторые средние значения. Различают среднюю арифметическую <u> и среднюю квадратичную <Uкв> скорость хаотического движения молекул.
Пусть имеется N молекул, скорости которых соответственно u1, u2,…., un. Средняя арифметическая скорость хаотического движения молекул по модулю равна
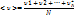
Средняя квадратичная скорость хаотического движения молекул
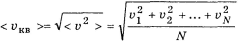
где<υ^2>-средний квадрат скорости движ. молекул.Его не следует с квадратом средней скорости< υ ^2>≠(< υ >)^2.Как показывают расчеты 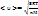 ;
; 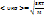 ;R-универ.газ постоянная.R=8.31Дж/моль*К; R=KNa ;
;R-универ.газ постоянная.R=8.31Дж/моль*К; R=KNa ;
Измерение температуры
Чтобы измерить темп. тела, его необходимо привести в тепловой контакт с термометром. Термометр фиксирует свою собственную темп., равную темп. тела, с которым он находится в термическом равновесии. Для измерения температуры можно воспользоваться зависимостью(V,P и др.) от температуры. В метрической системе принята шкала Цельсия
Термометры облодают недостатками:1)ограниченность диапозона температур (при низ. Темп. жидкость затвердев., при высокой испор)
2)показания не совсем точные.
В отличии от жидкости все идеальн газы при нагрев одинаково измен свой V,P, причём P газа прямопропорционально T. Давление газа при V=const можно считать в качестве T. Соединив сосуд , в котором находится газ с монометром, можно измерить T по показаниям монометра. Такой прибор наз. газовым термометром. Газовый термометр непригоден для опредиления T при высокой и низкой T
Внутренняя энергия тел
В состав внутренне энергии входят: 1)WKEN поступательная, вращательная и калебательного движения молекул и атомов; 2)потенциальная W взаимодействия атомов и малекул; 3)W электронных оболочек атомов; 4)внутри-ядерная W.
Внутренняя энерг. в Т/д представляют собой сумму WKEN всех малекул+Wпотенц. их взаимодействия. U=WKEN+Wпот. –Внутр. энерг.
В идеальном газе малекулы не взаимод. между собой,поэтому Wпот.=0 и внутрен. энерг. U=WKEN
Внутрен. энерг. представляет собой WKEN всех молекул зависит только от T и числа малекул. Изминение внутрен. энерг. определ. только изменением T и не зависит от характера процесса. ΔU=U2-U1; ΔT=T2-T1; U=NWKEN=3/2Nа kT; N= Nа; WKEN=3/2kT;
Количестао теплоты
Мерой изменения Wмех является А работа сил, приложенных к системе.ΔWмех=А. При теплообмене происходит изменения внутренней энергии тела.Мера изменения внутр. энергии –является
количеством теплоты.Количества теплоты- мера изменения внутр. энерг. которое тело получает в процессе теплообмена Q=ΔU.[Q]=1Дж
Количество теплоты необходимое для нагревания тела массой m от темп. Т1 до Т2,рассчитывается по форм.:Q=cm(T2-T1)=cmΔT. C-удел. теплоемкость вещества. с=Q/m(T2-T1). [c]=1дж/кг*К.
Удельная теплоемкость-равна колич.теплоты которое неоходимо сообщить телу m 1кг, чтобы нагреть его на 1Кл.Теплоемкость тела-
Ст=Q/(T2-T1)=cm.[C]=Дж/Кл.Для превращения жидкость в пар при T=const необходимо затр. Q=rm.r-уделю теплота парообразования.
При конденсации пара выдел. тоже кол. теплоты Q=-rm.
Для расплавления тела массой m при Т плав.неоходимо сообщ.телу Q
λ-удел. теплота плав. Q, которое выделяется при полном сгорании топлива =: Q=qm. q-удельная теплота сгорания.
Работа в термодинамике
F Газ с темп. Т1 нагрев. до Т2.Газ изобарически
2 расширяется и поршень переместится из
полож. 1 в 2.Газ совершает А против
F внешней F.Так как Р=const, то F=pS тоже
1 соnst. А рассчитывается: A=FΔL=pSΔL=pΔV=
L1 L2 ; =p(V2-V1).Газ выполняет А в процессе
изменения V причем газ расшир. и А>0,
ΔV>0.При зжатии газ V<0,A<0.
Уравн. Миндилеева-Клаперона:pV/T=m/M*R; pV1= m/M*R*T1;
pV2= m/M*R*T2; pV2-pV1= m/M*R*T2- m/M*R*T1; pΔV= m/M*R*ΔT.
A=pΔV;A= m/M*R*ΔT.Если m=M=1, ΔT=1К,то A=R.
Первый закон термодинамики
Первый закон термодинамики — это закон сохранения и превращения энергии в применении к тепловым процессам.
Если механическая энергия системы не изменяется, а система не замкнута и между ней и окружающей средой происходит теплообмен, то изменяется внутренняя энергия.
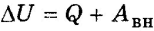
Первый закон термодинамики формулируется так:
изменение внутренней энергии при переходе системы из одного состояния в другое равно работе внешних сил плюс количество теплоты, переданное системе в процессе теплообмена.
Если вместо работы внешних сил Авнввести работу А системы над внешними телами А = -Авн, то запишется: 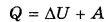
Тогда I закон термодинамики можно сформулировать так: количество теплоты, сообщенное системе, идет на изменение ее внутренней энергии и на совершение системой работы против внешних сил.
Из первого закона термодинамики вытекает невозможность создания вечного двигателя первого рода, т.е. такого двигателя, который совершал бы работу без затраты энергии извне.
Действительно, если к системе не подводится энергия Q = 0, то А =-ΔU и работа может быть совершена за счет убыли внутренней энергии системы. После того, как запас энергии окажется исчерпанным, двигатель перестанет работать.
Если система замкнута (Авн=0) и адиабатически изолирована (Q = 0) то первый закон термодинамики будет иметь вид:ΔU=0
Если в такой системе имеются тела с различной температурой, то между ними будет происходить теплообмен: тела, у которых температура выше, будут отдавать энергию и охлаждаться, а тела с меньшей температурой будут получать энергию и нагреваться. Это будет происходить до тех пор, пока температуры у всех тел не станут одинаковыми. При этом ΔU1+ΔU2+…ΔUn=0 или Q1+Q2+…+Qn=0
Первый закон термодинамики для незамкнутой и адиабатически изолированной системы называют уравнением теплового баланса.
Адиобатный процесс
Адиобатный проц.-проц., происход. без P адиоб.
теплообмена системы с окруж. средой т.е.
Q=0; ΔU+A=0; A=- ΔU; При адиобатн проц A изот.
может выполнятся за счёт уменьшен внутр. эн.
A>0 то ΔU<0 т.е. U2<U1,то T2<T1. A<0 то ΔU>0.
При адиаб расширении совершает роб. над V
окруж. сред.и сам охлождается A>0.
При адиаб. сжатии внешние силы совершает роб. над газом и газ нагревается
КПД теплавого двигателя.
Для идеального тепл. двиг: А=А1-А2=Q1-Q2. КПД–отношение полезной А к количеству теплоты, которое получило раб.тело от нагревателя. КПД (η)η=А/Q1=Q1-Q2/Q1=1-Q2/Q1. η<1.
Цикл Карно:наибольшее КПД для идеального двиг. получ.,если он работает по циклу Карно,состоящей из 2-х изотерм и2-х адиабат.
P 1 1-2,3-4}изотерма. η=T1-T2/T1=1-T2/T1
T1 2 2-3,4-1}адиабата.
4 Q=0.
T2 3
V
Испарение и конденсация
Переход вещества в газообразное состояние наз.-парообразованием.
Совокупность молекул, вылетевших из вещества, наз.- паром. Процесс парообразования связан с увеличением внутренней энергии вещества.Парообразование происходящее прямо из твердого состояния—сублимация.Испарение—это парообразование, происходящее при любой T. Закономерности:1) при одинаковых условиях различные вещества испаряются с различной скоростью.
скорость испорения больше:2) чем больше площадь свободной поверхности жидкости;3) чем меньше плотность паров над поверхностью жидкости. Скорость увеличивается при ветер;4) чем больше температура жидкости;5) при испарении температура тела понижается;6) испарение происходит до тех пор, пока все вещество не испарится.Скорость испарения-число молекул переходящих в пар с поверхности в-ва за 1с.Механизм испарения можно объяснить с точки зрения МКТ: молекулы, находящиеся на поверхности, удерживаются силами притяжения со стороны других молекул вещества. Молекула может вылететь за пределы жидкости лишь тогда, когда ее WKEN>AВЫХ. Поэтому покинуть вещество могут только быстрые молекулы. В результате средняя WKEN оставшихся молекул уменьшается, а температура жидкости понижается.Количество теплоты Q, необходимое для превращение жидкости в пар при постоянной температуре, наз.- теплотой парообразования.
Экспериментально установлено, что Q=г*т,где т—масса испарившейся жидкости, г — удельная теплота парообразования. r— величина, численно равная количеству теплоты, необходимому для превращения в пар жидкости единичной массы при неизменной температуре.г зависит от рода жидкости и внешних условий. При увеличении T r уменьшается. Это объясняется тем, что все жидкости при нагревании расширяются.Расстояния между молекулами при этом увеличиваются и силы молекулярного взаимодействия уменьшаются. Кроме того, чем больше T,тем больше средняя WKEN движения молекул и тем меньше энергии им нужно добавить, чтобы они могли вылететь за пределы поверхности жидкости.Молекулы пара хаотически движутся. Поэтому какая-то часть движется в сторону жидкости и, достигнув поверхности, втягивается в нее силами притяжения со стороны молекул поверхности и снова становится молекулами жидкости. Число конденсирующихся за определенный промежуток времени молекул тем больше, чем больше концентрация молекул пара, а следовательно, чем больше давление пара над жидкостью. Конденсация пара сопровождается нагреванием жидкости. При конденсации выделяется такое же количество теплоты, которое было затрачено при испарении.
Свойства жидкостей
По своим физ. свойствам жидкости занимают промежуточное положение между реальными газами и твердыми телами. Как твердые:1)Сохраняют V. 2)Не сжимаются. 3)Есть границы раздела.
Как газы:1)не сохраняют форму.Молекулы жидкости совершают непрерывные беспорядочные движения самых различных типов.Жидкости ближе к твердым телам, чем к газам. На это указывает" количественная близость их плотностей, удельных теплоем-костей, коэффициентов объемного расширения.
Поверхностная энергия
Наиболее характерным свойством жидкости, отличающим ее от газа, является то, что на границе с газом жидкость образует свободную поверхность, наличие которой приводит к возникновению явлений особого рода, называемых поверхностными.На каждую молекулу жидкости действуют силы притяжения со стороны окружающих ее молекул.На молекулу расположенную внутри жидкости, действуют силы со стороны таких же молекул, и равнодействующая этих сил близка к 0.Для молекулу находящейся частично на поверхности эти равнодействующие отличны от нуля и направлены они внутрь жидкости перпендикулярно к ее поверхности. Таким образом, все молекулы жидкости, находящиеся в поверхностном слое, втягиваются внутрь жидкости. Но пространство внутри жидкости занято другими молекулами, поэтому поверхностный слой создает давление на жидкость и малек. жидк. стремятся перейти в глубь (молекулярное давление).Молекулы поверхностного слоя жидкости обладают дополнительной потенциальной энергией по сравнению с молекулами внутри жидкости-поверхностной энергией.Очевидно, что величина поверхностной энергии тем больше, чем больше площадь свободной поверхности.
Пусть площадь свободной поверхности изменилась наΔS, при этом поверхностная энергия изменилась наΔWP=αΔS,где α — коэффициент поверхностного натяжения. Так как для этого изменения необходимо совершить работу A=ΔWP;A= αΔS α=A/ΔS; [α]=1Дж/м2
Коэффициент поверхностного натяжения — величина, числено равная работе, совершенной молекулярными силами при уменьшении площади свободной поверхности жидкости на единицу.
Жидк. стремится уменьшить свою S свободной поверхности,стрем. к форме шара.
Поверхностное натяжение
Равнодействующая сил, действующих на все молекулы, находящиеся на границе поверхности, и есть сила поверхностного натяжения.Она действует так,что стремится сократить поверхность жидкости.Сила поверхностного натяжения Р прямо пропорциональна длине I поверхностного слоя жидкости;Рассмотрим вертикальный прямоугольный каркас.подвижная часть перемещается из положения 1 в положение 2.Найдем работу, совершаемую при перемещении поперечины на расстояние h , А = 2Fh , где F — сила, поверхностного натяжения. А = 2α ΔS = 2αLh . 2Fh=α2Lh F=αL α=F/L.[α]=H/м
FНАТ 2
h L
FТЯЖ
Коэффициент поверхностного натяжения(α) численно равен силе поверхностного натяжения, действующей на единицу длины границы свободной поверхности жидкости.α зависит от природы жидкости, от температуры и от наличия примесей.При Т крит. α=0. Ткритическое- это темп. при которой исчезает разница между жидкостью и ее насыщ. паром.Примеси, в основном, уменьшают α.
Основные положения молекулярно-кинетической теории и их опытное обоснование
Основные положения молекулярно-кинетической теории (МКТ) вещества состоят в следующем:
1)Все вещества состоят из мельчайших частиц: молекул, атомов, ионов и др.
Молекула — мельчайшая частица вещества, способная к самостоятельному существованию и сохраняющая некоторые его свойства. Молекулы, образующие данное вещество, совершенно одинаковы; различные вещества состоят из различных молекул. В природе существует чрезвычайно большое количество различных молекул. Молекулы состоят из более мелких частиц - атомов.
Атомы — мельчайшие частицы химического элемента, сохраняющие его химические свойства. Число различных атомов сравнительно невелико и равно числу химических элементов (105) и их изотопов (около 1500). Атомы представляют собой весьма сложные образования, но классическая МКТ рассматривает их как твердые неделимые частички сферической формы, взаимодействующие между собой по законам механики.
Доказательством молекулярного строения вещества является диффузия, распространение запахов, при котором отдельные молекулы раздражают центры обоняния, а также фотографии молекул, полученные с помощью электронного микроскопа и ионного проектора.
2)Молекулы находятся на определенных расстояниях друг от друга.
Доказательством этого является возможность сжатия твердых тел и растворения одних веществ в других.
Величина этих расстояний зависит от степени нагретости тела и агрегатного состояния вещества.
3)Молекулы связаны друг с другом силами молекулярного взаимодействия - притяжения и отталкивания.
Эти силы зависят от расстояния между частицами (см.ниже, 6.4).
Опытным доказательством этого положения является трудность сжатия и растяжения твердых и жидких тел.
4)Молекулы находятся в непрерывном беспорядочном (тепловом) движении.
Характер теплового движения (поступательное, колебательное, вращательное) молекул зависит от характера их взаимодействия и изменяется при переходе вещества из одного агрегатного состояния в другое. Интенсивность теплового движения зависит от степени нагретости тела, характеризуемой абсолютной температурой. Доказательством этого положения является броуновское движение, диффузия, распространение запахов, испарение веществ и др. В настоящее время МКТ обоснована не какими-то отдельными экспериментами, а успешным развитием и применением на практике больших разделов физики и химии, использующих основные представления МКТ.
Диффузия
Диффузия — самопроизвольное взаимное проникновение молекул соприкасающихся веществ. При диффузии молекулы одного тела, находясь в непрерывном движении, проникают в промежутки между молекулами другого соприкасающегося с ним тела и распределяются между ними. В одном и том же неоднородном веществе вследствие движения молекул концентрация вещества выравнивается — вещество становится однородным.
Диффузия проявляется во всех телах — в газах, жидкостях и твердых телах, — но в разной степени. Диффузию в газах можно наблюдать, если, например, сосуд с пахучим газом открыть в помещении. Через некоторое время газ распространится по всему помещению.
Диффузия в жидкостях происходит значительно медленнее, чем в газах. Например, если в стакан налить сначала слой раствора медного купороса, а затем очень осторожно добавить слой воды и оставить стакан в помещении с неизменной температурой, где бы он не подвергался никаким сотрясением, то через некоторое время исчезнет резкая граница между купоросом и водой, а через несколько дней жидкости перемешиваются, несмотря на то, что плотность купороса больше плотности воды.
Диффузия в твердых телах происходит еще медленнее, чем в жидкостях (от нескольких, часов до нескольких лет). Она может наблюдаться только в хорошо отшлифованных телах, когда расстояние между поверхностями отшлифованных тел близки к расстоянию между молекулами (10~8 см). При этом скорость диффузии увеличивается при повышении температуры и давления.
Броуновское движение
Броуновское движение открыто в 1827 г. английским ботаником Р.Броуном, теоретическое обоснование с точки зрения МКТ дано в 1905 г. Эйнштейном и Смолуховским.
Броуновское движение — это беспорядочное движение мельчайших твердых частиц "взвешенных" в жидкостях (газах).
"Взвешенные" частицы — это частицы, распределенные по объему жидкости, не оседающие на дно и не всплывающие на поверхность жидкости.
Для броуновского движения характерно:
1) броуновские частицы совершают непрерывное хаотическое движение, интенсивность которого зависит от температуры и от размеров броуновской частицы;
2) траектория движения броуновской частицы очень сложная, не зависит от природы частиц и внешних условий.
3) Броуновское движение наблюдается в жидкостях и газах. Причинами броуновского движения являются:
1) хаотическое движение молекул среды 2)Нескомпенсированость ударов малекул на данную частичу Броуновское движение свидетельствует, что молекулы действительно существуют и что они непрерывно и хаотически движутся.
Масса молекул
Измерить массу молекулы обычным путем, т.е. взвешиванием, конечно, невозможно. Она для этого слишком мала. В настоящее время существует много методов определения масс молекул, в частности - с помощью масс-спектрографа. С их помощью определены массы то всех атомов таблицы Менделеева.
Так, для изотопа углерода 12/6*С т0= 1,995 ■ 10~26 кг.
Поскольку массы атомов и молекул чрезвычайно малы, то при расчетах обычно используют не абсолютные, а относительные значения масс, получаемые путем сравнения масс атомов и молекул с атомной единицей массы, в качестве которой выбрана 1/12 часть массы атома углерода 1 а.е.м. = 1/12 *т0C= 1,660 • 10'27 кг .
Относительной молекулярной (или атомной) массой Мr
называют величину, показывающую, во сколько раз масса молекулы (или атома) больше атомной единицы массы. Относительная молекулярная (атомная) масса является безразмерной величиной.
Относительные атомные массы всех химических элементов указаны в таблице. Относительная молекулярная масса данного вещества равна сумме относительных атомных масс элементов, входящих в состав данного вещества. Ее рассчитывают, пользуясь таблицей Менделеева и химической формулой вещества.
Так, для воды (Н2О ) Мr= 1*2 + 16 = 18.
