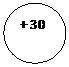Перечень лабораторных и практических работ
ХИМИЯ
Методические указания
по выполнению лабораторных и практических работ
для всех специальностей
I курса на базе основного общего образования
технический профиль
Белово 2015
Составлены в соответствии с требованиями к предъявляемыми к минимуму содержания и уровню подготовки студентов I курса всех специальностей технического профиля и рабочей программой утвержденной методическим советом техникума
Протокол №_____ «___» ________ 20___г.
| Одобрено ПЦК социально-экономических дисциплин и базисной подготовки Протокол №_____ от «____»_____________20__г от «____»_____________20__г Председатель ПЦК ____________М.И.Сюбаева ____________М.И.Сюбаева | Утверждено Методическим советом ГОУ СПО «Беловский политехнический техникум» Протокол №____ от «___» ____________ 20__г. от «___» ____________ 20__г. Зам. директора по НМР ____________Т.П. Салтымакова ____________Т.П. Салтымакова |

Составитель
Преподаватель общеобразовательных
дисциплин Н.Б. Таюшова
Рецензент
Преподаватель спецдисциплин З.С. Калачук
Внешний рецензент
Нач. отдела по НР
БФ ГБОУ ВПО «КузГТУ»
д.б.н. Л.И. Законнова
СОДЕРЖАНИЕ
Введение 4
Перечень лабораторных и практических работ 5
Практическая работа № 1 6
Лабораторная работа № 1 8
Практическая работа № 2 10
Лабораторная работа № 2 12
Лабораторная работа № 3 15
Лабораторная работа № 4 18
Лабораторная работа № 5 20
Лабораторная работа №6 21
Лабораторная работа № 7 23
Лабораторная работа № 8 24
Лабораторная работа № 9 25
Лабораторная работа № 10 27
Лабораторная работа № 11 29
Лабораторная работа № 12 32
Список литературы 36
ВВЕДЕНИЕ
Практические работы по дисциплине «Химия» составляют важную часть практической подготовки будущих специалистов. Выполнение студентами практических заданий направлено на:
-обобщение, систематизацию, углубление, закрепление полученных теоретических знаний по конкретным темам дисциплины;
-формирование умений применять полученные знания на практике;
-выработку при решении поставленных задач таких профессионально значимых качеств, как самостоятельность, ответственность, точность, творческая инициатива.
На выполнение лабораторных и практических работ рабочей программой предусмотрено 28 часов.
После выполнения лабораторных и практических работ студенты должны составить письменный отчет о проделанной работе.
В результате выполнения практических работ
студент должен:
уметь
- уметь характеризовать химический элемент по положению в периодической системе, свойства простых и сложных веществ на основе их состава и строения;
- сравнивать, анализировать, сопоставлять, самостоятельно применять и систематизировать знания;
- разъяснять на примерах причины многообразия органических веществ, причинно - следственную зависимость между составом, строением и свойствами веществ;
- составлять уравнения химических реакций, подтверждающих химические свойства неорганических и органических веществ;
- проводить расчеты по химическим формулам и уравнениям;
- выполнять обозначенные в лабораторных работах эксперименты, соблюдая правила техники безопасной работы в химической лаборатории
Перечень лабораторных и практических работ
| № темы | № п/п | Наименование лабораторных работ | Кол-во часов |
| 1.3 | 1. | «Ознакомление со свойствами дисперсных систем» | |
| 1.5 | 2. | «Изучение свойств кислот» | |
| 1.5 | 3. | «Изучение свойств солей. Гидролиз солей различного типа» | |
| 1.6 | 4. | «Типы химических реакций» | |
| 1.6 | 5. | «Скорость химической реакции» | |
| 1.7 | 6. | «Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа» | |
| 1.7 | 7. | «Получение, собирание и распознавание газов. Решение экспериментальных задач» | |
| 2.1 | 8. | «Изготовление моделей молекул органических веществ» | |
| 2.2 | 9. | «Ознакомление с коллекцией образцов нефти и продуктов ее переработки. Ознакомление с коллекцией каучуков и образцами изделий из резины» | |
| 2.3 | 10. | «Изучение свойств кислородосодержащих органических веществ» | |
| 2.4 | 11. | «Изучение свойств белка» | |
| 2.4 | 12. | «Решение экспериментальных задач на идентификацию органических соединений. Распознавание пластмасс и волокон» | |
| Итого: | часа |
| № темы | № п/п | Наименование практических работ | Кол-во часов |
| 1.2 | 1. | «Периодическая таблица химических элементов. Строение атома» | |
| 1.4 | 2. | «Приготовление раствора заданной концентрации» | |
| Итого: | часов |
ПРАКТИЧЕСКАЯ РАБОТА № 1
Часа
Тема «Периодическая таблица химических элементов. Строение атома»
Цель: систематизация знаний о Периодической системе химических элементов Д.И. Менделеева, строении атома, о взаимосвязи строения атомов химических элементов от положения в Периодической системе химических элементов.
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Задание: пользуясь выше перечисленными учебными пособиями и примером выполнения задания, дайте полную характеристику химическому элементу по плану. Результаты работы оформите в таблицу.
| № варианта | |||||||||||
| 1. | Химический элемент | P | Сa | N | Be | C | Na | S | AI | CI | K |
| 2. | Период | ||||||||||
| 3. | Группа | ||||||||||
| 4. | Подгруппа | ||||||||||
| 5. | Порядковый номер элемента | ||||||||||
| 6. | Атомная масса элемента | ||||||||||
| 7. | Формула высшего оксида | ||||||||||
| 8. | Количество энергетических уровней | ||||||||||
| 9. | Количество электронов на внешнем энергетическом уровне | ||||||||||
| 10. | Схема строения атома | ||||||||||
| 11. | Количество протонов | ||||||||||
| 12. | Количество нейтронов | ||||||||||
| 13. | Количество электронов |
Пример выполнения задания
| Химический элемент | Zn | ||||||||||
| Период | |||||||||||
| Группа | |||||||||||
| Подгруппа | Побочная | ||||||||||
| Порядковый номер элемента | |||||||||||
| Атомная масса элемента | |||||||||||
| Формула высшего оксида | ZnO | ||||||||||
| Количество энергетических уровней | |||||||||||
| Количество электронов на внешнем энергетическом уровне | |||||||||||
| Схема строения атома | 
  2 8 18 2 | ||||||||||
| Количество протонов | |||||||||||
| Количество нейтронов | 65-30=35 | ||||||||||
| Количество электронов |
Контрольные вопросы:
1. Чему равно количество энергетических уровней химического элемента?
2. Как определить число нейтронов в ядре атома?
3. Чему равно количество электронов на внешнем энергетическом уровне атома?
Форма контроля:
Письменный отчёт, с устной защитой.
ЛАБОРАТОРНАЯ РАБОТА № 1
Часа
Тема «Ознакомление со свойствами дисперсных систем»
Цель: систематизация знаний о дисперсных системах, приготовление и исследование свойств суспензий, эмульсий, пен
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: мерный цилиндр, мерная ложечка, стаканы 200мл., водный раствор СаСО3, моторное масло, стиральный порошок, вода.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
ПРАКТИЧЕСКАЯ РАБОТА № 2
Часа
Тема «Приготовление раствора заданной концентрации»
Цель: обобщение и систематизация знаний по теме «Вода. Растворы. Электролитическая диссоциация»
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Задание:пользуясь учебными пособиями и примерами выполнения заданий, проведите вычисления, запишите ответ. Сделайте выводы.
| № варианта | Вычислите массовую долю соли в полученном растворе | Рассчитайте массу соли и воды |
| m(H2O)= 400г m(соли)= 20г | m(раствора)= 800г W(соли) = 10% | |
| m(H2O)= 800г m(соли)= 30г | m(раствора)= 900г W(соли) = 20% | |
| m(H2O)= 240г m(соли)= 40г | m(раствора)= 400г W(соли) = 5% | |
| m(H2O)= 340г m(соли)= 50г | m(раствора)= 600г W(соли) = 15% | |
| m(H2O)= 280г m(соли)= 60г | m(раствора)= 700г W(соли) = 20% | |
| m(H2O)= 920г m(соли)= 70г | m(раствора)= 800г W(соли) = 12% | |
| m(H2O)= 460г m(соли)= 80г | m(раствора)= 900г W(соли) = 18% | |
| m(H2O)= 480г m(соли)= 60г | m(раствора)= 920г W(соли) = 30% | |
| m(H2O)= 520г m(соли)= 70г | m(раствора)= 420г W(соли) = 40% | |
| m(H2O)= 540г m(соли)= 80г | m(раствора)= 350г W(соли) = 50% |
Пример выполнения заданий
Задача №1
В 200г воды растворили 50г хлорида натрия. Вычислите массовую долю NaCl в полученном растворе.
| Дано: m(H2O)= 200г m(NaCl) = 50г Найти: W(NaCl) - ? | Решение: m( в-ва ) Х 100% ; W= m( р-ра ) m(р-ра) = m(H2O) + m(NaCl) = 200г + 50г = 250 (г) W(NaCl)= m(NaCl)/m(р-ра) · 100% = 50/250 · 100% = 20 (%) Ответ: W(NaCl)= 20% |
Задача №2
Сколько граммов воды и хлорида калия потребуется для приготовления 500г раствора с массовой долей хлорида калия 14%?
| Дано: m(р-ра)= 500г W(KCl) = 14% Найти: m (H2O) -? m (KCl) - ? | Решение: m( в-ва ) Х 100% ; W= m( р-ра ) m(в-ва) = W х m( р-ра ) / 100%; m(KCl) = 14%*500г./100% = 70 (г) m(H2O) = m(раствора) - m(KCl) = 500 – 70 =430 (г) Ответ: m(H2O)= 430г; m(KCl)= 70г. |
Контрольные вопросы:
1Что такое растворы?
2Чем гидраты отличаются от сольватов?
3Что такое растворимость?
4Что такое электролиты и неэлектролиты? Приведите примеры.
5Как называется отношение массы растворенного вещества к общей массе раствора?
Форма контроля:
Письменный отчёт, с устной защитой.
ЛАБОРАТОРНАЯ РАБОТА № 2
Часа
Тема «Изучение свойств кислот»
Цель: систематизация знаний о химических свойствах кислот.
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; таблица растворимости; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, универсальная лакмусовая бумага, водные растворы кислот, NaОН, CuSO4, хлорида бария, мерная ложечка, гранулы цинка и меди, оксид меди, раствор фенолфталеина.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Краткие теоретические сведения.
Кислоты – это сложные вещества, состоящие из ионов водорода
и кислотных остатков.
Общая формула кислот: 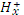
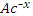 ,
,
где Ac – кислотный остаток.
Например: хлороводородная кислота HCl
серная кислота H2SO4
фосфорная кислота Н3РО4.
Кислоты могут быть твердыми (Н3РО4 , H2SiO3) и жидкими (HCl, H2SO4) , сильными (HCl, H2SO4, HNO3) и слабыми (H2SiO3 , Н2 СО3, H2S ), летучими (Н2СО3 , H2 SO3 ) и нелетучими (H2SiO3 , H2SO4).
Химические свойства кислот
1. В водных растворах кислоты диссоциируют на ионы водорода и ионы кислотного остатка.
HNO3 = Н+ + NO3- Свободные ионы водорода способны изменять окраску индикаторов. Лакмус и метиловый оранжевый окрашиваются в красный цвет.
2. При взаимодействии растворов кислот с металлами, образуется соль и газ водород.
2HCL + Zn = ZnCL2 + H2
· Данная реакция не идет с металлами, стоящими в ряду напряжений после водорода.
3. При взаимодействии растворов кислот с оксидами металлов, образуется соль и вода.
2HCL + СиО = СиCL2 + H2O
4. При взаимодействии растворов кислот с основаниями, образуется соль и вода.
HCL + KОН = KCL + H2O
5. При взаимодействии растворов кислот с солями, образуется новая соль и новая кислота.
HCL + AgNO3 = AgCL + HNO3
ЛАБОРАТОРНАЯ РАБОТА № 3
Часа
Тема «Изучение свойств солей. Гидролиз солей различного типа»
Цель: систематизация знаний о химических свойствах солей.
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; таблица растворимости; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, универсальная лакмусовая бумага, водные растворы кислот, NaОН, CuSO4, хлорида бария, мерная ложечка, гранулы цинка и меди, оксид меди, раствор фенолфталеина.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Краткие теоретические сведения.
Соли – это сложные вещества, состоящие из ионов металла и
кислотных остатков.
Например: хлорид калия КCl
сульфат кальция СаSO4
фосфат натрия Nа3РО4.
Все соли являются твердыми кристаллическими веществами разного цвета и по растворимости подразделяются на 3 группы: растворимые, малорастворимые и практически нерастворимые в воде (смотри таблицу растворимости).
В водных растворах соли подвергаются гидролизу.
Гидролиз соли–это реакция обмена ионов соли с ионами воды.
Гидролизу подвергаются соли образованные
- катионом сильного основания и анионом слабой кислоты
КNO2 + HOH ↔ КОН + НNО2 (молекулярное уравнение)
К+ + NO2 - + НОН ↔К++ ОН- + НNО2 (полное ионное уравнение)
NO2 - + HOH ↔ ОН- + НNО2 (сокращенное ионное уравнение)
В растворе накапливаются ионы ОН- - среда щелочная.
- катионом слабого основания и анионом сильной кислоты
СuSO4 + 2HOH ↔ Cu(OH)2 + H2SO4 (молекулярное уравнение)
Сu2+ + SO42- + 2НОН ↔ Cu(OH)2 + 2Н++ SO42- (полное ионное
уравнение)
Сu2+ +2НОН ↔ Cu(OH)2 + 2Н+ (сокращенное ионное уравнение)
В растворе накапливаются ионы Н+ - среда кислая.
- катионом слабого основания и анионом слабой кислоты
NH4NO2 + HOH ↔ NH4OH + НNО2 (молекулярное уравнение)
NH4 + + NO2 - + НОН ↔ NH4OH + НNО2 (полное ионное уравнение)
В растворе нет свободных ионов – среда нейтральная.
Химические свойства соли
1. При взаимодействии раствора соли с металлами, образуется новая соль и новый металл.
CuCL2 + Zn = ZnCL2 + Сu
· Данная реакция не идет, если металл в соли активнее свободного металла.
2. При взаимодействии растворов солей друг с другом, образуется две новые соли.
КCL + AgNO3 = AgCL + КNO3
Опыт №3 Гидролиз соли
Ход работы:
Пользуясь таблицей растворимости, учебником и краткой теорией, проведите гидролиз предложенных солей. Определите, какая среда образуется в растворе. Уравнения реакций запишите в таблицу.
| № варианта | ||||||||||
| Формулы солей | Al(NO3)3 | NH4CL | K2CO3 | ВаS | NaNO2 | Fe2(CO3)3 | Na2S | FeCL2 | KNO2 | CrCl3 |
| Номер опыта и ход работы | Наблюдения | Уравнения химических реакций |
Контрольные вопросы:
1. Что такое соли? Приведите примеры.
2. Почему сульфат меди с цинком реагирует, а с медью не реагирует?
3. Назовите по 2 растворимых, малорастворимых и практически нерастворимых солей.
4. Что такое гидролиз?
5. Что такое кислоты? Приведите примеры.
6. Что такое основания? Приведите примеры.
Форма контроля:
Письменный отчёт, с устной защитой.
ЛАБОРАТОРНАЯ РАБОТА № 4
Часа
Тема «Типы химических реакций»
Цель: систематизировать знания о классификации химических реакций
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; таблица растворимости; электрохимический ряд напряжений металлов; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, водные растворы хлороводородной кислоты, хлорида алюминия, NaОН, СаСО3, CuSO4, гранулы железа.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Краткие теоретические сведения.
Опыт №3 Образование осадка.
Ход работы:
В пустую пробирку налейте 1 миллилитр раствора хлорида алюминия и осторожно, по каплям приливайте раствор гидроксида натрия до образования студенистого осадка. Что наблюдаете? Наблюдения и уравнение реакции запишите в таблицу.
| Номер опыта и ход работы | Наблюдения | Уравнения химических реакций |
Контрольные вопросы:
1. Что такое химическая реакция? Приведите примеры.
2. Какие признаки химических реакций вы знаете?
3. Перечислите признаки необратимости химических реакций.
4. Что такое экзотермическая реакция?
5. Какая реакция называется реакцией ионного обмена?
6. Перечислите типы химических реакций.
Форма контроля:
Письменный отчёт, с устной защитой.
ЛАБОРАТОРНАЯ РАБОТА № 5
Часа
Тема «Скорость химической реакции»
Цель: систематизация знаний по теме «Скорость химической реакции»
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; таблица растворимости; электрохимический ряд напряжений металлов; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, водные растворы серной и соляной кислот, гранулы цинка, железа, оксид меди.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
ЛАБОРАТОРНАЯ РАБОТА № 6
Часа
Тема «Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа»
Цель: систематизация знаний по теме «Металлы и неметаллы»
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: спиртовка, спички, держатель, плоскогубцы, пинцет, стакан с холодной водой, стальные иголки, образцы чугуна и руд железа.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
ЛАБОРАТОРНАЯ работа №7
Часа
Тема «Получение, собирание и распознавание газов. Решение экспериментальных задач»
Цель: Выработать умение получать, собирать и распознавать кислород и водород
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, пробки с газоотводными трубками, спиртовка, спички, лучина, перманганат калия, серная кислота, гранулы цинка.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Опыт №1 Получение кислорода
Ход работы:
Насыпьте в пробирку на 1/4 ее объема перманганат калия и закройте ее пробкой с газоотводной трубкой. Прогрейте всю пробирку в пламени спиртовки, затем нагревайте дно пробирки. Газоотводную трубку поместите в чистую пробирку. Полноту заполнения сосуда кислородом проверяйте тлеющей лучиной. Свои наблюдения и уравнение реакции запишите в таблицу.
Опыт №2 Получение водорода
Ход работы:
Поместите в пробирку несколько гранул цинка и прилейте 2 мл серной кислоты. Закройте пробирку пробкой с газоотводной трубкой, трубку поместите в чистую пробирку. Наличие водорода проверяйте поднесением к отверстию сосуда горящей спички. Свои наблюдения и уравнение реакции запишите в таблицу.
| Номер и название опыта, ход работы | Наблюдения |
Контрольные вопросы:
1. Как доказать наличие кислорода в пробирке?
2. Как располагать пробирку для сбора водорода - вверх дном или вниз дном? Почему?
3. Как доказать наличие водорода?
Форма контроля:
Письменный отчёт, с устной защитой.
ЛАБОРАТОРНАЯ РАБОТА № 8
Часа
Тема «Изготовление моделей молекул органических веществ»
Цель: систематизация знаний по теме «Основные понятия органической химии и теория строения органических веществ»
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: спички, пластилин.
Задание:сделайте из пластилина небольшие шарики 3 цветов, составьте молекулы предложенных химических веществ, результаты работы оформите в таблицу, сделайте выводы.
ЛАБОРАТОРНАЯ РАБОТА № 9
Часа
Тема «Ознакомление с коллекцией образцов нефти и продуктов ее переработки. Ознакомление с коллекцией каучуков и образцами изделий из резины»
Цель: систематизация знаний по теме «Углеводороды и их природные источники»
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: образцы нефти, нефтепродуктов, каучука.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
ЛАБОРАТОРНАЯ РАБОТА № 10
Часа
Тема «Изучение свойств кислородосодержащих органических веществ»
Цель: систематизация знаний о свойствах спиртов, карбоновых кислот, сложных эфиров и углеводах
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, водные растворы уксусной кислоты, перманганата калия, глюкозы, сахарозы, NaОН, CuSO4, гранулы цинка, глицерин, СаСО3, вода, раствор фенолфталеина, растительное масло, крахмальный клейстер, раствор йода.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
ЛАБОРАТОРНАЯ РАБОТА № 11
Тема«Изучение свойств белка»
Цель: изучение химических свойств и биологических функций белков
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, водные растворы ацетата свинца, аммиака, белка куриного яйца, NaОН, CuSO4, концентрированная азотная кислота.
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Краткие теоретические сведения.
1. Денатурация. При нагревании, под действием сильных кислот
или оснований, солей тяжелых металлов и некоторых других реагентов происходит необратимое осаждение (свертывание) белков, называемое денатурацией. При денатурации происходят изменения во вторичной и третичной структуре белка, а первичная структура сохраняется. При этом их биологические функции полностью уничтожаются.
2. Гидролиз. Под действием ферментов, а также водных растворов
кислот или щелочей происходит разрушение первичной структуры белка в результате разрыва пептидных связей. Гидролиз приводит к образованию пептидов и аминокислот. Гидролиз – основа процесса пищеварения.
3. Биуретовая реакция. При действии на белки раствора солей меди
(II) в щелочной среде возникает сиреневое или фиолетовое окрашивание. Голубая окраска раствора соли меди изменяется на фиолетовую (или несколько иную в зависимости от природы белка) за счет образования комплексных соединений.
4. Ксантопротеиновая реакция. При действии на белки
концентрированной азотной кислоты образуется желтая окраска, связанная нитрованием ароматических колец в соответствующих аминокислотах.
5. Качественное определение серы в белках. При горении белки
издают характерный запах «жженого рога». В значительной степени этот запах определяется содержанием в белках атома серы (цистеин, метионин, цистин).
Опыт № 1 Денатурация белка
Приготовьте раствор белка. Для этого белок куриного яйца растворите в 150 мл воды. В пробирку налейте 4-5 мл раствора белка и нагрейте на спиртовке до кипения. Отметьте помутнение раствора. Охладите содержимое пробирки. Разбавьте водой в 2 раза. Результаты наблюдений запишите в таблицу.
ЛАБОРАТОРНАЯ РАБОТА № 12
Часа
Тема: «Решение экспериментальных задач на идентификацию органических соединений. Распознавание пластмасс и волокон»
Цель: обобщить и систематизировать знания по теме «Органические вещества», выработать умение распознавать органические соединения
Учебные пособия: МУ по выполнению практических и лабораторных работ; периодическая таблица химических элементов Д.И. Менделеева; Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2003.; раздаточный материал
Оборудование и реактивы: штатив с пробирками, спиртовка, спички, игла, пинцет, этановая кислота, универсальная лакмусовая бумага, водные растворы NaОН, CuSO4, глюкозы, сахарозы, аммиачный раствор оксида серебра, этиловый спирт, глицерин, образцы различных пластмасс и волокон
Задание:проведите химические опыты, результаты работы оформите в таблицу, сделайте выводы.
Краткие теоретические сведения
Среди изобилия самых разнообразных по строению и свойствам органических соединений есть особый класс – полимеры или высокомолекулярные вещества (ВМС). По своему происхождению полимеры подразделяются на природные (каучук, крахмал, целлюлоза, белки) и синтетически (синтетический каучук, различные пластмассы и волокна). ВМС играют важную роль в биологических процессах и практической деятельности человека. При нагревании многие синтетические полимеры не плавятся, а лишь размягчаются, что позволяет формировать из них различные изделия. Такие полимеры называются пластмассами. Для производства химического волокна используют различные виды полимерных смол (полиэфирные, полиамидные и др.). Смолу плавят и пропускают через фильеры. Струи полимера охлаждаются потоком холодного воздуха и превращаются в волоконца, при скручивании которых образуются нити. Полимеры и получаемые на их основе пластмассы и волокна постепенно вытесняют природные материалы. Они широко используются в новейших областях техники – атомной энергетике, электронике, ракетной технике и самолетостроении. Наконец, они прочно вошли в наш быт. Посуда, отделочные и упаковочные материалы, лаки и краски, синтетические ткани и одежда из них, игрушки, спортивный инвентарь – вот далеко не полный перечень изделий из полимеров.
Физические свойства некоторых полимеров:
Полиэтилен – полупрозрачный, эластичный, жирный на ощупь материал. При нагревании размягчается, из расплава можно вытянуть нити. Горит синеватым пламенем, распространяя запах расплавленного парафина, продолжает гореть вне пламени.
Поливинилхлорид – эластичный или жесткий материал, при нагревании быстро размягчается. Горит коптящим пламенем, распространяя острый запах, вне пламени не горит.
Полистирол – прозрачный или непрозрачный материал, часто хрупок. При нагревании размягчается, из расплава легко вытянуть нить. Горит коптящим пламенем, распространяя запах стирола, продолжает гореть вне пламени.
Полиметилметакрилат – обычно прозрачен, но может иметь различную окраску. При нагревании размягчается, нити не вытягиваются. Горит желтоватым пламенем с синей каймой и характерным потрескиванием, распространяя эфирный запах.
Фенолформальдегидная пластмасса – твердое хрупкое вещество темного цвета (от коричневого до черного) с блестящей поверхностью. При нагревании разлагается, распространяя запах фенола. Загорается с трудом, вне пламени постепенно гаснет.
Хлопок – горит быстро, распространяя запах жженой бумаги, после сгорания остается серый пепел.
Шерсть, натуральный шелк – горит медленно, с запахом жженых перьев, после сгорания образуется черный шарик, при растирании превращающийся в порошок.
Ацетатное волокно – горит быстро, образуя нехрупкий, спекшийся шарик темно-бурого цвета. В отличие от других волокон растворяется в ацетоне.
Капрон – эластичный материал при нагревании размягчается, затем плавится, из расплава можно вытянуть нить. Горит желто-синем пламенем, распространяя неприятный запах.
Лавсан – при нагревании плавится, из расплава можно вытянуть нить. Горит коптящим пламенем с образованием темного блестящего шарика.
СПИСОК ЛитературЫ
1. Габриелян, О. С. Практикум по общей, неорганической и органической химии [Текст] : учеб. пособие для студ. сред. проф. учеб. заведений / О. С. Габриелян, И. Г. Остроумов, Н. М. Дорофеева. – М., 2011. – 255с.
2. Габриелян, О. С. Настольная книга учителя химии: 10 класс [Текст] / О. С. Габриелян, И. Г. Остроумов. – М., 2004. – 480с.
3. Габриелян, О. С. Настольная книга учителя химии: 11 класс: в 2 ч. [Текст] / О. С. Габриелян, Г. Г. Лысова, А. Г. Введенская. – М., 2004. – 320с.
4. Ерохин, Ю. М. Химия [Текст] : учебник / Ю. М. Ерохин. – М., 2007. - 384с.
ХИМИЯ
Методические указания
по выполнению лабораторных и практических работ
для всех специальностей
I курса на базе основного общего образования
технический профиль
Белово 2015
Составлены в соответствии с требованиями к предъявляемыми к минимуму содержания и уровню подготовки студентов I курса всех специальностей технического профиля и рабочей программой утвержденной методическим советом техникума
Протокол №_____ «___» ________ 20___г.
| Одобрено ПЦК социально-экономических дисциплин и базисной подготовки Протокол №_____ от «____»_____________20__г от «____»_____________20__г Председатель ПЦК ____________М.И.Сюбаева ____________М.И.Сюбаева | Утверждено Методическим советом ГОУ СПО «Беловский политехнический техникум» Протокол №____ от «___» ____________ 20__г. от «___» ____________ 20__г. Зам. директора по НМР ____________Т.П. Салтымакова ____________Т.П. Салтымакова |

Составитель
Преподаватель общеобразовательных
дисциплин Н.Б. Таюшова
Рецензент
Преподаватель спецдисциплин З.С. Калачук
Внешний рецензент
Нач. отдела по НР
БФ ГБОУ ВПО «КузГТУ»