Металлическая связь. Металлические кристаллы
В металлах валентные электроны удерживаются атомами крайне слабо и способны мигрировать. Атомы, оставшиеся без внешних электронов, приобретают положительный заряд. Они образуют металлическую кристаллическую решётку.
Совокупность обобществлённых валентных электронов (электронный газ), заряженных отрицательно, удерживает положительные ионы металла в определённых точках пространства - узлах кристаллической решётки, например, металла серебро.
Внешние электроны могут свободно и хаотично перемещаться, поэтому металлы характеризуются высокойэлектропроводностью (особенно золото, серебро, медь, алюминий).
12.Метод валентных связей. Обменный и донорно-акцепторный механизм образования связи. Гипотеза гибридизации орбиталей, ее применимость и геометрическое строение молекул.
В основу метода МВС положено допущение, что координационный ион (соединение) образуется по донорно-акцепторному механизму за счет неподеленных электронных пар лигандов (доноров) и свободных гибридных орбиталей иона комплексообразователя (акцептора).
Образование парамагнитного иона [FeF6]4– можно представить таким образом. Свободный ион Fe2+ имеет электронную конфигурацию d6 и следующее распределение электронов по орбиталям:
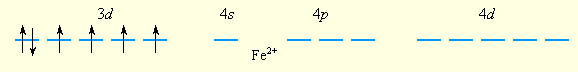
Шесть ионов F– смещают по одной из своих неподеленных электронных пар на вакантные sp3d2-гибридные орбитали иона Fe2+. Четыре неспаренных электрона иона Fe2+сохраняются и обусловливают высокий спин иона [FeF6]4–:
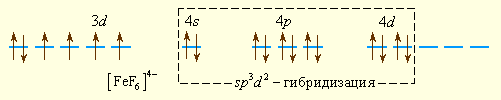
Так как число неспаренных электронов в комплексе и свободном ионе Fe2+ совпадает, то комплекс [FeF6]4– называется высокоспиновым.
Ионы CN– значительно сильнее взаимодействуют с ионом железа (II), следствием чего является спаривание d-электронов центрального иона и образование низкоспинового комплекса [Fe(CN)6]4– с d2sp3-гибридизацией.
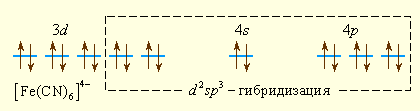
Аналогично можно представить образование и других комплексных ионов:
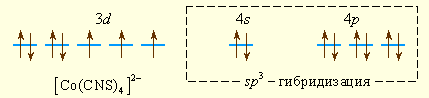
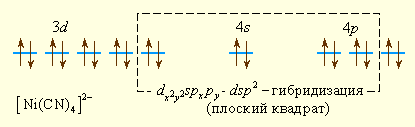
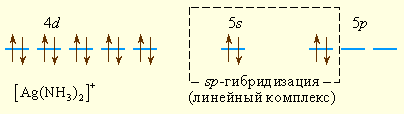
Комплексообразователем может быть не только положительный ион металла, но и металл в нулевой степени окисления, например, в карбонилах металлов – соединениях с
общей формулой [M(CO)n]. Связь в таких соединениях можно объяснить с позиций МВС в рамках правила 18 электронов: устойчивы такие карбонилы, в которых все d- , s- иp-орбитали металла заполнены электронными парами.
Насыщаемость и направленность связей. Полярность и поляризуемость связей. Типы связей, типы кристаллических решеток. Силы Ван-дер-Ваальса. Влияние характера связей на физико-химические свойства веществ.
Насыщаемость ковалентной связи обусловлена ограниченными валентными возможностями атомов, т.е. их способностью к образованию строго определенного числа связей, которое обычно лежит в пределах от 1 до 6. Общее число валентных орбиталей в атоме, т.е. тех, которые могут быть использованы для образования химических связей, определяет максимально возможную валентность элемента. Число уже использованных для этого орбиталей определяет валентность элемента в данном соединении.
Направленность ковалентной связи является результатом стремления атомов к образованию наиболее прочной связи за счет возможно большей электронной плотности между ядрами. Это достигается при такой пространственной направленности перекрывания
электронных облаков, которая совпадает с их собственной. Исключение составляют s-электронные облака, поскольку их сферическая форма делает все направления равноценными. Для p- и d-электронных облаков перекрывание осуществляется вдоль оси, по которой они вытянуты, а образующаяся при этом связь называется s-связью. s-Связь имеет осевую симметрию, и оба атома могут вращаться вдоль линии связи, т.е. той воображаемой линии, которая проходит через ядра химически связанных атомов.
Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов. По этому признаку ковалентные связи подразделяются на неполярные и полярные.
Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов. Полярность и поляризуемость ковалентных связей определяет реакционную способность молекул по отношению к полярным реагентам.
Кристалли́ческая решётка
Ионные, атомные, молекулярные, металлические.
Ван-дер-ваальсовы силы — силы межмолекулярного взаимодействия с энергией 0,8 — 8,16 кДж/моль Этим термином первоначально обозначались все такие силы, но сейчас он обычно применяется к силам, возникающим при поляризации молекул и образовании диполей. Открыты Я. Д. ван дер Ваальсом в 1869 году.
*К ван-дер-ваальсовым силам относятся взаимодействия между диполями (постоянными и индуцированными). Название связано с тем фактом, что эти силы являются причиной поправки на внутреннее давление в уравнении состояния реального газа Ван-дер-Ваальса. Эти взаимодействия в основном определяют силы, ответственные за формирование пространственной структуры биологических макромолекул.
14. Закономерности изменения свойств атомов в периодах и группах периодической системы Д. И. Менделеева. Периодичность свойств элементов (размер атомов, энергия ионизации, сродство к электрону).
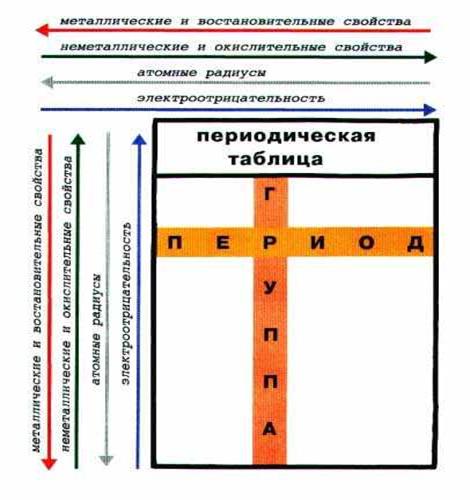
15. Химическая термодинамика. Основные понятия и определения. Система, термодинамические процессы, переменные и функции.
Хими́ческая термодина́мика — раздел физической химии, изучающий процессы взаимодействия веществ методами термодинамики.
Основными направлениями химической термодинамики являются:
1. Классическая химическая термодинамика, изучающая термодинамическое равновесие вообще.
2. Термохимия, изучающая тепловые эффекты, сопровождающие химические реакции.
3. Теория растворов, моделирующую термодинамические свойства вещества исходя из представлений о молекулярном строении и данных о межмолекулярном взаимодействии.
Химическая термодинамика тесно соприкасается с такими разделами химии, как: аналитическая химия; электрохимия; коллоидная химия; адсорбция и хроматография.
