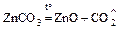V1. Силы Ван-дер-Ваальса (Межмолекулярные взаимодействия)
Это взаимодействия молекул между собой, не приводящие к разрыву или образованию новых химических связей. Основу составляют кулоновские силы взаимодействия между электронами и ядрами одной молекулы и ядрами и электронами другой молекулы; силы действуют между всеми молекулами, находящимися на близком расстоянии одна от другой. Особенно характерны для газов.
Межмолекулярное взаимодействие усиливается при увеличении внешнего давления и уменьшении температуры. Эти силы очень слабые, поэтому какая-либо молекула случайно может оказаться достаточно возбужденной, чтобы оторваться от соседних и вылететь в окружающее пространство. Так, например, даже твердые вещества могут испаряться.
Метод молекулярных орбиталей (МО)
Развили этот метод Р. Малликен и Ф. Гунд, он дополняет и углубляет метод валентных связей. Квантово-механические закономерности, установленные для атомов, распространяются на молекулу:
1.При образовании молекул имеет место не механическое перекрывание орбиталей, а валентные электроны с атомных орбиталей(АО) переходят на молекулярные орбитали (МО), новые по энергии и форме.
2.Из двух исходных атомных получают две молекулярные орбитали, одна из которых энергетически более выгодна и называется “связывающей”, а другая не выгодна по сравнению с атомной и называется “разрыхляющей”.
3.Устойчивость молекулы оценивается по величине порядка связи (ПС):
ПС = 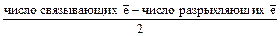
Если ПС =1(и больше), то молекула устойчива
ПС = 0,5 – молекула неустойчива
ПС = 0 - молекулы не существует
4.Для молекул, образованных неметаллами, значение рассчитанной величины ПС совпадает с величиной кратности связи, определенной по методу валентных связей. Однако метод МО позволяет доказать существование молекул Li2 , C2, заряженных частиц 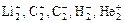 и др.
и др.
5.Метод объясняет наличие магнитных свойств у многих молекул (например жидкий кислород – парамагнетик):
а)если на всех молекулярных орбиталях находятся только спаренные электроны, то вещество – диамагнетик;
б)если на молекулярных орбиталях имеется хотя бы один неспаренный электрон (неважно, на связывающих или разрыхляющих) – то вещество парамагнетик.
Вопросы для закрепления материала:
1.Какой тип связей существует в молекулах HNO3? KNO2?
2.Какая из указанных молекул имеет наиболее ковалентный характер связи – а)LiCI? б) NaH? в) KCI?
ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
ОКСИДЫ – соединения, состоящие из двух элементов, один из которых кислород.
Делятся на солеобразующие: основные(о.оксиды) - К2О, CaO; кислотные (к.оксиды) - CO2, SО3; амфотерные (ZnO, MnO2);
несолеобразующие: просто оксиды(CO, NO) и пероксиды (H2O2, BaO2, CrO5).
Основные оксидыобразованы металлами:
1.щелочными или щелочно-земельными металлами (Li, Na, К, Rb, Cs, Fr, Ca, Sr, Ba);
2.элементами побочных подгрупп в минимальной степени окисления (FeO, CrO, MnO).
Физические свойства
Твёрдые, порошкообразные, на воздухе хранятся плохо, т.к. реагируют с водой.
Химические свойства
1. Оксид + вода = щёлочь
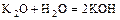
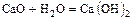
2. о. оксид + кислота = соль + вода
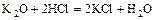
3. о. оксид + к. оксид = соль
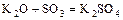
4. о. оксид + более активный металл = оксид + новый металл
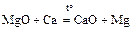 (см. ряд напряжений).
(см. ряд напряжений).
Получение
- металл + кислород = о. оксид
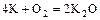 .
.
- прокаливание некоторых солей
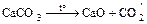 .
.
3. металлотермия
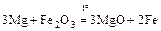 .
.
- прокаливанием соответствующих оснований получить такие оксиды практически невозможно.
Кислотные оксиды
(ангидриды кислот)
- Образованы неметаллами
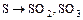 ;
; 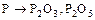 ;
; 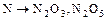 ;
; 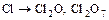 ;
;
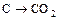 ;
; 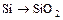 ;
; 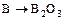 .
.
- Образованы элементами побочных подгрупп (d - элементами) в максимальной степени окисления (FeO3, CrO3, Mn2O7).
Физические свойства
В отличие от основных оксидов могут быть в разных агрегатных состояниях: газообразные, жидкие, твердые.
Химические свойства
1. к. оксид + вода = кислота; реакции идут по-разному:
а) некоторые оксиды очень активно взаимодействуют с водой, образуя устойчивые кислоты (поэтому их можно использовать как осушители)
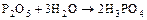 ,
,
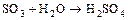 ,
,
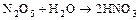 .
.
б) другие образуют неустойчивые кислоты
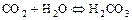
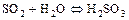
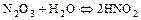
в)имеются оксиды, которые соответствуют кислотам, но с водой не реагируют
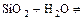 .
.
2. к. оксид + основание = соль + вода
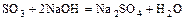 .
.
3. к. оксид + о. оксид = соль
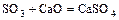 .
.
Получение
- Окисление соответствующего элемента
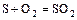 .
.
- Окисление других оксидов
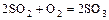 .
.
- Разложение некоторых солей
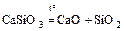 .
.
- Разложение некоторых кислот (неустойчивых)
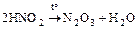 ,
,
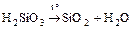 .
.
Амфотерные оксиды
1. образованы металлами с постоянной степенью окисления (BeO, ZnO, Al2O3).
2. если d–элемент проявляет различные степени окисления, то в амфотерных оксидах она промежуточная (Cr2O3, MnO2).
Химические свойства
- амф. оксид + вода ¹
- с сильными кислотами образуют соли
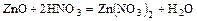 .
.
(как о. оксид)
- со щелочами образуют соли
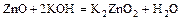 .
.
(как к. оксид)
- с кислотными и основными оксидами тоже образуют соли
а) 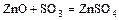 .
.
б) 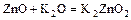
- металлотермия
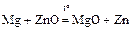
Получение
- окисление металлов
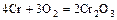 .
.
- разложение соответствующих оснований
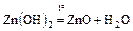 ,
,
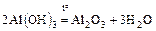 ,
,
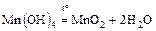 .
.
- прокаливание соответствующих карбонатов, силикатов, сульфитов