Условные обозначения и формулы для расчетов, применяемые в курсе медицинской химии
| Обозначение | Формулы для расчетов | Единицы измерения |
| m | Масса вещества (раствора) | мг, г, кг |
| M | Молярная масса вещества | г/моль |
| u | Количество вещества 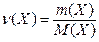 Для газов: Для газов: 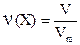 | моль |
| V | Объем раствора | мл, л, м3 |
| r | Плотность раствора m(р-ра) = V(р-ра) ∙ ρ | г/мл, г/см3, г/л, кг/м3 |
| w | Массовая доля вещества в растворе (процентная концентрация) 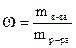 ; ; 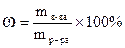 | доли ед., % |
| C | Молярная концентрация вещества в растворе (молярность) 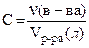 Формула пересчета: Формула пересчета: 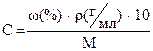 | моль/л или М, ммоль/л, моль/м3 |
| Cm | Моляльная концентрация (моляльность) 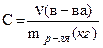 | моль/кг или m |
Сf, 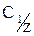 | Молярная концентрация эквивалента (нормальность) 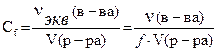 , , 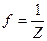 f- фактор эквивалентности Z - основность для кислот; кислотность для оснований; произведение степени окисления металла на его количество для солей. f- фактор эквивалентности Z - основность для кислот; кислотность для оснований; произведение степени окисления металла на его количество для солей. | моль/л или н |
| c | Мольная доля вещества 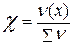 | - |
Основная лабораторная посуда(зарисовать):
Лабораторная работа: “Физико-химические методы исследования растворов.
Приготовление растворов”.
Ход работы:
Приготовить 1%, 2% и 4% растворы хлорида натрия массой 250 грамм, используя готовые навески. С помощью ареометра определить плотность приготовленного раствора и установить ω% по справочной таблице. С помощью рефрактометра определить коэффициент рефракции полученного раствора и установить ω% его раствора по таблице. Сравнить полученные результаты.
Таблица 1
Зависимость показателя преломления (n) и плотности раствора (r)
От концентрации натрия хлорида (при 20 С)
| Плотность, | Концентрация | Коэффициент рефракции | |
| г/мл | ω % | С | (n) |
| 1.00 | 1.333 | ||
| 1.007 | 0.17 | 1.335 | |
| 1.015 | 0.34 | 1.337 | |
| 1.022 | 0.51 | 1.338 | |
| 1.029 | 0.70 | 1.340 | |
| 1.036 | 0.85 | 1.342 | |
| 1.044 | 1.07 | 1.343 | |
| 1.051 | 1.26 | 1.345 | |
| 1.058 | 1.45 | 1.347 | |
| 1.066 | 1.64 | 1.348 | |
| 1.073 | 1.83 | 1.350 | |
| 1.080 | 2.03 | 1.352 |
Работа с рефрактометром.
Одну или две капли исследуемого раствора соли, помещают между призмами рефрактометра. В окно верхней призмы направляют источник света. Через нижнюю призму свет попадает на шкалу прибора, частично её освещая и создавая чёткую границу света снизу и тени сверху. Если граница светотени недостаточно чёткая, имеет радужные полоски, то вращением компенсатора добиваются их исчезновения. Поворотом рычага, на котором закреплён окуляр, добиваются совмещения трёх чёрточек с границей светотени и считывают по левой шкале коэффициент рефракции, по правой - процентное содержание вещества. Контроль работы производится по дистиллированной воде, коэффициент рефракции которой равен 1,333. Зная коэффициент рефракции раствора, по таблице находят его процентное содержание. Необходимо помнить, что таблица составляется только для определенного вещества.
Занятие № 2. Тема: «Основы химического анализа. Качественный и количественный анализ. Основы титриметрического анализа. Метод кислотно-основного титрования. Алкалиметрия».
Вопросы для обсуждения.
| 1. | Предмет и задачи аналитической химии. Качественный и количественный анализ. |
| 2. | Основные понятия качественного анализа: а) аналитические реакции; б) реагент (реактив) в) дробный и систематический метод анализа; г) макро-, микро-, полумикроанализ; д) способы выполнения аналитических реакций. |
| 3. | Методы количественного анализа. Классификация методов количественного анализа. |
| 4. | Закон эквивалентов. Основные понятия объемного (титриметрического) анализа: а) рабочий раствор (титрант); б) исходные вещества, требования к ним; в) анализируемый раствор; г) титрование; д) точка эквивалентности, точка нейтрализации; е) конец титрования. |
| 5. | Индикаторы, выбор индикатора. Понятие о кривых титрования, их анализе. |
| 6. | Метод нейтрализации. Основные реакции метода. Алкалиметрия и ацидиметрия. Техника выполнения метода алкалиметрии. |
| 7. | Значение методов качественного и количественного анализа в медицине и других областях практической деятельности (санитарно-гигиенической практике). |
2. Выполнить тестовые задания (письменно):
| В качественном анализе используют методы: | ||
| А | Хроматографический | |
| Б | Гравиметрический | |
| В | Нейтрализации | |
| Г | Титриметрический | |
| 2. | Какое количество вещества исследуют в микроанализе: | |
| А | 0,5-1,0 г | |
| Б | 0,05-0,5 г | |
| В | 0,001-0,01 г | |
| Г | 1,0-1,5 г | |
| Аналитические реакции между электролитами записывают: | ||
| А | Сильные и слабые электролиты в ионном виде | |
| Б | В ионном виде только слабые электролиты | |
| В | Слабые электролиты и малодиссоциированные вещества в молекулярном виде | |
| Г | Сильные и слабые электролиты в молекулярном виде | |
| 4. | При добавлении к анализируемому раствору раствора нитрата свинца (ΙΙ) образовался черный осадок. Присутствие каких ионов вероятно в растворе? | |
| А | I- | |
| Б | Cl- | |
| В | S2- | |
| Г | SO42- | |
| 5. | Какой реактив может быть использован для определения в растворе карбонат-ионов? | |
| А | NaCl | |
| Б | CaCO3 | |
| В | NaOH | |
| Г | CaCl2 | |
| 6. | Какой реактив может быть использован для определения в растворе ионов Fe2+? | |
| А | NaCl | |
| Б | CaCO3 | |
| В | NaOH | |
| Г | CaCl2 | |
| 7. | Как изменится окраска индикатора фенолфталеина в щелочной среде? | |
| А | С бесцветной на желтую | |
| Б | С бесцветной на малиновую | |
| В | С бесцветной на красную | |
| Г | С бесцветной на фиолетовую | |
| 8. | Какую окраску приобретает индикатор лакмус в кислой среде? | |
| А | Бесцветная | |
| Б | Синяя | |
| В | Красная | |
| Г | Желтая | |
| 9. | Ионы К+ окрашивают пламя горелки в: | |
| А | Красный цвет | |
| Б | Фиолетовый цвет | |
| В | Зеленый цвет | |
| Г | Желтый цвет | |
| 10. | Какой раствор является рабочим раствором? | |
| А | Раствор с точно известной концентрацией | |
| Б | Раствор, концентрацию активного вещества которого надо установить | |
| В | Раствор, содержащий определенную массовую долю растворённого вещества | |
| Г | Раствор, не содержащий активного вещества | |
| 11. | Какой закон используют для расчётов в объёмном анализе? | |
| А | Закон Авогадро | |
| Б | Закон эквивалентов | |
| В | Закон постоянства состава | |
| Г | Закон перехода количества в качество | |
| 12. | Какая реакция лежит в основе метода кислотно-основного титрования: | |
| А | Окислительно-восстановительная реакция | |
| Б | Образование комплексного соединения | |
| В | Образование газа | |
| Г | Реакция нейтрализации | |
| Какие вещества используются в методе нейтрализации в качестве исходных? | ||
| А | NaOH и HCl | |
| Б | Na2CO3 и HCl | |
| В | NH3 и H2O | |
| Г | BaCl2 и H2SO4 | |
| Алкалиметрия – это метод определения содержания: | ||
| А | Оснований в растворах титрованием стандартным раствором кислоты | |
| Б | Многоосновных кислот в растворе титрованием раствора гидроксидом натрия | |
| В | Кислот в растворе титрованием стандартным раствором основания | |
| Г | Гидросульфатов в растворе титрованием стандартным раствором гидроксида натрия | |
| Момент титрования, в котором окраска раствора резко изменяется, называется: | ||
| А | Эквивалентная точка | |
| Б | Конечная точка титрования | |
| В | Кривая титрования | |
| Г | Точка нейтрализации | |
| Чему равна эквивалентная масса гидроксида калия? | ||
| А | 28 г/моль | |
| Б | 56 г/моль | |
| В | 5,6 г/моль | |
| Г | 14 г/моль | |
| Резкое изменение рН на кривой титрования в методе нейтрализации наблюдается вблизи точки эквивалентности. Этот участок называется: | ||
| А | Конец титрования | |
| Б | Скачок титрования | |
| В | Интервал перехода индикатора | |
| Г | Нет специального названия |
3. Ситуационные задачи:
| № | Текст задания: |
| 1. | Написать уравнения качественных реакций на ионы меди и хлора в растворе CuCl2 и определить признаки их прохождения. |
| 2. | Рассчитать молярную концентрацию эквивалента соляной кислоты, если на титрование 10 мл HCl израсходовано 13,6 мл 0,0485 н раствора NaOH. |
| 3. | Для титрования 10 мл анализируемого раствора гидроксида калия методом ацидиметрии израсходовано 16 мл раствора серной кислоты, с молярной концентрацией эквивалента 0,05 н. Рассчитать молярную концентрацию эквивалента гидроксида калия . |
| № | Эталоны ответов: |
| 1. | Качественная реакция на ион Cu2+: CuCl2 + 2NaOH → Cu(OH)2¯ + 2NaCl (молекулярное уравнение) голубой Cu2+ + 2Cl- + 2Na+ + 2OH- → Cu(OH)2¯ + 2Na+ + 2Cl- ( полное ионное уравнение) Cu2+ + 2OH- → Cu(OH)2¯ (сокращенное ионное уравнение) Качественная реакция на ион Cl-: CuCl2 + 2AgNO3 → 2AgCl¯ + Cu(NO3)2 (молекулярное уравнение) белый Cu2+ + 2Cl- + 2Ag+ + 2NO3- → 2AgCl¯ + Cu2+ + 2NO3- (полное ионное уравнение) Cl- + Ag+ → AgCl¯ сокращенное ионное уравнение) |
| 2. | 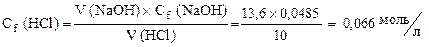 |
| 3. | 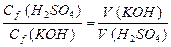 Þ Þ 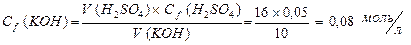  |
3. Задачи для самостоятельного решения (выполнить письменно):
1. Написать уравнения качественных реакций на ион аммония и сульфат ион в растворе (NH4)2SO4 и определить признаки их прохождения.
2. Рассчитать навеску карбоната натрия для приготовления 500 мл раствора с молярной концентрацией эквивалента 0,1 моль/л.
3. На титрование 20 мл анализируемого раствора уксусной кислоты методом алкалиметрии израсходовано 25 мл раствора гидроксида натрия, с молярной концентрацией эквивалента 0,1 моль/л. Рассчитать молярную концентрацию эквивалента уксусной кислоты в растворе.
4. Тематика рефератов по учебно-исследовательской работе студентов (УИРС).
| 1. | Использование качественных методов анализа в практической деятельности человека, в медицине. |
| 2. | Аналитические методы анализа в фармации. |
| 3. | Применение методов кислотно-основного титрования в медико-биологических и санитарно-гигиенических исследованиях. |
5. Вспомогательные материалы по самоподготовке:
Аналитическая химия – наука о методах и приемах определения качественного и количественного химического состава веществ или их смесей
Качественный анализ- это определение (открытие) химических элементов, ионов, атомов, атомных групп, молекул в анализируемом веществе. Исследование химического вещества всегда начинается с качественного анализа.
Качественный анализ
| Систематический (разделение смеси ионов на аналитические группы катионов и анионов) | Дробный (открытие каждого иона без предварительного разделения на ионы) |
Методы:
1. Химические (образование окрашенных продуктов реакции, выделения газа).
2. Хроматография.
3. Окрашивание пламени
Количественный анализ – это определение количественного состава вещества т.е. установление количества химических элементов, ионов, атомов, атомных групп. молекул в анализируемом веществе.
В химических методах качественного анализа используют характерные качественные аналитические реакции, для которых присущи определенные внешние проявления: образование в растворах цветных осадков, изменение цвета раствора или сплава, выделение газообразных продуктов без запаха или с определенным запахом и т.д. Вещество, которое используют для проведения качественной реакции, называют реагентом.
Аналитические реагенты и аналитические реакции подразделяют на специфические(характерные), селективные(избирательные), групповые.
Специфическиереагенты и реакции позволяют обнаруживать данное вещество или данный ион в присутствии других веществ или ионов.
Селективные реагенты и реакции позволяют обнаруживать несколько веществ или ионов.
Групповыереагенты и реакции позволяют обнаруживать ионы определенной аналитической группы.
Аналитическая реакция – химическое превращение анализируемого вещества при действии аналитического реагента с образованием продуктов с заметными аналитическими признаками.
Качественный химический анализ включает дробныйи систематический анализ.
Дробный анализ- обнаружение ионов или вещества в анализируемой пробе с помощью специфического реагента в присутствии всех компонентов пробы.
Систематический анализ- предусматривает разделение смеси анализируемых ионов по аналитическим группам с помощью групповых реагентов и последующее обнаружение каждого иона.
При выполнении качественного анализа нужна определенная масса пробы. В зависимости от величины взятой для анализа пробы методы разделяют на: макро-, полумикро-, микро- и ультрамикрометоды качественного анализа.
В макро- анализе используют 0,5-1,0 г вещества. В микроанализе используют, как правило, от 0,010 до 0,001 г вещества
Полумикроанализ занимает промежуточное место между макро- и микро-методами. Для анализа, как правило, используют от 0,01 до 0,10 г сухого вещества.
Аналитические реакции выполняют с помощью капельниц. Отделение твердой и жидкой фаз проводят с помощью центрифуги. В аналитической практике используют чаще полумикрометод.
Аналитические реакции выполняют сухим или мокрым способом. В первом случае исследуемую пробу и аналитический реагент берут в твердом состоянии и подвергают нагреванию при высокой температуре. К таким способам относят окрашивание пламени и спекание с некоторыми сухими реагентами (Nа2CO3, KClO3, KNO3) для получения характерных окрашенных продуктов и др. Реакции, выполняемые мокрым способом сопровождаются внешним эффектом: изменение окраски раствора, образование или растворение осадка, выделение газа.
Схема: «Качественные реакции на катионы и анионы в растворах» 
Количественный анализ
| Физико-химический | Физический | Химический |
| Метод колориметрии | Метод рефрактометрии | Гравиметрический (весовой) Титриметрический(объемный) Измеряют точный объем раствора реактива(исходное вещество) с известной концентрацией, который добавляют к раствору анализируемого вещества, концентрацию которого определяют. Методы Нейтрализации, оксидиметрии, комплексометрии, осаждения |
Количественный анализ служит для определения количественного состава отдельных частей в исследуемом веществе или смеси. Одним из методов количественного анализа является титриметрический (объемный) анализ.
Титриметрический анализ основан на точном измерении количества реактива, затраченного на реакцию с определенным компонентом. Раствор, содержащий реагент, концентрация которого известна с большой точностью называетсярабочим раствором или титрантом. Второй раствор, вступающий во взаимодействие с рабочим раствором, содержит вещество неизвестной концентрации и называетсяанализируемым раствором.
Объемный анализ основан на процессетитрования. Титрованием называют добавление небольших порций одного из растворов к заранее известному объему другого раствора. В процессе титрования наступаетточка эквивалентности, когда количество реагирующих веществ в смеси становится эквивалентным. Чтобы зафиксировать конец титрования используютиндикаторы - вещества изменяющие свою окраску в зависимости от pH среды.
Для приготовления растворов в титриметрическом методе используют стандартные вещества.
Стандартный раствор– раствор, имеющий известную концентрацию активного реагента.Различают первичный и вторичный стандартные растворы
Первичный стандартный раствор– это раствор исходного вещества, приготовленный из первичного стандартного вещества, концентрация которого известна по массе этого вещества в определённом объёме раствора. В качестве исходного вещества используют буру Na2B4O7·10H2O, карбонат натрия безводный Na2CO3, щавелевую кислоту H2C2O4·2H2O и др. Навески этих веществ находятся в фиксаналах- стеклянных запаянных ампулах. Для приготовления стандартного раствора фиксанал разбивают и переносят в мерную колбу, доводя дистиллированной водой до метки на колбе, соответствующей определённому объёму. Эти растворы используются как стандарты.
Вторичный стандартный раствор(рабочий раствор) это раствор, концентрация которого установлена очень точно стандартизацией. В качестве вторичного стандартного раствора в методе алкалиметрии используется 0,1н раствор гидроксида калия или натрия, а в методе ацидиметрии - раствор 0,1н HCl.
Конечная точка титрования- это момент титрования, в котором в присутствии индикатора окраска раствора резко изменяется. Точку эквивалентности можно определять по появлению флуоресценции, изменению оптической плотности или электропроводности.
Интервал перехода индикатора- это область титрования, в которой можно обнаружить изменение в оттенке цвета или интенсивности, вызванное изменением соотношения двух соответствующих форм индикатора.
Кривая титрования– это графическое изображение изменения pH титруемого раствора в зависимости от количества титранта.
(Таблица индикаторов)
Титриметрический анализ делится на:
1. Кислотно-основное титрование (метод нейтрализации) –это титрование, основанное на реакции переноса протона Н+ от одной реагирующей частицы к другой. Различают алкалиметрию и ацидиметрию (acidum – кислота, alkali – щёлочь).
- Алкалиметрия -определение концентрации вещества титрованием, в котором стандартным (рабочим) раствором является раствор сильного основания.
- Ацидиметрия -определение концентрации вещества титрованием, в котором стандартным (рабочим) раствором является раствор сильной кислоты.
2. Окислительно-восстановительное титрование (оксидиметрия) -это титрование, которое сопровождается переходом электронов от восстановителя к окислителю.
В методах оксидиметрии в зависимости от применяемого титрованного раствора окислителя различают несколько частных методов:
а) перманганатометрия,метод, в котором рабочим раствором служит раствор КMnO4 в кислой среде.
б) йодометрия,метод,в котором рабочим раствором служит раствор йода.
3. Осадительное титрование -такое титрование, в результате которого титруемое вещество при взаимодействии с титрантом выделяется из раствора в виде осадка.
4. Комплексонометрическое титрование -титрование, которое сопровождается образованием слабодиссоциирующего растворимого комплексного соединения.
В аналитической химии используют различные способы титрования.
а) прямое титрование;
б) обратное титрование;
в) заместительное (косвенное) титрование.
Прямое титрование -титрование, при котором анализируемое вещество титруют стандартным раствором титранта.
Обратное титрование (титрование по остатку) -титрование непрореагировавшего остатка вещества, взятого в избытке.
Косвенное титрование (заместительное)- титрование, при котором определяемое вещество не реагирует с титрантом непосредственно, а определяется косвенно в результате использования стехиометрически протекающей реакции с образованием другого вещества, реагирующего с титрантом.
