Окислительно-восстановительные реакции. Понятие восстановительного потенциала.
Окислительно-восстановительными реакциями называются реакции, протекающие с изменением степени окисления атомов элементов, входящих в состав реагирующих веществ.
Окислительно-восстановительные реакции – это реакции, сопровождающиеся изменением степени окисления атомов в молекулах реагирующих веществ в результате перехода электронов от одних атомов к другим.
Под степенью окисления понимают условный заряд атома в соединении, вычисленный, исходя из предположения, что соединение состоит из ионов. Степень окисления атомов определяют, пользуясь следующими правилами:
1. Степень окисления в простом веществе (например, O2, N2, Cl2, Zn, S и др.) равна нулю
2. Степень окисления кислорода в соединениях равна -2, за исключением пероксидов (например, Н2О2–1) и и фторида кислорода O+2F2.
3. Степень окисления водорода в соединениях равна +1, за исключением гидридов (например, NaH–1, CaH2–1).
4. Степень окисления фтора в соединениях равна -1.
5. Алгебраическая сумма степеней окисления всех атомов в молекуле равна нулю, а в сложном ионе – заряду иона.
Руководствуясь этими правилами, можно рассчитать степень окисления любого атома. Например,
+1 x -2
HNO3 Степень окисления азота х=+5
+1 2х -2
K2Cr2O7 Степень окисления хрома х=+6
Межмолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl
Внутримолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
2H2O → 2H2 + O2
Диспропорционирование (самоокисление-самовосстановление) — реакции, в которых атомы с промежуточной степенью окисления превращаются в эквимолярную смесь атомов с более высокой и более низкой степенями окисления, например:
Cl2 + H2O → HClO + HCl
Репропорционирование (компропорционирование) — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления, например:
NH4NO3 → N2O + 2H2O
21.Общая характеристика элементов 1-7 групп периодической системы:
Положение элемента в ПС, валентные возможности, правило четности, распространение в природе и основные природные формы соединений, характеристики простых тел, физические и химические свойства, важнейшие соединения, кислотно-основные и окислительно-восстановительные свойства.


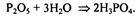

Б) Характеристика калия.

Химия воды.
Вода H2O – это оксид водорода , в котором водород проявляет степень окисления +1, а O-2
Молекула воды полярна и имеет угловую форму. Молекула воды взаимодействует между собой, образуя водородную связь. Это обуславливает аномалию температур плавления и кипения - они значительно выше, чем у ее химических аналогов.
Физические свойста:
Чистая вода не имеет цвета, вкуса и запаха, толстые слои воды (более 5 м) имеют голубую окраску. Затвердевание воды в лёд сопровождается увеличением объёма на 9%, то есть лёд легче жидкой воды (вторая аномалия воды). T кип = +100,0 °C Наибольшую плотность вода имеет не при 0 °C, а при 4 °C (третья аномалия воды).
Сущ-ет в 3 агрегатных состояниях: тв.- лед, жидкое и газообразное – водяной пар.
Химические свойства:
Вода - чрезвычайно слабый электролит (H2O <—> Н+ + ОН−), электропроводность чистой (дистиллированной) воды весьма мала, поэтому электролиз воды проводят в присутствии сильных электролитов.
По химическим свойствам вода - достаточно активное вещество, в подходящих условиях она реагирует со многими металлами и неметаллами, основными и кислотными оксидами:
2H2О + 2Na = 2NaOH + H2↑ H2O + BaO = Ba(OH)2
H2O + Cl2 = HClO + HCl 3H2O + P2O5 = 2H3PO4
- Благодаря полярности молекул воды в ней растворяются и диссоциируют основания, кислоты и соли, большинство солей вступает с водой в реакции обратимого гидролиза.
- Вода как растворитель способствует протеканию огромного количества обменных и окислительно-восстановительных реакций.
- Со многими безводными солям вода образует кристаллогидраты ( белого сульфата меди(II) CuSO4 в голубой медный купорос CuSO4 . 5H2O).
