Получение и свойства оснований
Получение.
1. Щелочи (растворимые в воде основания) можно получить:
а) при взаимодействии щелочных и щелочноземельных металлов с водой:
2Na + 2H2O = 2NaOH + H2
б) при взаимодействии оксидов щелочных и щелочноземельных металлов с водой:
Na2O + Н2O = 2NaOH
СаО + Н2O = Са(ОН)2
2. Нерастворимые в воде основания получаются при взаимодействии водного раствора соли со щелочью:
FeSO4 + 2NaOH = Fe(ОН)2¯ + Na2SO4
AlC13 + 3КОН = Al(ОН)3¯ + 3КС1
Физические свойства. Основания — твердые вещества, различно окрашенные: КОH, Са(ОН)2, NaOH — белые, Ni(ОН)2 — зеленый и др.
По растворимости в воде основания делятся на две группы: растворимые в воде (щелочи) и нерастворимые. Щелочами являются гидроксиды щелочных (элементов главной подгруппы I группы), щелочноземельных (элементов главной подгруппы II группы, кроме Be и Mg) металлов. Например, КОН — гидроксид калия, NaOH — гидроксид натрия, Ca(OH)2 — гидроксид кальция. Щелочи - это ионные соединения. В узлах кристаллических решеток твердых щелочей находятся ионы металлов и гидроксид-ионы.
Гидроксиды всех других металлов нерастворимы в воде.
Химические свойства.
1. Растворы щелочей изменяют окраску многих индикаторов (см. «Кислоты»).
2. Основания взаимодействуют с кислотами. При этом образуются соль и вода. Реакция между основанием и кислотой называется реакцией нейтрализации.
NaOH + HC1 = NaCl + Н2О
гидроксид хлороводородная хлорид
натрия кислота натрия
Mg(ОН)2 + HC1 = MgOHCl + Н2О
гидроксид хлороводо - хлорид
магния родная гидроксо -
кислота магния
MgOHCl + HCl = MgCl2 + Н2О
Са(ОН)2 + H3PO4 = СаНРО4 + 2Н2О
гидроксид ортофосфор - гидрофосфат
кальция ная кислота кальция
3. Щелочи взаимодействуют с кислотными оксидами. При этом образуются соль и вода:
Са(ОН)2 + СО2 = СаСО2¯ + Н2О
гидроксид оксид карбонат
кальция углерода(IV) кальция
4. Щелочи взаимодействуют с солями. При этом могут образоваться новое основание и соль (средняя или основная)(необходим признак протекания реакции):
а) средняя соль: NiCl2 + 2NaOH = Ni(ОН)2↓ + 2NaCl
хлорид гидроксид гидроксид хлорид
никеля (II) натрия никеля (II) натрия
в) основная соль: CuCl2 + NaOH = CuOHCl + NaCl
хлорид гидроксид хлорид хлорид
меди(II) натрия гидроксо - натрия
меди(II)
5. При нагревании основания разлагаются на оксид металла и воду:
Сu(ОН)2 = СuО + Н2О
гидроксид оксид
меди меди
Амфотерные гидроксиды
Гидроксиды, которые взаимодействуют с кислотами и щелочами с образованием солей, называются амфотерными.
C позиций теории электролитической диссоциации, амфотерными называются гидроксиды, которые при диссоциации образуют и катионы водорода и гидроксид-ионы.
К амфотерным гидроксидам относятся гидроксиды некоторых металлов главных подгрупп (бериллия, алюминия), а также некоторых металлов побочных подгрупп периодической системы элементов в промежуточных степенях окисления. Например,Ве(ОН)2,Al(ОН)3, Zn(OH)2, Ge(OH)2, Sn(ОН)4, Fе(ОН)3, Сr(ОН)3 — амфотерные гидроксиды.
Получение. Амфотерные гидроксиды нерастворимы в воде. Получают их, как и другие нерастворимые в воде основания, при взаимодействии солей со щелочами (чтобы получившийся гидроксид не растворился в избытке щелочи, берут эквивалентное количество щелочи). Например,
Cr2(SO4)3 + 6NaOH = 2Cr(OH)3¯ + 3Na2SO4
Химические свойства. В зависимости от условий амфотерные гидроксиды могут проявлять основные или кислотные свойства.
Al3+ + 3OH- « Al(OH)3 º Al(OH)3 + 3H2O « [Al(OH)4(H2O)2]- + H+
1. При взаимодействии с кислотами амфотерные гидроксиды проявляют основные свойства:
А1(ОН)3 + 3НС1 = А1С13 + 3Н2О
2. При взаимодействии со щелочами амфотерные гидроксиды проявляют кислотные свойства:
3А1(ОН)3 + 3NaOH = 3Na[Al(OH)4]
кислота основание тетрагидроксоалюминат натрия
Соли
Названия и формулы солей
Соли — это продукты замещения водорода кислоты металлом или гидроксогрупп оснований кислотными остатками.
Например,
H2SO4 + Zn = ZnSO4 + Н2
NaOH + НС1 = NaCl + H2O
С позиций теории электролитической диссоциации, соли – это электролиты, при диссоциации которых образуются катионы,отличные от катионов водорода, и анионы, отличные от анионов ОН- .
Классификация. Соли бывают средние, кислые, основные, двойные, комплексные.
Средняя соль — это продукт полного замещения водорода кислоты металлом или гидроксогруппы основания кислотным остатком. Например, Na2SO4, Ca(NO3)2 — средние соли.
Кислая соль — продукт неполного замещения водорода многоосновной кислоты металлом. Например, NaHSO4, Са(НСО3)2 — кислые соли.
Основная соль — продукт неполного замещения гидроксогрупп многокислотного основания кислотными остатками. Например, Mg(OН)С1, Bi(OH)Cl2 — основные соли
Если атомы водорода в кислоте замещаются атомами разных металлов или гидроксогруппы оснований замещаются различными кислотными остатками, то образуются двойные соли. Например, KAl(SO4)2, Са(ОС1)С1. Двойные соли существуют только в твердом состоянии.
Комплексные соли — это соли, в состав которых входят комплексные ионы. Например, соль K4[Fe(CN)6] — комплексная, так как в ее состав входит комплексный ион [Fe(CN)6]4-.
Составление формул солей. Можно сказать, что соли состоят из остатков оснований и остатков кислот. При составлении формул солей нужно помнить правило: абсолютная величина произведения заряда остатка основания на число остатков основания равна абсолютной величине произведения заряда кислотного остатка на число кислотных остатков. Для 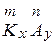 тх = пу, где K — остаток основания, A — кислотный остаток, т — заряд остатка основания, n — заряд кислотного остатка, х — число остатков основания, у — число кислотных остатков. Например,
тх = пу, где K — остаток основания, A — кислотный остаток, т — заряд остатка основания, n — заряд кислотного остатка, х — число остатков основания, у — число кислотных остатков. Например,
| Формулы: | 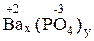 | 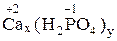 | 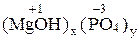 |
| 2x = 3y x = 3, y = 2 Ba3(PO4)2 | 2x = 1y x = 1, y = 2 Ca(H2PO4)2 | 1x = 3y x = 3; y = 1 (MgOH)3PO4 |
Номенклатура солей. Названия солей составляют из
названия аниона (кислотного остатка (табл.. 15)) в именительном падеже и названия катиона (остатка основания (табл. 17 )) в родительном падеже (без слова «ион»).
Для названия катиона используют русское название соответствующего металла или группы атомов (в скобках римскими цифрами указывают степень окисления металла, если это необходимо).
Анионы бескислородных кислот называют, используя окончание –ид (NH4F – фторид аммония, SnS – сульфид олова (II), NaCN – цианид натрия). Окончания названий анионов кислородсодержащих кислот зависят от степени окисления кислотообразующего элемента:
| Окончание названия кислоты | Название аниона |
| -ная, -овая | -ат |
| -истая | -ит |
| -оватистая | Гипо- + -ит |
Названия кислых и основных солей образуются по тем же общим правилам, что и названия средних солей. При этом название аниона кислой соли снабжают приставкой гидро-, указывающей на наличие незамещенных атомов водорода (число атомов водорода указывают греческими числительными приставками). Катион основной соли получает приставку гидроксо-, указывающую на наличие незамещенных гидроксогрупп.
Например,
MgС12 – хлорид магния
Ba3(РО4)2 – ортофосфат бария
Na2S – сульфид натрия
CaHPO4 – гидрофосфат кальция
K2SO3 – сульфит калия
Ca(H2PO4)2 – дигидрофосфат кальция
А12(SO4)3 – сульфат алюминия
Mg(OH)Cl – хлорид гидроксомагния
КА1(SO4)2 – сульфат калия-алюминия
(MgOH)2SO4 – сульфат гидроксомагния
KNaHPO4 – гидрофосфат калия-натрия
MnCl2 – хлорид марганца (II)
Са(OCI)C1 – хлорид-гипохлорит кальция
MnSO4 – сульфат марганца (II)
К2S – cульфид калия
NaHCO3 – гидрокарбонат натрия
К2SO4 – сульфат калия
Получение и свойства солей
Получение. Соли получают:
1. При взаимодействии металла с неметаллом:
Fe + S = FeS
2. При взаимодействии металла с кислотами:
Zn + 2НС1 = ZnCl2 + Н2
3. При взаимодействии металла с солями:
Сu + Hg(NО3)2 = Hg¯ + Сu(NO3)2
4. При взаимодействии металлов, оксиды которых амфотерны, со щелочами:
Zn + 2NaOH = Na2ZnO2 + Н2
5. При взаимодействии основных оксидов с кислотами:
СаО + 2НС1 = CaCl2 + H2О
6. При взаимодействии основныхоксидов с кислотными оксидами:
MgO + СO2 = MgСO3
7. При взаимодействии оснований с кислотами:
2КОH + H2SO4 = K2SO4 + 2H2O
КОН + H2SO4 = KHSO4 + Н2О
Bi(ОН)3 + HC1 = Bi(ОН)2С1 + Н2О
8. При взаимодействии оснований с кислотными оксидами:
NaОН + СO2 = NаНСО3
3NaОН + СО2 = Na2CO3 + H2O
9. При взаимодействии щелочей с солями:
CuCl2 + NaOH = СuОНСl + NaCl
CuCl2 + 2NaOH = Сu(ОН)2 + 2NaCl
10. При взаимодействии щелочей с неметаллами:
2NaOH + Cl2 = NaCl + NaClO + H2O
11. При взаимодействии солей с кислотами:
ВaС12 + Н2SO4 = ВaSO4¯ + 2НС1
12.При взаимодействии солей с кислотными оксидами:
Na2CO3 + SiO2 = Na2SiO3 ¯+ СО2
CaCO3 + CO2 + H2O = Ca(HCO3)2
13.При взаимодействии солей между собой:
Ва(NО3)2 + Na2SO4 = BaSO4 ¯ + 2NaNO3
14. При взаимодействии солей с неметаллами:
2KI + Сl2 = 2КСl + I2
Физические свойства. Соли — твердые кристаллические вещества. Остатки оснований и кислот в солях связаны между собой, как правило, ионной связью. Соли имеют разный цвет и характеризуется различной растворимостью в воде.
Химические свойства.
1. Соли реагируют со щелочами. При этом образуются новая соль и новое основание или основная соль:
MgCl2 + 2NaOH = Mg(OH)2 + 2NaCl
MgCl2 + NaOH = MgOHCl + NaCl
2. Соли взаимодействуют с кислотами. При этом образуются
а) новая кислота и новая средняя соль:
Ва(NO3)2 + H2SO4 = BaSO4¯+ 2HNO3
б) кислая и средняя соли
Са3(РO4)2 + 2Н2SO4 = Са(Н2РO4)2 + 2CaSO4
в) только кислая соль
Na2S + H2S = 2NaHS
3. Соли могут взаимодействовать между собой. При этом образуются новые соли. Реакции обмена между растворами солей идут до конца, если в результате реакции образуется нерастворимая соль:
CaCl2 + Nа2СО3 = СаСО3 ¯ + 2NaCl
4. Соли могут взаимодействовать с металлами.
CuSO4 + Fe = FeSO4 + Cu¯
Каждый металл может вытеснить из растворов солей все металлы, стоящие в ряду напряжений после него, и не может вытеснить металлы, стоящие перед ним:
FeSO4 + Сu ® реакция не идет
5. Некоторые соли разлагаются при нагревании:
СаСО3 = СаО + СО2
УПРАЖНЕНИЯ
1. Какие способы получения солей вызнаете?
2. Составьте уравнения реакций между следующими веществами:а) железоми хлороводородной кислотой; б) серной кислотой и гидроксидом натрия; в) хлоридом алюминия и гидроксидом калия; г) нитратомбарияи сульфатом натрия; д) хлоридом магния и нитратом серебра.
3. Напишите уравнения реакций, при помощи которыхможноосуществить следующиепревращения:
1) Сu ® СuО ® CuSO4 ® Сu(ОН)2 ® CuCl2 ® Сu
2) Zn ® ZnO ® ZnSO4 ® Zn(ОH)2 ® Na2 ZnO2
3) Р ® Р2О5®Н3РО4 ®Na3PO4 ®Са3(PO4)2
4) Mg ® МgО ® Mg(OH)2 ® MgCl2 ® Mg(NO3)2
