Возбужденные состояния атома водорода
Полученное решение уравнения Шредингера для основного состояния атома водорода является частным случаем, когда волновая функция сферически симметрична и не зависит от угловых координат. Для атома водорода решениями уравнения Шредингера могут быть и другие функции, как сферически симметричные, так и более сложной симметрии.
В общем виде волновая функция в полярных координатах является функцией трех переменных Y=  , поэтому уравнение Шредингера будет представлять собою дифференциальное уравнение с частными производными. Стандартный метод решения уравнения данного типа - метод разделения переменных.
, поэтому уравнение Шредингера будет представлять собою дифференциальное уравнение с частными производными. Стандартный метод решения уравнения данного типа - метод разделения переменных.
Полагают, что волновая функция  может быть представлена в виде произведения трех волновых функций, каждая из которых содержит только одну переменную:
может быть представлена в виде произведения трех волновых функций, каждая из которых содержит только одну переменную:
Y(r, J ,j) = R(r)×Q(J)×F(j).
Часто две угловые функции заменяют одной функцией углового распределения Y(q,j):
Y(r, J ,j) = R(r)×Y(q,j),
где R(r) и Y(q,j) – функции радиального и углового распределения электронной плотности.
Явный вид волновых функций, полученный при решении уравнения Шредингера, показывает, что они содержат целочисленные параметры: R(r) содержит n, l, а Y(q,j) – l, m.
Таким образом, решением общего волнового уравнения является набор собственных волновых функций, которые содержат в качестве целочисленных параметров три числа: n, l, m, которые получили названия главного (n), орбитального (l) и магнитного (m) квантовых чисел. Квантовые числа характеризуют набор волновых функций и соответствующих им энергетических состояний электрона в атоме водорода.
Кроме трех квантовых чисел имеется четвертое – спиновое. Непосредственно из решения уравнения Шредингера для атома водорода спиновое квантовое число не получается.
В 1933 г. Поль Дирак (Dirac) описал состояние электрона в атоме с учетом релятивистских эффектов (привел в соответствие представления Шредингера с теорией относительности Эйнштейна). Полученные решения содержат кроме трех квантовых чисел четвертый параметр –спиновое квантовое число (mS).
Физический смысл квантовых чисел.
n - главное квантовое число – определяет разрешенные (дискретные, квантовые) значения полной энергии электрона, характеризует размер электронных орбиталей (соответственно является мерой расстояния между электроном и ядром).
Решение уравнения Шредингера дает следующее выражение для возможных значений полной энергии электрона в атоме водорода:
 .
.
Главное квантовое число может принимать целочисленные значения от единицы до бесконечности: n = 1,2,3,4…¥.
Для электронов в атомах элементов периодической системы, находящихся в невозбужденном состоянии, максимальное значение n равно 7.
l – орбитальное квантовое число – определяет возможные квантовые значения орбитального момента количества движения электрона, то есть связано с его кинетической энергией.Пространственная конфигурация (форма) электронной орбитали связана со значением орбитального квантового числа. Возможные величины l соответствуют n и могут принимать целочисленные значения от 0 до n-1: l = 0,1,2,3...(n–1).
Исторически сложилось, что численным значениям l соответствуют буквенные обозначения: l = 0 – s; l = 1 – p; l = 2 – d; l = 3 – f и т. д. Они соответствуют также электронам, их волновым функциям, орбиталям и энергетическим состояниям.
Пространственная конфигурация простейших орбиталей (форма) показана на рис.1.10: s-орбиталь (l = 0) – сферически симметричная; p-орбиталь (l = 1), d-орбиталь (l = 2), f –орбиталь (l = 3) и т.д имеют более сложную пространственную симметрию.
m - магнитное квантовое число– определяет разрешенные направления в пространстве вектора орбитального момента количества движения. Возможные значения m определяются для каждого значения l и могут принимать целочисленные значения от от +l до -l: m = +l, (l-1),...,0,...,(-l+1), -l.
 |
Рис. 1.10. Пространственная конфигурация простейших орбиталей
Набор значений mопределяет числовозможных ориентаций s, p, d, … орбиталей в пространстве для данного числа n. Поскольку потенциальная энергия частицы зависит от ее положения в пространстве, то магнитное квантовое число связано с потенциальной энергией электрона.
s-орбитали (l=0) – магнитное квантовое число принимает единственное значение m=0 – единственный способ ориентации в пространстве (сферически-симметричная орбиталь).
 p-орбитали (l=0) – магнитное квантовое число принимает три возможных значения m=+1,0,-1 – три возможных способа ориентации орбитали в пространстве (рис.1.11).
p-орбитали (l=0) – магнитное квантовое число принимает три возможных значения m=+1,0,-1 – три возможных способа ориентации орбитали в пространстве (рис.1.11).
d-орбитали (l=2) – магнитное квантовое число принимает пять возможных значений m=+2,+1,0,-1,-2 – пять возможных способов ориентации орбитали в пространстве (рис. 1.12).
 |
Рис. 1.12. Возможные ориентации d–орбитали в пространстве
ms - спиновое квантовое число – характеризует собственный момент количества движения и может принимать только два значения:  , которые в модели Уленбека и Гаудсмита соответствуют вращению электрона вокруг собственной оси по или против часовой стрелки.
, которые в модели Уленбека и Гаудсмита соответствуют вращению электрона вокруг собственной оси по или против часовой стрелки.
Собственный момент количества движения электрона связан с собственным магнитным моментом, взаимодействие которого с магнитным полем атома приводит к двум возможным энергетическим состояниям.
Электронные орбитали атома водорода.
Поскольку электронную орбиталь характеризует набор трех квантовых чисел, то все возможные электронные орбитали атома водорода, получаются путем различных комбинаций квантовых чисел. Для первых четырех значений главного квантового числа возможные орбитали (энергетические состояния электрона) приведены в и на энергетической диаграмме (рис. 1.13).
Обозначение орбитали складывается из цифры, которая указывает главное квантовое число, и буквы, указывающей тип орбитали (орбитальное квантовое число). Например, 5р – это орбиталь, имеющая n=5 и l=1. Графически орбитали изображаются в виде черточек или прямоугольников.
| n | l=0,1,2…(n-1) | m=+l, (l–1),...0...(1– l),-l | Энергия орбитали | Число орбиталей |
| 0 - s | E1 | |||
| 0 – s 1 - p | +1,0,-1 | E2 | ||
| 0 – s 1 – p 2 - d | +1,0,-1 +2,+1,0,-1,-2 | E3 | ||
| 0 – s 1 – p 2 – d 3 - f | +1,0,-1 +2,+1,0,-1,-2 +3,+2,+1,0,-1,-2,-3 | E4 |
 |
Рис. 1.13. Диаграмма энергетических состояний электрона в атоме водорода
На приведенной диаграмме видно, что для атома водорода энергетические состояния электрона вырождены по орбитальному и магнитному квантовым числам (энергия электрона зависит только от главного квантового числа):
E1s < E2s = E2p< E3s = E3p = E3d < E4s = E4p = E4d = E4f < …
Радиальное распределение электронной плотности.
В квантово-механической модели атома не существует понятия траектории движения электрона, оно заменено на вероятность нахождения электрона в элементарном объеме пространства, а каким образом туда попадает электрон, не определяется. Так же как и для основного состояния, для возбужденных состояний имеются функции радиального распределения электронной плотности:
s(r)  y2×4pr2.
y2×4pr2.
Графический вид функций приведен на рис. 1.14. Площадь под любой кривой радиального распределения равна единице, поскольку она равна вероятности нахождения электрона во всем объеме:
 .
.
В радиальном распределении 1s электрона имеется один максимум на расстоянии, равном первому боровскому радиусу (1/a = 0,53A). Число максимумов в функции распределения ns электронов (n>1) равно n, 2s – два максимума, 3s – три максимума и т.д.
Функции радиального распределения для p,d,f-электронов подобны функциям для s электронов, с учетом того, что число максимумов равно n – l: 1s, 2p, 3d...– функции радиального распределения с одним максимумом, 2s, 3p, 4d...– с двумя, 3s, 4p, 5d.. – с тремя максимумами.
 |
Рис. 1.14. Функции радиального распределения электронной плотности для различных энергетических состояний атома водорода
Из приведенных рисунков видно, что, во-первых, положение главного максимума, расстояние от ядра до области с максимальной вероятностью нахождения электрона, определяется в основном главным квантовым числом n, то есть можно говорить о том, что n характеризует «расстояние электрона до ядра». Во-вторых, для электронов, находящихся в состояниях с одинаковым главным квантовым числом, вероятность нахождения электрона вблизи ядра уменьшается с увеличением орбитального квантового числа (иногда говорят о различной «проникающей способности» орбиталей). Это имеет большое значение при рассмотрении многоэлектронных атомов.
Различия в проникающей способности орбиталей можно проиллюстрировать также зависимостью вероятности нахождения электрона в объеме сферы радиуса r в зависимости от ее радиуса (рис. 1.15):
 |
 .
. Рис. 1.15. Вероятность нахождения электрона атома водорода в объеме сферы радиуса r, занимающего 3s, 3p или 3d-орбиталь
Многоэлектронные атомы
В случае многоэлектронного атома (число электронов два и более) получить точные решения уравнения Шредингера невозможно (сложно), поскольку необходимо учитывать энергию взаимодействия электронов не только с ядром, но и между собой. Поэтому при определении волновых функций и энергетических состояний используют приближенные методы. В частности, при описании системы рассматривают движение одного электрона в эффективном поле, которое образуется полем ядра и полем остальных электронов. При этом используют понятие эффективного заряда ядра.
Эффективный заряд ядра (Zэ) равен заряду ядра (Z) за вычетом константы экранирования (s) –постоянной величины, учитывающей влияние остальных электронов атома на рассматриваемый электрон: Zэ = Z - s. При таком приближенном рассмотрении состояние электрона описывается волновыми функциями, подобными тем, которые были получены для атома водорода. Увеличение заряда ядра и различия в радиальном распределении электронной плотности для электронов, находящихся на различных орбиталях, приводят к изменению энергии орбиталей по сравнению с атомом водорода. Отличия заключаются в следующем.
1. Увеличение заряда ядра приводит к возрастанию энергии притяжения электрона к ядру и соответственно к понижению энергии электронной орбитали (рис. 1.16).
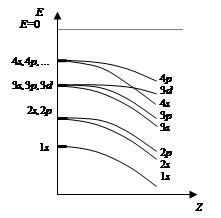 |
2. Вследствие различного радиального распределения электронной плотности s, p, d, f-электронов величина константы экранирования зависит не только от числа электронов, создающих эффективный заряд ядра, но и от типа орбиталей, которые они занимают (sn,l). Понижение энергии орбиталей с ростом заряда ядра (для одного значения n) различно для s, p, d, f-состояний, что приводит к снятию вырождения по орбитальному квантовому числу.
Рис. 1.16. Схема изменения энергии орбиталей в зависимости от Z
3. Вследствие снятия вырождения по орбитальному квантовому числу энергия электрона определяется не только главным квантовым числом n, но и орбитальным l.
Пример. Константа экранирования (s) и эффективный заряд ядра (Zэ) атомов для первых 11 элементов периодической таблицы:
| Атом | H | He | Li | Be | B | C | N | O | F | Ne | Na |
| Z | |||||||||||
| s | 0,3 | 1,70 | 2,05 | 2,40 | 2,75 | 3,10 | 3,45 | 3,80 | 4,15 | 8,80 | |
| Zэ=Z-s | 1,7 | 1,30 | 1,95 | 2,60 | 3,25 | 3,90 | 4,55 | 5,20 | 5,85 | 2,20 |
Энергия орбитали 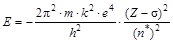 ,
,
Z – s = Zэ – эффективный заряд ядра; n* – эффективное главное квантовое число, s; Zэ; n* вычисляются по правилам, разработанным Слэтером (Slater).
Таким образом получается последовательность энергетических состояний в многоэлектронном атоме (стационарные состояния реально существующих атомов):
E1s<E2s<E2p<E3s<E3p<E4s<E3d<E4p<E5s<E4d<E5p<E6s<E4f<…
 Эту последовательность можно проиллюстрировать энергетической диаграммой электронных орбиталей многоэлектронного атома с определенным значением Z (рис. 1.17). Диаграмма показывает энергетическое положение орбиталей относительно друг друга в атоме с определенным зарядом ядра Z, но не их абсолютные значения.
Эту последовательность можно проиллюстрировать энергетической диаграммой электронных орбиталей многоэлектронного атома с определенным значением Z (рис. 1.17). Диаграмма показывает энергетическое положение орбиталей относительно друг друга в атоме с определенным зарядом ядра Z, но не их абсолютные значения.
Рис. 1.17. Диаграмма энергетических состояний невозбужденного многоэлектронного атома
Каждый последующий атом в периодической системе отличается от предыдущего тем, что заряд его ядра увеличивается на единицу и соответственно на единицу увеличивается число электронов. Каждому электрону должно соответствовать свое энергетическое состояние, которое описывается четырьмя квантовыми числами. В изолированных многоэлектронных атомах энергетические состояния электронов вырождены по магнитному и спиновому квантовому числу. В электромагнитном поле (внешнее поле или поле окружающих атомов) это вырождение может сниматься (рис. 1.18).
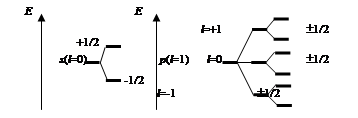 |
Рис. 1.18. Схема снятия вырождения для s и р энергетических состояний
в электромагнитное поле
