А. п. киселев, а.а. крашенинников
Кафедра химии
А. П. КИСЕЛЕВ, А.А. КРАШЕНИННИКОВ
ОСНОВЫ ОБЩЕЙ ХИМИИ
Часть 1
Строение вещества
Учебное пособие
Санкт-Петербург
2002
УДК 541(075.8)
ББК 24.1
К44
|
Основы общей химии. Ч.1. Строение вещества: Учебное пособие / Балт. гос. техн. ун-т. СПб., 2002. 109 с.
Пособие содержит материалы по вопросам строения атома, химической связи и строения твердых веществ в соответствии с одноименными разделами курса химии.
Предназначено для самостоятельной подготовки студентов всех специальностей.
УДК 541(075.8)
ББК 24.1
Рецензенты: кафедра общей и неорганической химии Санкт-Петербургского государственного политехнического университета (зав. каф. д-р. хим. наук, проф. Л.Н. Блинов); зав. каф. физической химии Санкт-Петербургского государственного технологического института (университета), д-р. хим. наук, проф. Л.В. Пучков
Утверждено
редакционно-издательским
советом университета
 ã БГТУ, СПб., 2002
ã БГТУ, СПб., 2002
|
Введение...................................................................................................................................................................... 4
Используемые единицы измерений и основные константы.................................................. 5
1.Строение атома....................................................................................................................................................... 6
1.1.Предпосылки возникновения волновой механики............................................................... 6
1.1.1.Корпускулярно-волновая природа электромагнитного излучения........................ 6
1.1.2 .Теория строения атома Бора................................................................................... 7
1.1.3.Корпускулярно-волновой дуализм свойств материи............................................... 9
1.1.4.Принцип неопределенности....................................................................................... 10
1.2.Волновая (квантовая) механика...................................................................................... 10
1.2.1.Волновое уравнение. Уравнение Шредингера........................................................... 10
1.2.2.Решение уравнения Шредингера для простейших случаев..................................... 12
1.3.Квантово-механическая модель атома.......................................................................... 16
1.3.1.Основное состояние атома водорода...................................................................... 16
1.3.2.Радиальное распределение электронной плотности. Электронная орбиталь.... 18
1.3.3.Возбужденные состояния атома водорода............................................................ 19
1.3.4.Многоэлектронные атомы........................................................................................ 22
1.3.5.Электронные конфигурации многоэлектронных атомов...................................... 24
1.3.6.Связь периодического закона со строением атома................................................ 25
1.3.7.Физико-химические характеристики атома........................................................... 26
2.Химическая связь.................................................................................................................................................. 28
2.1.Основные характеристики химической связи. Классификация моделей
описания химической связи................................................................................................. 29
2.1.1.Основные параметры химической связи................................................................. 29
2.1.2.Типы химической связи............................................................................................... 30
2.2.Ковалентная химическая связь.......................................................................................... 31
2.2.1.Метод валентных связей (ВС).................................................................................. 31
2.2.2.Кратные связи. s- и p-связи...................................................................................... 34
2.2.3.Геометрия простейших молекул. Гибридизация АО............................................... 35
2.2.4.Донорно-акцепторный механизм образования ковалентной связи....................... 38
2.2.5.Метод молекулярных орбиталей (МО).................................................................... 40
2.3.Полярность связи. Дипольный момент молекулы........................................................... 43
3.Химическая связь в твердых веществах и жидкостях....................................................................................... 43
3.1.Агрегатные состояния.......................................................................................................... 43
3.2.Межмолекулярное взаимодействие..................................................................................... 45
3.2.1.Межмолекулярные взаимодействия (силы Ван-дер-Ваальса)............................... 45
3.2.2.Водородная связь........................................................................................................ 46
3.3.Химическая связь в твердом теле................................................................... 47
3.3.1.Основные понятия о строении кристаллов............................................................ 47
3.3.2.Молекулярные кристаллы......................................................................................... 49
3.3.3.Ковалентные (атомные) кристаллы........................................................................ 50
3.3.4.Ионные кристаллы. Ионный тип химической связи............................................... 50
3.3.5.Металлические кристаллы. Металлическая химическая связь............................. 52
3.3.6.Зонная модель кристаллического тела.................................................................... 54
3.3.7.Металлы, полупроводники и диэлектрики............................................................... 56
3.3.8.Кристаллические материалы.................................................................................... 57
3.3.9.Аморфные твердые тела......................................................................................... 60
3.4.Химическая связь в жидкостях........................................................................................ 61
3.4.1.Жидкое состояние вещества................................................................................... 61
3.4.2.Жидкие кристаллы..................................................................................................... 62
Библиографический список........................................................................................................... 62
«Природе все равно, как мы это назовем,
она просто делает свое дело».
Р. Фейнман
ВВЕДЕНИЕ
При обучении квалифицированного специалиста в высшем техническом учебном заведении общенаучная подготовка играет важную роль. Во-первых, она является базой для общепрофессиональных и специальных дисциплин, во-вторых, формирует мировоззрение будущего специалиста, помогает ему быстро и правильно ориентироваться во все возрастающем потоке научно-технической информации, оценивать научный уровень технических решений. Химия, являясь одной из фундаментальных естественнонаучных дисциплин, занимает особое место в ряду других наук, преподаваемых в техническом вузе нехимического профиля.
В естествознании можно выделить несколько уровней изучения строения материальных тел, в каждом из которых действуют как свои специфические законы (законы астрономии, физики, химии, биологии и др.), так и общие фундаментальные (законы сохранения материи, энергии и др.). Каждая из естественных наук занимается своими объектами. Так, поведение макроскопических тел описывают астрономия, механика, биология и т.д. Строением молекул, атомов, ядер, элементарных частиц занимается физика. Объектом исследования химии являются вещества и материалы. Методы и применения различных наук взаимосвязаны, но каждая имеет свои специфические особенности. При этом представления каждого последующего уровня используются для объяснения, более глубокого понимания закономерностей предыдущего. Но это не значит, что все естественные науки можно свести к одной единственной («нет других естественных наук, кроме физики и аппарата ее – математики»).
Химия – наука, изучающая свойства и превращения веществ, сопровождающиеся изменением их состава и строения. Процесс превращения одних веществ в другие, в ходе которого изменяется состав, строение или заряд частиц при неизменности природы атомов, называется химической реакцией. Способность вещества участвовать в тех или иных химических реакциях характеризует его химические свойства. Химические свойства веществ и закономерности протекания химических реакций зависят от строения молекул и атомов и характера химических связей между ними. Этими же факторами определяются и многие физические свойства веществ и материалов. И все это является объектом изучения химии как науки.
К середине ХХ века объем химических знаний стал настолько большим, что это привело к делению химии на отрасли и, соответственно, появились различные химические учебные дисциплины. На основе изучаемых объектов или методов исследования выделяются следующие отрасли химических наук: неорганическая, органическая, физическая, коллоидная, радиохимия, аналитическая химия, экологическая, биохимия, радиационная, квантовая, плазмохимия, механохимия. Естественно, приведенный перечень далеко не полно охватывает все существующие отрасли химических наук, число которых увеличивается по мере накопления и углубления знаний об окружающем мире.
Студенты вузов химического профиля за время обучения изучают, в зависимости от специализации в том или ином объеме, практически все разделы химических наук. В технических вузах нехимического профиля время, отводимое учебными планами на изучение химии, весьма ограничено. Поэтому основной задачей курса «Химия» является формирование «химического мировоззрения». В первую очередь в нем обращается внимание на изучение строения химического вещества (строение атомов и молекул, химическая связь), объясняющее его химические свойства, и наиболее общих закономерностей протекания химических реакций (термодинамика и кинетика химического процесса). Изучая курс «Химия», студент должен получить представление о том, почему вещество обладает такими свойствами и что может произойти при взаимодействии тех или иных веществ. Изучение же конкретных химических свойств веществ следует проводить в рамках специальных химических дисциплин (неорганическая, органическая, коллоидная химия и др.). Необходимо отметить, что часть конкретных знаний, относящихся к химической подготовке бакалавра, магистра или дипломированного инженера, будущий специалист получает при изучении других различных учебных дисциплин (материаловедение, экология, термодинамика и др.), но представления о наиболее общих химических свойствах веществ и закономерностях протекания химических процессов должны быть сформированы в рамках базового курса. Усвоение курса «Химия» осложнено тем, что он изучается на первых курсах, при недостаточной подготовке студента по физике и математике, да и уровень элементарных знаний по химии, полученный в школе, к сожалению, часто оставляет желать лучшего.
В естествознании все теории о структуре вещества и закономерностях протекающих процессов базируются на опыте (на экспериментально наблюдаемых реальных явлениях). Любая теория только относительно верно отражает действительность. Во-первых, она обобщает лишь известные на момент ее создания экспериментальные факты и закономерности. При дальнейшем расширении и углублении знаний о мире теории уточняются или создаются новые. Во-вторых, при создании теории создается модель явления, которая абсолютизирует отдельные стороны проблемы и только в той или иной мере соответствует реальному объекту. Научные законы естествознания, с одной стороны, носят объективный характер, отражая закономерности явлений природы, с другой стороны, они верны только в определенных границах, обусловленных используемой моделью явления и условиями. Например, если размеры тела много меньше размеров пространства, в котором рассматривается это тело, используется понятие «материальная точка». Или если скорость тела много меньше скорости света, то закономерности его движения описываются законами классической механики (постоянство массы тела), если скорость движения сравнима со скоростью света, необходимо учитывать увеличение массы тела с увеличением скорости (релятивистская механика Эйнштейна).
При рассмотрении строения вещества и закономерностей протекания различных процессов необходимо обращать внимание на границы данных конкретных представлений. Если использовать для описания какого-нибудь явления закон вне границ его достоверности, то получим результаты, противоречащие опыту.
С методологической точки зрения, в учебных дисциплинах, особенно изучаемых на первых курсах, целесообразно рассматривать проверенные временем экспериментальные факты и устоявшиеся теоретические представления. В них избегают включать дискуссионные вопросы и положения имеющие частный характер.
Предлагаемое пособие написано на основе опыта преподавания курса «Химия» студентам 1 – 2-го курсов БГТУ «Военмех».
Авторы выражают благодарность коллегам по кафедре за ценные советы при обсуждении рукописи и, в первую очередь, заведующему кафедрой профессору Б.Т. Плаченову за поддержку в работе и полезную критику, а также надеются, что пособие будет полезно студентам при изучении курса химии.
И ОСНОВНЫЕ КОНСТАНТЫ
Единицы длины – [м, см, нм, Å] 1м=102см =109нм=1010Å.
Единицы энергии – [Дж, кДж, эВ] 1Дж= 10-3кДж; 1 эВ = 1,6×10-19 Дж.
Единицы массы – [кг, г] 1кг = 103 г.
Относительная атомная масса (А) и относительная молекулярная масса (М) – средняя масса атома или молекулы отнесенная к 1/12 массе атома углерода 12С (1 атомная единица массы). 1а.е.м. = 1,6605×10-27 кг.
Количество вещества – моль – количество вещества, содержащее 6,02×1023 структурных единиц (атомов, молекул, ионов).
NА=6,02×1023 [1/моль] – число Авогадро.
Молярная масса (mn) – масса одного моля вещества, выраженная в граммах, численно равна молекулярной массе (mn = М г).
Молярный объем – объем одного моля вещества. Для любого вещества в газообразном состоянии при нормальных условиях (Р = 1,013×105 Па (Н/м2); Т = 273,15 К) молярный объем равен 22,4 л.
Абсолютная термодинамическая шкала температур (Кельвина)
T K = t oC + 273,15.
Стандартные термодинамические условия:
Р0 = 1,013×105 Па (Н/м2); Т0 = 298,15 К.
Элементарный электрический заряд е = 1,602×10-19 Кл.
Электрон: масса m = 9,11×10-31 кг, заряд е = 1,60×10-19 Кл.
Скорость света в вакууме c = 2,9979×108 м/с.
Постоянная Планка h = 6,6262×10-34 Дж×с, 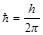 =1,0546×10-34 Дж×с.
=1,0546×10-34 Дж×с.
Константа в законе Кулона 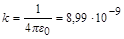 (Н×м/Кл).
(Н×м/Кл).
Радиус первой боровской орбиты атома водорода r1 = 0,53Å.
Энергия электрона атома водорода в основном состоянии Е1= –13,6 эВ.
Постоянная Больцмана k = 1,381×10-23 Дж/К.
Универсальная газовая постоянная R = 8,314 Дж/моль×К.
СТРОЕНИЕ АТОМА
Химия – фундаментальная отрасль естествознания, наука о веществах и законах их превращения, при которых молекулы одного соединения обмениваются атомами с молекулами других соединений, распадаются на молекулы с меньшим числом атомов, а также вступают в химические реакции, в результате которых образуются новые вещества. Атомы претерпевают в химических процессах некоторые изменения лишь в наружных электронных оболочках; ядро и внутренние оболочки при этом не изменяются, поэтому для курса химии теория строения атома есть в первую очередь рассмотрение способов описания состояния электронов в атоме (энергия и нахождение электрона в пространстве).
Теория строения атома Бора
Первой теорией строения атома, использующей идеи квантования энергии и описывающей ряд экспериментальных фактов, в частности линейчатые спектры атомов, стала теория строения атома Нильса Бора (Bohr).
Основным недостатком планетарной модели строения атома Резерфорда было ее противоречие теории классической электродинамики, которая утверждает, что, двигаясь по круговой орбите, электрон как заряженная частица должен непрерывно излучать энергию и "достаточно быстро упасть на ядро". Нильс Бор, разрабатывая теорию строения атома, пришел к выводу, что микрочастицы должны иметь иные свойства, чем макрообъекты, и классической электродинамики недостаточно для описания частиц атомного и субатомного размера. В своей теории описания движения электрона в атоме Нильс Бор использовал представления классической механики о движении заряженной частицы в электрическом поле, дополнив их идеями квантования энергии. При этом он выдвинул три постулата (постулат – утверждение в теории, принимаемое за истинное, хотя и недоказуемое в рамках этой теории).
Первый постулат. Существует ряд стационарных состояний атома, соответствующих определенным значениям его энергии. Электроны в атоме могут двигаться только по некоторым определенным устойчивым стационарным круговым орбитам. При движении по этим орбитам электроны не излучают энергию.
Второй постулат.При переходе с одной стационарной орбиты на другую электрон излучает или поглощает квант излучения, равный разности энергий стационарных состояний:
hn=E1–E2.
Третий постулат. В атоме существуют только такие электронные орбиты, находясь на которых электрон обладает моментом количества движения, кратным 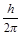 часто вводят обозначение
часто вводят обозначение 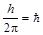 ):
):
M = m×v×r = 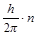 ,
,
где M – момент количества движения электрона; m = 9,11×10-31 кг – масса электрона; v – скорость электрона; r – радиус орбиты электрона; h – постоянная Планка; n = 1,2,3 ... – целое число, получившее название «квантовое число»
Используя эти постулаты, Нильс Бор рассчитал размеры стационарных орбит электронов в атоме, энергию электронов на стационарных орбитах и выразил постоянную Ридберга через основные константы.
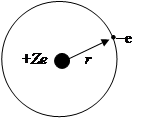
Радиусы электронных орбит: 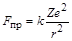 – сила кулоновского притяжения; k = 1/4pe0; Z – заряд ядра; e0 = 8.85×10-12 Кл/Н×м2 – электрическая постоянная; е = 1.6×10-19 Кл – единичный электрический заряд (заряд электрона)
– сила кулоновского притяжения; k = 1/4pe0; Z – заряд ядра; e0 = 8.85×10-12 Кл/Н×м2 – электрическая постоянная; е = 1.6×10-19 Кл – единичный электрический заряд (заряд электрона) 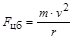 – центробежная сила;
– центробежная сила; 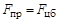 ;
; 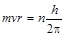 – постулат Бора;
– постулат Бора; 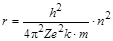 – радиусы орбит электрона; n = 1,2,3... – квантовое число.
– радиусы орбит электрона; n = 1,2,3... – квантовое число.
Радиус первой (n=1) стационарной орбиты электрона для атома водорода (Z=1) составляет величину:
r1 = h2/4p2e2mk= 5,29×10-11 м = 0,53 Å
и называется «радиус первой боровской орбиты».
Энергия электрона: 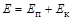 – полная энергия электрона;
– полная энергия электрона; 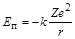 – потенциальная энергия электрона;
– потенциальная энергия электрона; 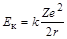 – кинетическая энергия электрона;
– кинетическая энергия электрона; 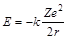 – полная энергия электрона;
– полная энергия электрона; 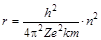 – радиус орбит электронов;
– радиус орбит электронов; 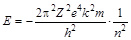 .
.
Электрон, находящийся на первой стационарной орбите (n=1) атома водорода (Z=1), будет обладать энергией
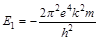 =–2,17×10-18 Дж=– 13,6 эВ.
=–2,17×10-18 Дж=– 13,6 эВ.
Отрицательное значение энергии свидетельствует о том, что электрон связан с ядром и для его удаления из атома необходимо затратить энергию (потенциальная энергия электрона равна нулю на бесконечном удалении его от ядра). Чтобы перевести электрон на более удаленную стационарную орбиту, нужно затратить энергию. При переводе электрона на бесконечно большое расстояние от ядра необходимо затратить энергию, называемую энергией ионизации (Eи). Численное значение энергии электрона в основном состоянии совпадает с экспериментально определенным значением энергии ионизации. При переходе электрона с более удаленной стационарной орбиты на менее удаленную энергия выделяется в виде квантов электромагнитного излучения.
Необходимо отметить, что квантовое число n определяет в известном смысле энергию электрона и радиус орбит, по которым двигается электрон, обладающий соответствующей энергией. Набор стационарных орбит электрона может быть представлен в виде набора энергетических состояний (уровней) – рис. 1.1.
 |
Рис. 1.1. Диаграмма энергетических состояний электрона в атоме водорода: n – главное квантовое число; Еi – энергия электрона на i орбите; hnij=Ei-Ej – квант электромагнитного излучения
Теория Бора сыграла положительную роль, открыв дорогу квантовой механике. Основное ее достоинство заключалось в количественном описании линейчатых спектров простейших атомов. С усовершенствованием приборов и техники спектроскопии обнаружилось, что линии, принимавшиеся за единичные, в действительности состоят из нескольких близко расположенных друг к другу линий. Следовательно, для каждого квантового числа, скорее всего, существует несколько близких друг к другу энергетических уровней. Потребовалось введение дополнительных квантовых чисел, получить которые из теории Бора непосредственно было невозможно. До некоторой степени эти противоречия разрешил Арнольд Зоммерфельд (Sommerfeld), который допустил существование в атоме эллиптических орбит. Было введено еще два дополнительных квантовых числа: побочное и магнитное. Однако в целом необходимо констатировать, что в рамках классической физики не удалось создать "хорошую" модель описания поведения микрочастиц. Основным недостатком теории Бора для химии явилась невозможность дать качественное и тем более количественное описание химической связи.
Корпускулярно-волновой дуализм свойств электрона, как и других микрообъектов, является первым фундаментальным положением, на котором строится волновая механика – механика, применимая для описания объектов атомных и субатомных размеров.
Принцип неопределенности
Вторым фундаментальным положением, на котором строится волновая механика, является принцип неопределенности Гейзенберга. Поскольку электрон обнаруживает одновременно свойства волны и частицы, возникают трудности, связанные с измерением корпускулярных свойств электрона, а именно одновременного определения координат и импульса электрона.
Вернер Гейзенберг (Heisenberg) в 1927 г. сформулировал следующее положение: для микрочастицы невозможно одновременно точно определить ее координаты и импульс. Ограничения в точности определения даются соотношением Гейзенберга:
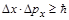 ,
, 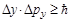 ,
, 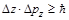 ,
, 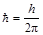 – постоянная Планка.
– постоянная Планка.
Из принципа неопределенности следует вероятностный подход к описанию механики микрообъектов. Точное определение координат частицы и ее импульса заменяется определением вероятности нахождения частицы в какой-то области пространства.Для движущейся частицы с вполне определенной энергией, а следовательно, импульсом мы не можем указать точные значения координат (траектории движения), а можем говорить лишь о вероятности нахождения ее в какой-либо части пространства.
Вероятностный характер механики микрочастиц следует также из опытов по дифракции электронов. Если пропускать не поток электронов, а последовательно по одному, то каждый электрон попадет в какое-то определенное место экрана и дифракционной картины не будет (от одного электрона). В какое конкретное место попадет следующий электрон, мы не знаем, но знаем, где вероятность его появления максимальна и где минимальна. И только большое число электронов, пропущенных последовательно друг за другом, создадут на экране дифракционную картину.
Энергетическое состояние электрона в кулоновском поле ядра достаточно близко соответствует ситуации нахождения электрона в трехмерном потенциальном ящике. Поэтому все закономерности, которые были получены, а главное дискретность энергетических состояний, распространяются и на атом.
Электронная орбиталь
Наиболее наглядно вероятность нахождения электрона в пространстве характеризует функция распределения электронной плотности (вероятность нахождения электрона в элементарном объеме пространства). Для атома водорода таким элементарным объемом пространства является сферический слой толщиной dr (рис.1.8), а зависимость вероятности нахождения электрона в нем от расстояния до ядра – функция радиального распределения электронной плотности.
Вероятность нахождения электрона в элементарном сферическом слое
dP = Y2×dV = Y2×4pr2dr.
Радиальное распределение электронной плотности– зависимость плотности вероятности ( 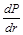 ) от радиуса – равно:
) от радиуса – равно:
s(r) = 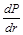 = Y2×4pr2 =
= Y2×4pr2 = 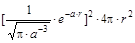 .
.
Вероятность нахождения электрона в сфере радиусом r
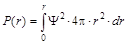 .
.
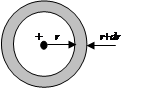 |
Рис. 1.8. Элементарный сферический слой: dV = 4pr2dr - объем сферического слоя
Какие выводы можно сделать из функции радиального распределения электронной плотности для основного состояния атома водорода (рис. 1.9)?
|
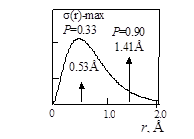
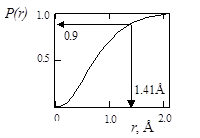
Рис. 1.9. Радиальное распределение электронной плотности - s(r). Вероятность нахождения электрона в сфере радиусом r - [Р(r)].
1. Функция s(r) имеет максимум при r = 1/a = 0,53 Å. На этом расстоянии от ядра максимальна вероятность нахождения электрона. Необходимо отметить, что это расстояние совпадает с радиусом первой орбиты по теории Бора. Оно находится из условия равенства нулю первой производной функции радиального распределения:
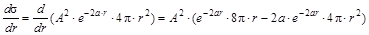 ,
,
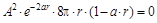 ,
, 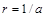 .
.
2. Функция радиального распределения – вероятность нахождения электрона в элементарном объеме пространства – асимптотически стремится к нулю при увеличении расстояния от ядра (при r®¥ s(r)®0), но не становится равной нулю. При этом вероятность нахождения электрона в сфере Р(r) с увеличением радиуса сферы асимптотически приближается к единице, но не становится равной единице ни на каком расстоянии. Поэтому точно указать объем пространства, в котором вероятность нахождения электрона равна единице, невозможно, как невозможно и указать, в какой точке пространства находится электрон в данный момент. Поэтому указывается объем пространства, в пределах которого вероятность нахождения электрона составляет величину 0,9 (90%). Данная область пространства называется орбиталью электрона, в отличие от орбиты в классической теории. Для основного состояния атома водорода радиус орбитали составляет величину r =1,41Å.
Многоэлектронные атомы
В случае многоэлектронного атома (число электронов два и более) получить точные решения уравнения Шредингера невозможно (сложно), поскольку необходимо учитывать энергию взаимодействия электронов не только с ядром, но и между собой. Поэтому при определении волновых функций и энергетических состояний используют приближенные методы. В частности, при описании системы рассматривают движение одного электрона в эффективном поле, которое образуется полем ядра и полем остальных электронов. При этом используют понятие эффективного заряда ядра.
Эффективный заряд ядра (Zэ) равен заряду ядра (Z) за вычетом константы экранирования (s) –постоянной величины, учитывающей влияние остальных электронов атома на рассматриваемый электрон: Zэ = Z - s. При таком приближенном рассмотрении состояние электрона описывается волновыми функциями, подобными тем, которые были получены для атома водорода. Увеличение заряда ядра и различия в радиальном распределении электронной плотности для электронов, находящихся на различных орбиталях, приводят к изменению энергии орбиталей по сравнению с атомом водорода. Отличия заключаются в следующем.
1. Увеличение заряда ядра приводит к возрастанию энергии притяжения электрона к ядру и соответственно к понижению энергии электронной орбитали (рис. 1.16).
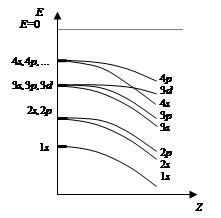 |
2. Вследствие различного радиального распределения электронной плотности s, p, d, f-электронов величина константы экранирования зависит не только от числа электронов, создающих эффективный заряд ядра, но и от типа орбиталей, которые они занимают (sn,l). Понижение энергии орбиталей с ростом заряда ядра (для одного значения n) различно для s, p, d, f-состояний, что приводит к снятию вырождения по орбитальному квантовому числу.
Рис. 1.16. Схема изменения энергии орбиталей в зависимости от Z
3. Вследствие снятия вырождения по орбитальному квантовому числу энергия электрона определяется не только главным квантовым числом n, но и орбитальным l.
Пример. Константа экранирования (s) и эффективный заряд ядра (Zэ) атомов для первых 11 элементов периодической таблицы:
| Атом | H | He | Li | Be | B | C | N | O | F | Ne | Na |
| Z | |||||||||||
| s | 0,3 | 1,70 | 2,05 | 2,40 | 2,75 | 3,10 | 3,45 | 3,80 | 4,15 | 8,80 | |
| Zэ=Z-s | 1,7 | 1,30 | 1,95 | 2,60 | 3,25 | 3,90 | 4,55 | 5,20 | 5,85 | 2,20 |
Энергия орбитали 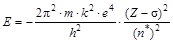 ,
,
Z – s = Zэ – эффективный заряд ядра; n* – эффективное главное квантовое число, s; Zэ; n* вычисляются по правилам, разработанным Слэтером (Slater).
Таким образом получается последовательность энергетических состояний в многоэлектронном атоме (стационарные состояния реально существующих атомов):
E1s<E2s<E2p<E3s<E3p<E4s<E3d<E4p<E5s<E4d<E5p<E6s<E4f<…
 Эту последовательность можно проиллюстрировать энергетической диаграммой электронных орбиталей многоэлектронного атома с определенным значением Z (рис. 1.17). Диаграмма показывает энергетическое положение орбиталей относительно друг друга в атоме с определенным зарядом ядра Z, но не их абсолютные значения.
Эту последовательность можно проиллюстрировать энергетической диаграммой электронных орбиталей многоэлектронного атома с определенным значением Z (рис. 1.17). Диаграмма показывает энергетическое положение орбиталей относительно друг друга в атоме с определенным зарядом ядра Z, но не их абсолютные значения.
Рис. 1.17. Диаграмма энергетических состояний невозбужденного многоэлектронного атома
Каждый последующий атом в периодической системе отличается от предыдущего тем, что заряд его ядра увеличивается на единицу и соответственно на единицу увеличивается число электронов. Каждому электрону должно соответствовать свое энергетическое состояние, которое описывается четырьмя квантовыми числами. В изолированных многоэлектронных атомах энергетические состояния электронов вырождены по магнитному и спиновому квантовому числу. В электромагнитном поле (внешнее поле или поле окружающих атомов) это вырождение может сниматься (рис. 1.18).
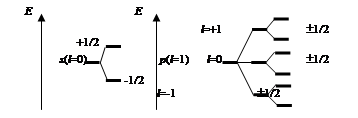 |
Рис. 1.18. Схема снятия вырождения для s и р энергетических состояний
в электромагнитное поле
ХИМИЧЕСКАЯ СВЯЗЬ
Отдельные атомы химических элементов, не взаимодействующие друг с другом, в природе практически не встречаются. Как правило, мы имеем дело с более или менее устойчивыми образованиями, состоящими из двух и более одинаковых или различных атомов. Это молекулы, сложные радикалы и ионы, входящие в состав газообразных, жидких и твердых веществ. В этом случае говорят, что между атомами существует химическая связь. Какие силы при этом действуют, что обеспечивает устойчивость образовавшихся частиц – эти вопросы решаются теорией химической связи.
Атомы будут объединяться, образовывая устойчивые системы, в случае если при этом будет происходить понижение полной энергии многоатомной системы по сравнению с энергией изолированных атомов. Например, условием образования молекулы АВ из атомов А и В является
ЕАВ < ЕА + ЕВ, DЕ = ЕАВ – (ЕА + ЕВ) < 0,
где ЕА, ЕВ – полная энергия изолированных атомов, ЕАВ – энергия молекулы, DЕ – суммарное изменение энергии системы при образовании молекулы.
Химическая связь обусловлена наличием сил притяжения и отталкивания, удерживающих атомы на определенном расстоянии друг от друга. Атомы содержат отрицательно (электроны) и положительно заряженные (ядра) частицы. Следовательно, природа этих сил обусловлена взаимодействием зарядов (носит электромагнитный характер). Образование химической связи происходит в результате взаимодействия электронных оболочек и ядер атомов и сопровождается уменьшением полной энергии системы. При этом существенно не изменяется электронное строение атомов – сохраняются ядра атомов и общая структура электронных оболочек. В основе образования химической связи лежит перераспределение электронной плотности внешних электронов атомов. В зависимости от характера этого перераспределения используют различные модели описания химических связей.
Типы химической связи
Химическая связь возникает в результате взаимодействия электронных оболочек, при этом происходит перераспределение электронной плотности при сохранении в целом структуры отдельных атомов. Основную роль в изменение энергии системы при образовании химической связи играют электроны внешних уровней (валентные электроны). Поэтому в большинстве случаев ограничиваются описанием именно их состояния. В зависимости от характера перераспределения валентных электронов для описания химической связи используют различные модели. Как правило, различают три основных типа химической связи: ковалентную, ионную, металлическую.
Ковалентная связь образуется при обобществлении валентных электронов. Для определения параметров связи необходимо решать уравнение Шредингера. В случае если рассматривается химическая связь между одинаковыми атомами (разность электроотрицательностей DcАВ=0), электронная плотность в равной степени принадлежит обоим атомам, следовательно, эффективный заряд на атомах d = 0– ковалентная неполярная связь. При DcАВ¹0 происходит сдвиг электронной плотности в сторону атома с большим значением электроотрицательности – поляризация связи, на атомах возникают эффективные заряды, равные по величине, но противоположные по знаку – ковалентная полярная связь. Атом с большим значением электроотрицательности приобретает заряд d < 0, с меньшим – d > 0; чем больше разница в электроотрицательностях (DcАВ), тем больше величина возникающего заряда.
