Общие закономерности реакционной способности органических соединений
120. Электрофильные реагенты – это:
1) частицы, являющиеся донором пары электронов;
2) частицы, являющиеся акцептором пары электронов;
3) катионы;
4) атомы благородных газов;
5) галогенид-ионы.
121. Возрастание реакционной способности молекул в реакциях электрофильного замещения происходит в ряду:
1) бензол, толуол, хлорбензол, анилин
2) бензол, нитробензол, бензальдегид
3) фенол, п-нитрофенол, бензальдегид, толуол
4) бензойная кислота, бензол, фенол, п-гидроксифенол
5) фуран, бензол, анилин, пиридин.
122. Какие частицы являются электрофильными реагентами:
1) Н+;
2) SO3;
3) FeBr3;
4) Br-;
5) СН2=СН2.
123. Какие частицы являются электрофильными реагентами:
1) НО-;
2) AlCl3;
3) Br+;
4) F-;
5) ZnCl2.
124. Уменьшение реакционной способности молекул в реакциях электрофильного замещения происходит в ряду:
1) имидазол, пиррол, пиридин
2) пиррол, имидазол, пиридин
3) пиридин, пиррол, пиримидин
4) пиримидин, имидазол, пиррол
5) пиридин, бензол, пиррол.
125. Какие частицы являются нуклеофильными реагентами:
1) НО×;
2) Н2О;
3) Н2S;
4) НО-;
5) NH3.
126. Какие частицы являются нуклеофильными реагентами:
1) CН3ОН;
2) СН2=СН2;
3) I- ;
4) NO2+;
5) Н- .
127. Нуклеофил – это частица, которая:
1) присоединяет протон
2) атакует положительно заряженный атом углерода
3) поставляет пару электронов для образования химической связи
4) поставляет свободную орбиталь для образования химической связи
5) присоединяет электроны.
128. Радикальными реагентами являются:
1) катионы, имеющие на внешнем слое только спаренные электроны;
2) анионы;
3) атомы, имеющие неспаренный электроны;
4) атомы, имеющие на внешнем слое октет электронов;
5) группировки атомов, имеющие неспаренный электрон.
129. По механизму радикального замещения (SR) протекают реакции:
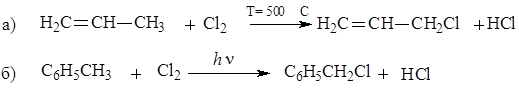
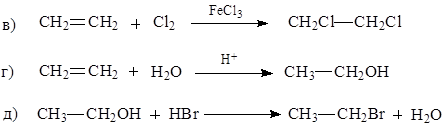
1) а,б;
2) б,в;
3) в,г;
4) г,д;
5) а,д.
130. Электрофил – это частица:
1) способная к образованию связи с нуклеофилом
2) способная к образованию связи со свободным радикалом
3) акцептор электронной пары
4) донор электронной пары
5) донор электрона.
131. Статистическая вероятность образования 1,1-дихлорэтана в реакции хлора с хлорэтаном составляет:
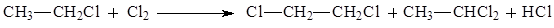
1) 20%;
2) 30%;
3) 40%;
4) 50%;
5) 60%.
132. Укажите нуклеофильные частицы:
1) NO2+
2) H-
3) H+
4) RO-
5) Н3О+.
133. Статистическая вероятность образования 1,2-дихлорэтана в реакции хлора с хлорэтаном составляет:
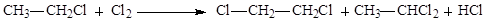
1) 20%;
2) 30%;
3) 40%;
4) 50%;
5) 60%.
134. Статистическая вероятность образования 2-метил-1-хлорбутана в реакции хлора с 2-метилбутаном составляет:
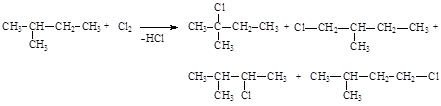
1) 10%;
2) 15%;
3) 20%;
4) 25%;
5) 50%.
135. Статистическая вероятность образования 2-метил-3-хлорбутана в реакции хлора с 2-метилбутаном составляет:
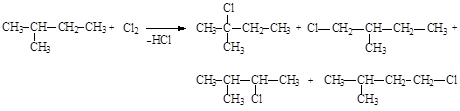
1) 6,67%;
2) 8,33%;
3) 16,67%;
4) 21,33%;
5) 33,33%.
136. Укажите электрофильные реагенты:
1) НS-
2) Cl+
3) R-C+=O
4) CH2-CH3+
5) Н+.
137. Статистическая вероятность образования 2-метил-2-хлорбутана в реакции хлора с 2-метилбутаном составляет:
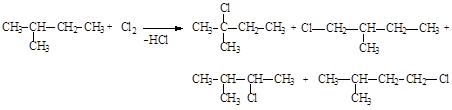
1) 6,67%;
2) 8,33%;
3) 16,67%;
4) 21,33%;
5) 33,33%.
138. Статистическая вероятность образования 3-метил-1-хлорбутана в реакции хлора с 2-метилбутаном составляет:
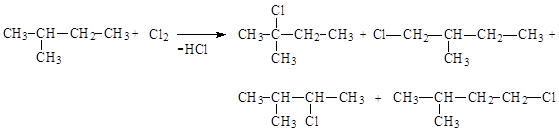
1) 10%;
2) 15%;
3) 20%;
4) 25%;
5) 50%.
139. Статистическая вероятность образования 2-хлорпропана в реакции хлора с пропаном составляет:
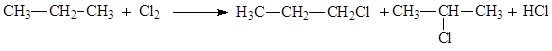
1) 20%;
2) 25%;
3) 50%;
4) 75%;
5) 80%..
140. Статистическая вероятность образования 1-хлорпропана в реакции хлора с пропаном составляет:
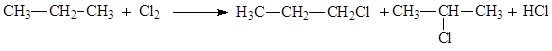
1) 20%;
2) 25%;
3) 50%;
4) 75%;
5) 80%.
141. Свободные радикалы:
1) являются электроноизбыточной системой
2) являются электронодефицитной системой
3) стабилизируются электронодонорами
4) образуются в полярных растворителях
5) стабилизируются электроноакцепторами.
142. Справедливы утверждения о том, что изопропил-радикал:
1) электронодефицитен
2) содержит sp2-гибридный атом углерода
3) менее стабилен, чем н-пропил радикал
4) способен отщеплять атом хлора у молекулы хлора
5) содержит sp-гибридизированнный атом углерода.
143. Для реакции этилбензола с бромом (реакция SR, схема приведена ниже) выберите справедливое(ые) утверждение(ия):
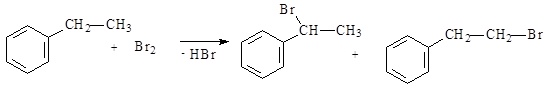
1) преимущественно образуется 1-бром-1-фенилэтан;
2) преимущественно образуется 1-бром-2-фенилэтан;
3) главный продукт образуется из радикала бензильного типа;
4) главный продукт образуется из первичного радикала;
5) главный продукт обладает оптической активностью.
144. При бромировании 2-метилбутана на стадии образования монобромпроизводного в качестве главного продукта образуется:
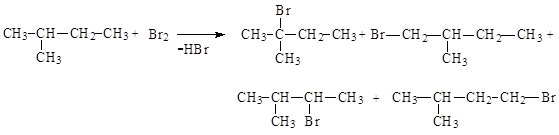
1) смесь монобромпроизводных в равных количествах;
2) 2-бром-2-метилбутан;
3) 1-бром-2-метилбутан;
4) 2-бром-3-метилбутан;
5) 1-бром-3-метилбутан.
145. Справедливы утверждения о том, что карбокатион:
1) электронодефицитен
2) содержит атом углерода с положительным зарядом
3) стабилизируется электроноакцепторами
4) образуется при гомолитическом разрыве ковалентных связей
5) дестабилизируется электронодонорами.
146. Справедливы утверждения о том, что карбанион:
1) содержит атом углерода с одним неспаренным электроном
2) содержит атом углерода с отрицательным зарядом
3) содержит атом углерода в sp2-гибридизированном состоянии
4) образуется при гетеролитическом разрыве ковалентной связи
5) образуется при гомолитическом разрыве связи.
147. Ориентанты второго рода содержат молекулы:
1) бензойной кислоты;
2) фенола;
3) толуола;
4) нитробензола;
5) хлорбензола.
148. Ориентанты первого рода содержат молекулы:
1) нитробензола;
2) анилина;
3) фенола;
4) этилбензола;
5) салициловой кислоты.
149. Для каких соединений возможно электрофильное присоединение?
1) пропан
2) циклогексен
3) 2-бромбутан
4) бутен-2-овая кислота
5) метан.
150. Из перечисленных молекул более высокую реакционную способность в реакциях электрофильного замещения (SE), чем бензол, проявляют:
1) этилбензол;
2) фторбензол;
3) нитробензол;
4) анилин;
5) фуран.
151. По механизму радикального замещения будут протекать реакции:
1) СН3–СН2–СН2–Сl + Cl2 →
2) СН2=СН2+Вr2 →AlCl3
3) C6H5-CH3 + Br2 hv→
4) C6H5-CH3 + Br2 →AlBr3
152. Из перечисленных молекул более высокую реакционную способность чем бензол в реакциях электрофильного замещения (SE) проявляют:
1) хлорбензол;
2) кумол;
3) бензойная кислота;
4) фенол;
5) пиррол.
153. Из перечисленных молекул наименьшую реакционную способность в реакциях электрофильного замещения (SE) проявляет:
1) этилбензол;
2) пиридин;
3) толуол;
4) бензол;
5) анилин.
154. Какие утверждения верны? При бромировании этилена:
1) электрофилом является Br–
2) электрофилом является Br+
3) электрофил атакует атом углерода
4) электрофил атакует π-связь.
155. Какие утверждения верны? В реакциях электрофильного присоединения алкенов образование π-комплекса сопровождается:
1) разрушением π-связи
2) взаимодействием электронодефицитной частицы с π-связью
3) переходом атома углерода из sp2 в sp3 гибридное состояние
4) образованием карбокатиона.
156. При гидратации бутена-1 в качестве главного продукта образуется:
1) бутанол-1;
2) бутанол-2;
3) бутандиол-1,2;
4) бутан;
5) бутанлиол-2,3.
157. Наибольшую реакционную способность при взаимодействии с HBr проявляет:
1) этилен;
2) пропилен;
3) 2-метилпропен;
4) акролеин;
5) 3,3,3-трифторпропен.
158. Какие утверждения верны? В реакциях электрофильного присоединения алкенов образование σ-комплекса сопровождается:
1) разрушением π-связи
2) образованием σ-связи
3) образованием карбокатиона
4) образованием карбаниона.
159. Возрастание реакционной способности молекул в реакциях галогенирования происходит в ряду:
1) пропеновая кислота, 2-метилпропен, пропен
2) пропен, 2-метилпропен, пропеновая кислота
3) пропеновая кислота, пропен, 2-метилпропен
4) 2-метилпропен, пропен, пропеновая кислота.
160. По механизму нуклеофильного присоединения (AN ) протекают реакции:
1) гидратация пропилена;
2) гидролиз этилацетата;
3) присоединение синильной кислоты к ацетону;
4) присоединение брома к бутадиену-1,3;
5) альдольная конденсация.
161. В результате взаимодействия 2-хлорбутана со спиртовым раствором щелочи в качестве главного продукта образуется:
1) бутанол-1;
2) бутен-1;
3) бутен-2;
4) бутадиен-1,3;
5) бутанол-2.
162. Какие утверждения верны? Согласно правилу Марковникова:
1) при присоединении к несимметричному алкену атом водорода реагента присоединяется к наиболее гидрогенизированному атому углерода при двойной связи
2) из двух возможных карбокатионов быстрее образуется карбокатион с наибольшей энергией
3) АЕ-присоединение протекает через стадию образования наиболее стабильного карбокатиона
4) бромирование этилена протекает региоселективно.
163. По механизму электрофильного присоединения протекают реакции:
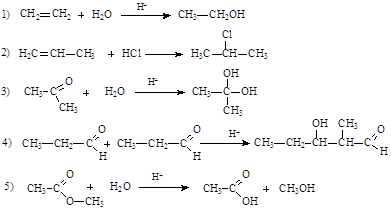
164. По механизму бимолекулярного нуклеофильного замещения (SN2) протекают реакции:
а) СН3-СН2-Cl + NaOH(спирт.р-р) ®; б) СН3-СН2-Cl + NaOH(водный р-р)®; в) СН3ОН + HBr ®; г) СН3-СН2-Cl +NH3®.
1) а,б;
2) б,в;
3) в,г;
4) а,г;
5) б,в,г.
165. Какие реакции протекают против правила Марковникова?
1) гидратация пропена
2) гидратация пропеновой кислоты
3) гидролиз хлорэтана
4) гидрирование циклогексена
5) гидрогалогенирование пропена.
166. По механизму электрофильного присоединения протекают реакции:
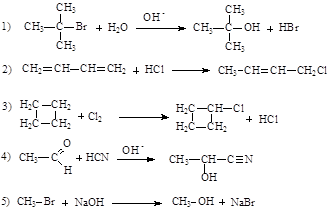
167. В результате дегидратации бутанола-2 в качестве главного продукта образуется:
1) бутанол-1;
2) бутен-1;
3) бутен-2;
4) бутадиен-1,3;
5) бутин-2.
168. Соединения, способные бромироваться по механизму электрофильного замещения:
1) толуол
2) индол
3) нитробензол
4) циклогексанол
5) пропен.
169. Какие утверждения верны? В реакциях электрофильного замещения:
1) образование π-комплекса не лимитирует скорость реакции
2) образование σ-комплекса лимитирует скорость реакции
3) π-комплекс не ароматичен
4) σ-комплекс ароматичен
5) реакция идет с участием свободных радикалов.
170. В результате гидрирования 1 моль водорода бутадиена-1,3 в качестве главного продукта при обычных условиях образуется:
1) бутен-1;
2) бутен-2;
3) бутан;
4) бутанол-2;
5) бутин-1.
171. Хлорангидрид уксусной кислоты может быть получен в результате взаимодействия:
1) СН3-СН2-ОН + SOCl2 ®;
2) СН3-СООН +Cl2 ®;
3) СН3-СООН + SOCl2 ®;
4) СН3СООС2Н5 + HCl®;
5) СН3СН2СООН + SOCl2 ®.
172. По механизму мономолекулярного нуклеофильного замещения (SN1) протекает реакция:
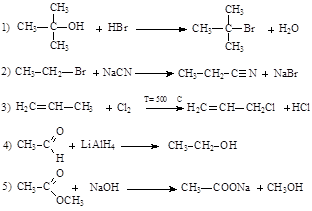
173. В каких условиях протекание реакций электрофильного замещения невозможно?
1) С6Н6 + Br2 → hυ
2) С6Н5 – NH2 + CH3 – Cl →AlCl3
3) CH3 – C6H5 + CH3 -CH3 →
4) C6H6 + CH3COCl AlCl3 →
174. К заместителям орто- и пара-ориентантам, имеющимся в бензольном ядре, относятся группы:
1) –СОН
2) –ОН
3) –Cl
4) -С3Н7 .
175. Хлорэтан образуется в результате реакций:
1) СН2=СН2 + Cl2 ®;
2) СН3-СН2-ОН + SOCl2 ®;
3) СН2=СН2 + HCl ®;
4) СН3-СН2-ОН + HCl ®;
5) СН3-СН2-ОН + NaCl ® .
176. К заместителям мета-ориентантам в бензольном ядре относятся группы:
1) – СН3
2) –NH2
3) –COR
4) –SO3H
5) -ОН.
177. Какие заместители дезактивируют бензольное кольцо, являясь орто- и пара-ориентантами?
1) –CНO
2) –F
3) –NH2
4) –NH CH3
5) –NH2.
178. 1-хлорпропан образуется в результате реакции:
1) СН3-СН=СН2 + HCl ®;
2) СН3-СН2-СН2-ОН +SOCl2 ®;
3) СН3-СООН + SOCl2 ®;
4) СН3-СН2-СН2-ОН + HCl ®;
5) СН3-СН=СН2 + Cl2 ®.
179. Пропаналь образуется в результате:
1) окисления трет-бутилового спирта;
2) окисления пропанола-2;
3) окисления пропанола-1;
4) гидратации пропина;
5) восстановления пропанона-2.
180. Реакционная способность молекул в реакциях электрофильного замещения увеличивается в ряду:
1) бензол, фенол, пиррол, пиридин
2) пиридин, бензол, фенол, пиррол
3) пиррол, бензол, пиридин, фенол
4) фенол, пиррол, бензол, пиридин.
181. В галоформную реакцию вступают:
1) бутанон;
2) пентанон-3;
3) этаналь;
4) метаналь;
5) пентанон-2.
182 .Качественной реакцией на многоатомные спирты является их взаимодействие с:
1) аммиачным раствором оксида серебра (I);
2) азотной кислотой;
3) бромной водой;
4) гидроксидом меди(II);
5) металлическим натрием.
183. Какие реакции являются окислительно-восстановительными:
1) СН2=СН2 +Н2 ®;
2) СН2=СН2 + КМnO4 +Н2О ®;
3) СН3-СН2-ОН +HВr®;
4) СН3-СН3 +Cl2 ®;
5) СН2=СН2 +Н2О2 ®;.
184. Ацилирующими агентами являются:
1) (СН3СО)2О;
2) СН3-СО-SКоА;
3) СН3СНО;
4) СН3СН2ОН;
5) С6Н5СН2ОН.
185. Какие утверждения неверны?
1) реакция нуклеофильного замещения у насыщенного атома углерода осуществляется только тогда, когда уходящий нуклеофил стабильнее вступающего в молекулу
2) реакция нуклеофильного замещения у насыщенного атома углерода осуществляется только тогда, когда уходящий нуклеофил менее стабилен, чем вступающий в молекулу
3) анионы более сильные нуклеофилы, чем соответствующие им молекулы
4) в водном растворе нуклеофильность аниона тем больше, чем больше его радиус.
Реакции ацилирования протекают по механизму:
1) электрофильного замещения;
2) нуклеофильного присоединения;
3) нуклеофильного замещения;
4) радикального замещения;
5) электрофильного присоединения.
187. В водном растворе нуклеофильность ионов возрастает в порядке:
1) F- < Cl- < Br- < I-
2) F- > Cl- = Br- = I-
3) I- > Br- > Cl- > F-
4) Br- > Cl- > F- > I-
188. Какие утверждения верны?
1) сильные основания являются хорошо уходящими группами
2) сильные основания бывают плохо уходящими группами
3) слабые основания – хорошо уходящие группы
4) слабые основания плохо уходящие группы.
189. Какие утверждения верны?
1) SN2–реакции характерны для первичного электрофильного атома углерода
2) SN2 –реакции протекают с обращением конфигурации
3) скорость SN2 –реакций пропорциональна концентрации субстрата, и не зависит от концентрации нуклеофила
4) скорость SN2 –реакции имеет второй суммарный порядок.
190. Какие реакции не осуществляются?
1) Br– + CH3OH → CH3Br + OH–
2) Br– + CH3 – CH3 → CH3Br + CH3–
3) HBr+ CH3OH → CH3Br + HOH
4) NH3 + CH3 – CH2I → [CH3 – CH2NH3]+ I-
191. Укажите признаки мономолекулярного нуклеофильного замещения у ненасыщенного атома углерода:
1) образование связи с нуклеофилом и разрыв связи с уходящей группой происходят одновременно (согласованно)
2) отрыв уходящей группы и присоединение нуклеофила протекает в две стадии
3) образуется промежуточное соединение – карбокатион
4) скорость реакции не зависит от концентрации нуклеофила.
192. В схемах каких реакций содержатся ошибки?
1) (CH3)3C – Br + NaOH → CH3-CH2- CH2-CH2-OH + NaBr
водный раствор
2) CH3-CHBr-CH2-CH3 + NaOH → CH3-CH=CH-CH3 + NaBr + H2O
спиртовой раствор
3) CH3-CH2 -CH2-CH2Br + NaOH → CH3–CH=CH-CH3 + NaBr + H2O
спиртовой раствор
Н2SO4, t
4) (CH3)2-CH-CH(OH)-CH3 → (CH3)2C=CH-CH3 + H2O
193. Какой из альдегидов наименее активен в реакциях нуклеофильного присоединения?
1) трихлоруксусный
2) уксусный
3) муравьиный
4) 2-метилпропионовый.
194. Какое из соединений наименее активно в АN-реакциях?
1) СН3СН2СНО
2) СН3СНО
3) СН3СОСН3
4) С2Н5СОСН3
195. Для каких соединений характерна иодоформная проба?
1) С3Н7СНО
2) НСНО
3) СН3СОС2Н5
4) СН3СНО
196. Какие соединения подвергаются альдольной конденсации при обработке водным раствором щёлочи?
1) СН3СОСН3
2) СН3СНО
3) (СН3)3ССНО
4) СН3СН2СНО
197. Продукт альдольной конденсации пропаналя:
1) пропановая кислота
2) 2-метил-3-гидроксипентаналь
3) 3-метил-3-гидроксипентаналь
4) пропанол-1
198. В каких схемах содержатся ошибки?
1) СН3СНО + Н2О Н+→ С2Н5ОН
2) СН3СНО + СН3ОН Н+ → СН3СН(ОН)СН3
3) СН3СНО + С2Н5-SН → СН3-SН + С2Н5СНО
4) С6Н5СНО + СН3NН2 → С6Н5СН=N-СН3
199. Какие превращения соответствуют диспропорционированию?
1) 2СН3ОН → СН3ОСН3 + Н2О
2) СН3СНО + Н2 → СН3СН2ОН
3) 2НСНО → НСООН + СН3ОН
4) 2С6Н5СНО → С6Н5СООН + С6Н5СН2ОН
200. В каком ряду стабильность карбоксилат-анионов уменьшается?
1) СН3СН2СОО- > НСОО-СОО- > НООС-СН2-СОО-
2) СН3СН2СОО- > НООС-СН2-СОО- > НСОО-СОО-
3) НСОО-СОО- > НООС-СН2-СОО- > СН3СН2СОО-
4) НООС-СН2-СОО- > НСОО-СОО- > СН3СН2СОО-
201. Какие из реакций протекают по СН- кислотному центру у карбоновых кислот?
1) СН3-СООН + С2Н5ОН →
2) СН3-СООН + PCl5 →
3) СН3-CH2-СООН + Cl2 →
4) СН3-СООН + NН3 →
202. Между какими парами веществ возможны реакции нуклеофильного замещения?
1) С2Н5-СООН + СН3ОН Н+ →
2) СН3СОСl + 2NН3 →
3) СН3СОО-СН3 + Н2О ОН– →
4) С6Н5–СООН + Br2 →
203. Реакции ацилирования – это - реакции
1) электрофильного присоединения
2) электрофильного замещения
3) нуклеофильного присоединения
4) нуклеофильного замещения.
204. Какие из соединений являются ацилирующими агентами?
1) СН3-CОSKоA
2) R-CHO
3) (R-CO)2O
4) RCOONa
205. Ацилирующая способность реагентов убывает в ряду:
1) R-COOH > (RCO)2O > RCOCl
2) R-CO-Cl > (RCO)2O > R-COOН
3) R-CO-NH2 > (RCO)2O > R-CO-Cl
4) (RCO)2O >R-CO-Сl > R-CO-OH
206. Наибольшей ацилирующей способностью обладает:
1) (СН3СО)2О;
2) СН3СООС2Н5;
3) СН3СОNH2;
4) СН3СОСl;
5) СН3СООNa.
