Часть II. Приготовление раствора заданной молярной концентрации
Для приготовления раствора с определенной молярной концентрацией рассчитывают массу вещества, соответствующую указанному числу молей, взвешивают и помещают в мерную колбу нужного объема. Колбу заполняют дистиллированной водой до метки.
Оборудование: Реактивы:
Весы Гидроксид натрия (NaОН)
Мерная колба 0,2л Дистиллированная вода
Воронка
Стакан
Шпатель
Задание. Рассчитать массу гидроксида натрия, необходимую для приготовления 0,2 л 0,1 молярного раствора и приготовить указанный раствор.
Расчет:
Дано: Решение:
Vраствора= v(X)= C(X) Vраствора
C(NaOH)= m(X) = v(X) M(X)
Найти:
m(NaOH)
Ответ:
Выполнение опыта:
- Взвесить рассчитанную массу гидроксида натрия с точностью до 0,01г в предварительно взвешенном стакане.
- Через воронку всыпать навеску в мерную колбу на 0,2л.
- Налить немного дистиллированной воды в стакан, где взвешивалась щелочь и тщательно смыть остатки сухой щелочи со стенок воронки в мерную колбу (как вы думаете, зачем нужна эта операция?).
- Держа мерную колбу за горлышко, круговыми движениями перемешать содержимое до растворения щелочи.
- Аккуратно доливая дистиллированную воду, довести уровень раствора в мерной колбе до метки.
- Закрыть колбу пробкой и тщательно перемешать раствор.
Расчет и последовательность ваших действий занести в бланк отчета.
Отчет
Практическое работа
Способы выражения концентрации растворов
Приготовление растворов определенной концентрации
Выполнил студент…………..…………………….
фамилия, инициалы
Группа №……….
Цель работы:……………………………………………………………………….
………………………………………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………
Вариант №………
Часть I. Приготовление раствора с заданной массовой долей вещества.
Задание.
Рассчитать массы хлорида натрия и воды, необходимые для приготовления 200г. 4% раствора и приготовить указанный раствор.
Расчет:
Дано: Решение:
Найти
Ответ:
Выполнение опыта:
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
Часть II. Приготовление раствора заданной молярной концентрации
Задание.Рассчитать массу гидроксида натрия, необходимую для приготовления 0,2 л 0,1 молярного раствора и приготовить указанный раствор.
Расчет:
Дано: Решение:
Ответ:
Выполнение опыта:
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
……………………………………………………………………………..
Выводы:
……………………………………………………………………………..
Урок 22
Электролиты и электролитическая диссоциация
Хорошо известно, что одни вещества в растворенном или расплавленном состоянии проводят электрический ток, другие в тех же условиях ток не проводят. По электрической проводимости растворов или расплавов все вещества делят на электролиты и неэлектролиты.
Электролиты
Электролитами называют вещества, которые в расплавах или в растворах при взаимодействии с растворителем распадаются на ионы (диссоциируют).
Ионы
– это заряженные частицы, образованные из одного или нескольких атомов. Положительно заряженные ионы называют катионами, отрицательно заряженные – анионами.
Важным понятием теории электролитической диссоциации является понятие о степени диссоциации.
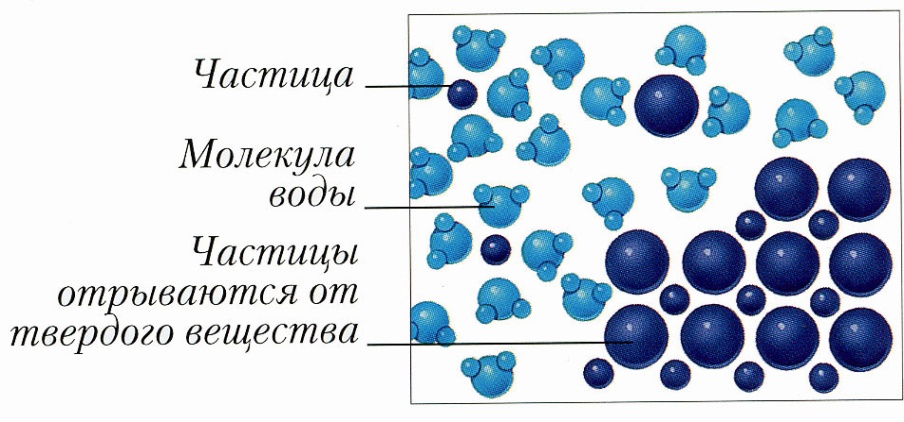 Электролитическая диссоциация
Электролитическая диссоциация
– это процесс распада электролита на ионы при растворении в воде или расплавлении.
Степень диссоциации α
– это отношение числа молекул, распавшихся на ионы (n), к общему числу растворенных молекул (N).
α = n/N
Степень диссоциации α может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация). Степень диссоциации часто выражают в процентах.
Электролиты со степенью диссоциации больше 30% называют сильными, со значениями α от 3 до 30% – средними , менее 3% – слабыми электролитами.
Растворы сильных электролитов в результате полной диссоциации содержат в основном ионы, а растворы слабых электролитов содержат в основном нераспавшиеся (недиссоциированные) молекулы и небольшую часть ионов.
К сильным электролитам относят:
а) практически все растворимые соли;
б) кислоты: H2SO4, HNO3, HCl, HBr, HI, HClO4, HMnO4 и некоторые другие;
в) растворимые основания (щелочи) – гидроксиды металлов IA и IIA групп периодической системы.
К слабым электролитам относят остальные кислоты и основания, воду и другие вещества.
При диссоциации молекулы электролитов (кислот, солей, оснований) распадаются на положительно заряженные ионы, называемые катионами и отрицательно заряженные ионы, называемые анионами. Катионы и анионы в растворе химически связаны с молекулами воды – гидратированы, но для простоты написания уравнений электролитической диссоциации в них обычно гидратацию не показывают.
Кислоты
Диссоциация кислот:
HCl 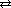 H+ + Cl-
H+ + Cl-
HNO3 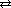 H+ + NO3-
H+ + NO3-
Диссоциация многоосновных кислот происходит ступенчато:
первая ступень H2S 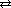 H+ + HS-
H+ + HS-
вторая ступень HS- 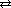 H+ + S2-
H+ + S2-
Из уравнений диссоциации видно, что общим для всех кислот является присутствие в растворе катионов водорода(H+).
Кислоты –
это электролиты, при диссоциации которых в качестве катионов образуются только ионы водорода(H+).
Именно катионы водорода обусловливают общие свойства всех кислот: кислый вкус, изменение окраски индикаторов, взаимодействие с металлами, основными оксидами, основаниями.
Основания
Диссоциация оснований:
NaOH D Na+ + OH-
KOH D K+ + OH-
Диссоциация многокислотных оснований происходит ступенчато:
первая ступень Ba(OH)2 D BaOH+ + OH-
вторая ступень BaOH+ D Ba+ + OH-
Из уравнений диссоциации видно, что общим для всех оснований является присутствие в растворе гидроксид-ионов(OH-).
Основания
– это электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы(OH-).
Именно гидроксид-ионы обусловливают общие свойства всех оснований:
изменение окраски индикаторов (для растворимых оснований – щелочей), взаимодействие с кислотными оксидами, с кислотами, с растворами солей.
Соли
Диссоциация солей:
NaCl " Na+ + Cl-
K2CO3 " 2K+ + CO32-
Диссоциация практически всех растворимых солей происходит сразу, полностью и необратимо. Таким образом, соли являются сильными электролитами. Общих ионов для разных солей в растворе нет.
Соли
– это сильные электролиты, при диссоциации которых образуются катионы металлов и анионы кислотных остатков.
Гидролиз солей
Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого образуется слабый электролит.
Гидролиз соли – это разновидность ионообменной реакции. Реакция протекает в направлении, обратном реакции нейтрализации. Поэтому при гидролизе соли образуются кислота (или кислая соль) и основание (или основная соль), и обычно среда раствора становится соответственно щелочной или кислой. Будет ли соль подвергаться гидролизу и какое значение рН приобретет раствор, можно определить, зная силу кислот и оснований, которыми образована соль.
К сильным электролитам относят: а) практически все растворимые соли; б) кислоты: H2SO4, HNO3, HCl, HBr, HI, HClO4, HClO3, HMnO4, HCrO3; в) растворимые основания (щелочи) – гидроксиды металлов IA и IB групп периодической системы:
KOH, NaOH, LiOH, Ba(OH)2, Ca(OH)2. К слабым электролитам относят остальные кислоты и основания, воду и другие вещества.
Соли, образованные сильным основанием и сильной кислотой, гидролизу не подвергаются (KCl, Na2SO4, Ba(NO3)2 и др.). Среда водного раствора остается нейтральной.
Если растворимая соль содержит хотя бы один ион слабого электролита (основания, кислоты), то такая соль обязательно подвергается гидролизу; характер среды при этом соответствует более сильному электролиту, образовавшему соль. То есть соль сильного основания и слабой кислоты дает щелочную среду, рН > 7 (Na2CO3, K2SO3, (CH3COO)2Ba и др.); соль слабого основания и сильной кислоты дает кислую среду, рН < 7 (AlCl3, Zn(NO3)2, CuSO4 и др.). Если оба электролита слабые, то в зависимости от того, какой из них сильнее, среда становится слабокислой, нейтральной или слабощелочной.
Напишем уравнения гидролиза. Обычно уравнения гидролиза записывают в трех формах: сокращенной ионной, ионной и молекулярной. Удобнее начинать с сокращенной ионной формы, которая отражает сущность процесса гидролиза – взаимодействие ионов соли с водой. Необходимо помнить, что в реакции участвуют ион слабого электролита и одна молекула воды (H+OH-).
1. Соли, образованные слабым основанием и сильной кислотой
хлорид аммония NH4Cl
NH4+ + H2O D NH4OH + H+
NH4+ + Cl- + H2O D NH4OH + H+ + Cl-
NH4Cl + H2O D NH4OH + HCl
хлорид алюминия AlCl3
Al3+ + H2O D AlOH2+ + H+
Al3+ + 3Cl- + H2O D AlOH2+ + H+ + 3Cl-
AlCl3 + H2O D AlOHCl2 + HCl
Обычно реакция гидролиза с участием многозарядного иона протекает по более сложной схеме, включающей несколько стадий. Об этом следует помнить, но нет необходимости писать остальные стадии, так как первая достаточно полно характеризует процесс: образование иона Н+ указывает на кислую среду раствора, осадок Al(OH)3 не образуется, потому что гидролиз протекает преимущественно по первой стадии.
2.Соли, образованные сильным основанием и слабой кислотой
цианид калия KCN
CN- + H2O D HCN + OH-
K+ + CN- + H2O D HCN + K+ + OH-
KCN + H2O D HCN + KOH
сульфит калия K2SO3
SO32- + H2O D HSO3- + OH-
2K+ + SO32- + H2O D 2K+ + HSO3- + OH-
K2SO3 + H2O D KHSO3 + KOH
Наличие ионов ОН- указывает на щелочную среду раствора
3. Соли, образованные слабым основанием и слабой кислотой
ацетат аммония.CH3COONH4
CH3COO- + NH4+ + H2O D CH3COOH + NH4OH
CH3COONH4 + H2O D CH3COOH + NH4OH
Раствор в данном случае имеет нейтральную среду, так как степени
диссоциации продуктов гидролиза примерно равны.
Многие соли, образованные многозарядными (двух-, трехзарядными) ионами слабых оснований и слабых кислот, подвергаются полному необратимому гидролизу. В таблице растворимости для таких солей указывается прочерк.
карбонат алюминия
Al2(CO3)3 + 3H2O = 2Al(OH)3$ + 3CO2#
MgS +2H2O = Mg(OH)2$ + H2S#
Вопросы для самопроверки
6. Что называют процессом электролитической диссоциации?
7. Почему соли, кислоты и основания в водных растворах диссоциируют на ионы?
8. Исходя из теории электролитической диссоциации, дайте определения понятиям кислота, основание, соль.
9. Какие электролиты называют сильными, какие слабыми? Приведите примеры.
Урок 23
Реакции ионного обмена
Реакции ионного обмена
– это реакции в растворах электролитов, при которых ионы одного вещества обмениваются с ионами другого вещества.
В реакциях ионного обмена наряду с растворимыми сильными электролитами участвуют (образуются или расходуются) нерастворимые вещества, газы, малодиссоциированные соединения (слабые электролиты). Уравнения ионообменных реакций записывают в трех формах:
1) молекулярной
2) полной ионной
3) сокращенной ионной.
В качестве примера составим уравнение для реакции между растворами нитрата бария и сульфата натрия.
Молекулярное уравнение
Ba(NO3)2 + Na2SO4 = BaSO4$ + 2NaNO3
Полное ионное уравнение
Ba2+ + 2NO3-+ 2Na+ + SO42- = BaSO4$ + 2Na+ + 2NO3-
Сокращенное ионное уравнение
Ba2+ + SO42- = BaSO4$
При составлении ионных уравнений сильные растворимые электролиты записывают в виде ионов: катионов (положительно заряженных ионов) и анионов (отрицательно заряженных ионов). Нерастворимые вещества, газы и слабые электролиты записывают в виде молекул. Внимательно изучите таблицу растворимости – она не только подскажет, какие вещества нерастворимы, но и поможет вам правильно определить заряды катионов и анионов для сильных электролитов.
Сокращенное ионное уравнение наиболее ясно выражает сущность реакции. В нашем примере видно, что реакция свелась к образованию нерастворимого вещества (осадка) сульфата бария.
Реакции в растворах электролитов практически необратимы и идут до конца в случаях, когда образуется: а) осадок, б) газ, в) слабый электролит.
Примеры уравнений реакций с образованием осадка
Взаимодействие растворов кислоты и соли
H2SO4 + Pb(NO3)2 = PbSO4$ + 2HNO3
Pb2+ + SO42- = PbSO4$
Взаимодействие растворов сильного основания (щелочи) и соли
2NaOH +MgSO4 = Mg(OH)2$ + Na2SO4
Mg2+ + 2OH- = Mg(OH)2$
Взаимодействие газа (кислотного оксида) с сильным основанием
SO2 + Ca(OH)2 = CaSO3$ + H2O
SO2 + Ca2+ + 2OH- = CaSO3$ + H2O
 Взаимодействие растворов двух солей (на рисунке)
Взаимодействие растворов двух солей (на рисунке)
Pb(NO3)2 + 2KI = 2KNO3 + PbI2$
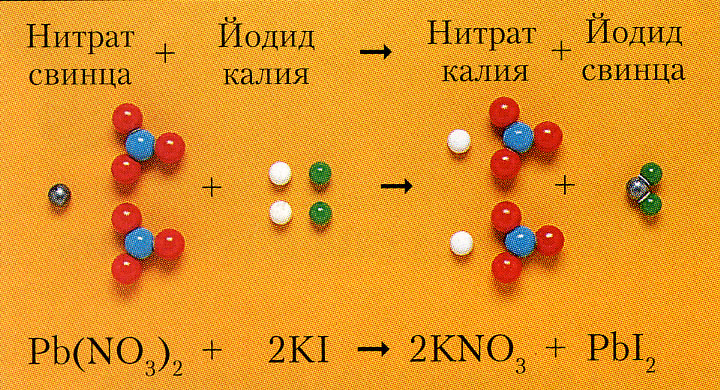 Pb + + 2I- = PbI2$
Pb + + 2I- = PbI2$
Примеры уравнений реакций с образованием газа
Взаимодействие кислоты и соли
H2SO4 + K2SO3 = K2SO4 + H2O + SO2#
2H+ + SO32- = H2O + SO2#
Взаимодействие сильного основания и соли
NaOH + NH4NO3 = NaNO3 + NH3# + H2O
NH4+ + OH- = NH3# +H2O
Примеры уравнений реакций с образованием слабого электролита
Реакция нейтрализации
2NaOH + H2SO4 = Na2SO4 + 2H2O
OH- + H+ = H2O
Взаимодействие нерастворимого основания и кислоты
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + H2O
Образование слабой кислоты
2NaCH3COO + H2SO4 = Na2SO4 + CH3COOH
CH3COO- + H+ = CH3COOH
Вопросы для самопроверки
1. Какие реакции называют ионообменными? В каких случаях они идут до конца?
2. В каких формах записывают уравнения РИО? Приведите примеры.
Урок 24.
