Карбоновые кислоты Сложные эфиры. Строение, свойства, применение
Карбоновые кислоты — это органические соединения, молекулы которых содержат карбоксильную группу -СООН, связанную с углеводородным радикалом.
Строение
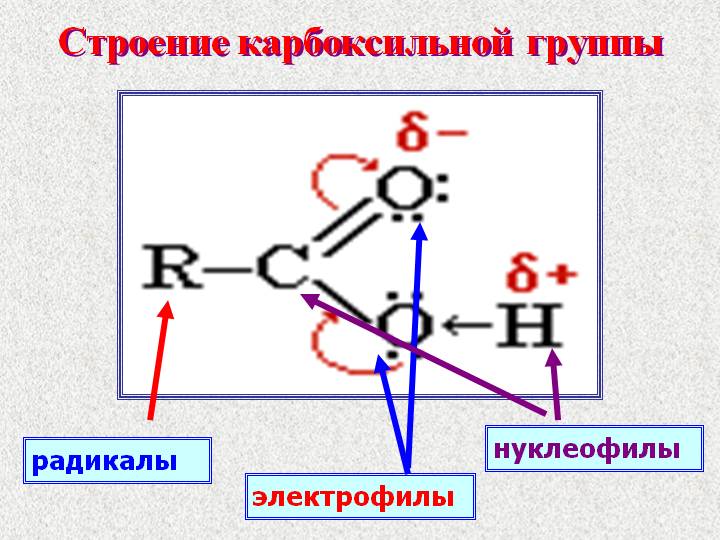
Физические свойства карбоновых кислот.
Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде и их плотность уменьшаются, а температура кипения повышается. Высшие кислоты, начиная с н-нонановой СН3-(СН2)7-СООН, — твердые вещества, без запаха, нерастворимые в воде. Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота.
Химические свойства карбоновых кислот.
Карбоновые кислоты содержат сильно полярную связь между атомами кислорода и водорода в гидроксильной группе, которая еще больше поляризуется под влиянием атома кислорода, входящего в состав карбонильной группы.
1). В водном растворе карбоновые кислоты обратимо диссоциируют:
RCOOH 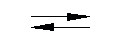 RCOO- + Н+
RCOO- + Н+
Лакмус в растворе карбоновых кислот приобретает красный цвет.
Карбоновые кислоты — слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей.
2). Реагируют с
- активными металлами
2RCOOH + Mg → (RCOO)2 Mg+Н2
- основными оксидами
2RCOOH + СаО → (RCOO)2 Са+Н2О
- основаниями
RCOOH + NаОH → RCOONа+Н2О
- солями слабых кислот
RCOOH + NаHCО3 → RCOONа+Н2О+CО2
3). Взаимодействуют со спиртами:
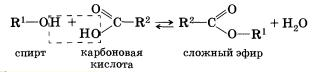
4).При действии галогенов на свету образуются галогензамещенные кислоты :
hν
СH3-CH2-COOH + Br2 → CH3-CHBr-COOH + HBr
Альдегиды
Альдегиды — это органические вещества, в молекулах которых углеводородный радикал связан с особой группой атомов — альдегидной группой:
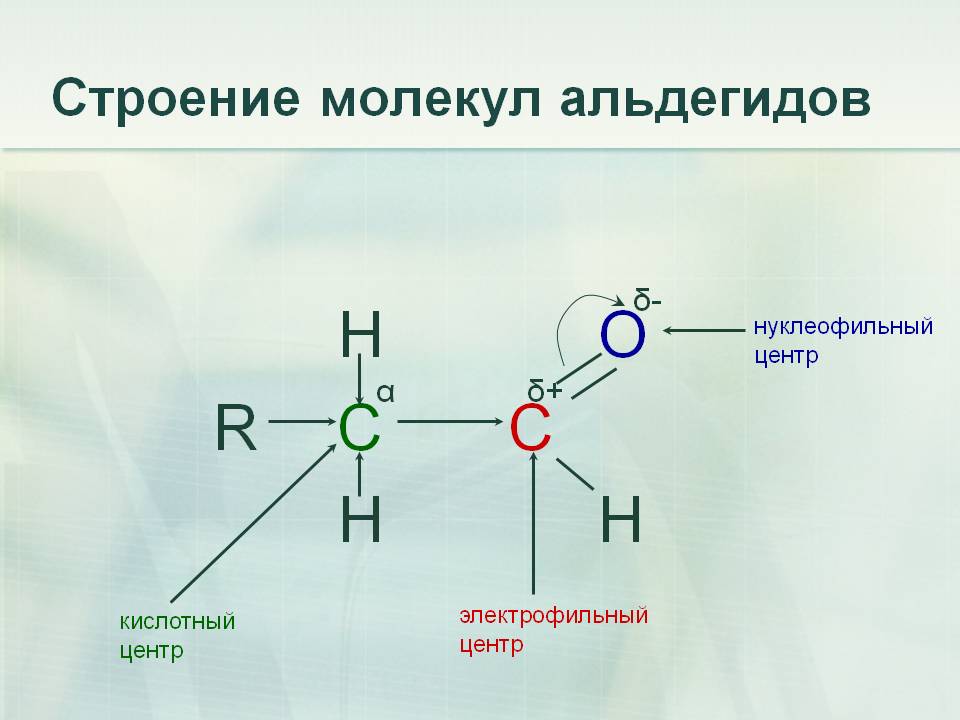
Начинает гомологический ряд альдегидов не уксусный альдегид (другое его название этаналь), а муравьиный альдегид, у которого с альдегидной группой связан не радикал, а атом водорода.
Другие названия муравьиного альдегида — метаналь, формальдегид.
Названия «муравьиный альдегид», «уксусный альдегид» — это исторически сложившиеся, так называемые тривиальные названия, которые широко еще используются в органической химии. По рекомендуемой к применению международной системе названий органических веществ названия альдегидов, как вы уже, наверное, догадались, строятся из названия соответствующего углеводорода (с тем же числом атомов углерода) с добавлением суффикса -аль.
Муравьиный альдегид — бесцветный газ с резким специфическим запахом. Хорошо растворяется в воде. Водный раствор формальдегида носит название формалина (обычно применяют 40% -ный раствор).
Формальдегид ядовит. Он вызывает воспаление слизистых оболочек глаз и дыхательных путей, возможны явления острого отравления организма. В качестве противоядия пострадавшему дают белок сырого яйца, слизистые отвары, промывают желудок раствором питьевой соды или уксуснокислого натрия.
В медицине формальдегид применяют только в виде разбавленных растворов в качестве дезинфицирующего и дезодорирующего средства: для обмывания кожи при повышенной потливости, для дезинфекции инструментов (в виде 0,5% растворов).
Дезинфицирующее свойство формалина обусловлено его способностью соединяться с белковыми веществами с образованием нерастворимых соединений, вследствие чего погибают микроорганизмы, в клетках которых содержатся белковые вещества. Это же свойство положено в основу сохранения биологических и анатомических препаратов.
Громадные количества формальдегида расходуются для получения пластических масс, изделия из которых широко применяются в технике и быту.
Уксусный альдегид - бесцветная легколетучая жидкость с запахом прелых яблок. Хорошо растворим в воде. Применяется для получения уксусной кислоты.
Альдегиды легко отличить от других органических веществ с помощью красивой реакции «серебряного зеркала».
Еще одна характерная реакция на альдегиды — это взаимодействие с гидроксидом меди(II).
В результате этих реакций альдегиды окисляются: муравьиный альдегид до муравьиной кислоты, уксусный альдегид до уксусной кислоты. В общем виде уравнение реакции, проделанной в первом опыте, можно записать так:
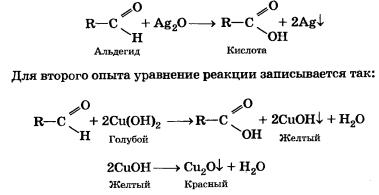
Таким образом, основные классы органических соединений производятся из углеводородов путем последовательных превращений: предельный углеводород непредельный углеводород спирт —> альдегид —> кислота.
Урок 12
Лабораторная работа
