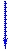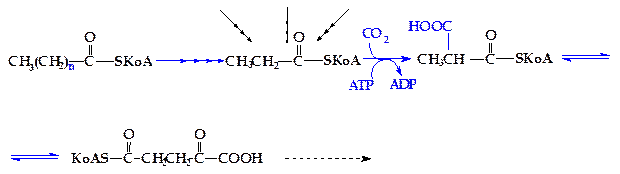Исходными веществами для биосинтеза молекул ДНК служат дезокси-
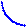
Рисунок 4.12 - Катаболизм пуриновых оснований
       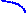    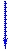  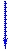  Рисунок 4.13 - Катаболизм пиримидиновых оснований | рибонуклеозид-5'-трифосфаты, а специфическое расположение нуклеотидных остатков в молекулах ДНК обеспечивается взаимодействием комплементарных оснований, принадлежащих, с одной стороны, полинуклеотидной матрице, а с другой — нуклеозидтрифосфатам. Аналогично идет специфический биосинтез РНК из рибонуклеозидтрифосфатов на ДНК-матрице.
Из трех основных частей нуклеотида (азотистого основания, фосфорной кислоты и пентозы) фосфорная кислота всегда присутствует в клетках, рибоза образуется при распаде углеводов, и только гетероциклическое основание создается специфическим путем.
Пути синтеза пуриновых и пиримидиновых оснований различны. Но есть некоторые сходные черты в механизмах синтеза пуринового и пиримидинового циклов:
использование глицина, аспарагина и глутамина в качестве источников азота гетероциклических колец;
включение в состав пуриновых и пиримидиновых циклов атомов углерода углекислого газа и муравьиной кислоты;
построение пуринового основания и завершение синтеза пиримидинового основания на рибозо-5-фосфате, в результате чего конечными продуктами биосинтеза являются сразу нуклеозид-5'-фосфаты;
ферментативный характер всех реакций, осуществляющихся в процессе синтеза нуклеотидов;
возникновение на определенном этапе биосинтеза общих предшественников (инозин-5'-монофосфата — для пуриновых нуклеотидов, уридин-5'-монофосфата — для пиримидиновых).
Как видно на схеме, два атома азота пуринового кольца происходят из амидной группы глутамина, третий атом азота — из аспартата (аспарагиновой кислоты) и, наконец, четвертый — из глицина. Четвертый и пятый атомы углерода также происходят из глицина. Таким образом, молекула глицина дает три атома. Второй и восьмой атомы углерода происходят из формиата (муравьиной кислоты), а шестой атом углерода — из СО
2:






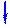



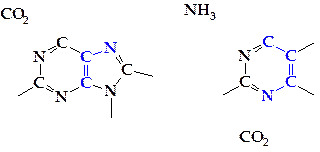
Формирование пуринового кольца сразу идет на рибозо-5-фосфате, и в результате последовательных реакций наращивания пуринового цикла образуется инозин-5'-монофосфат (ИМФ) — ключевое соединение в синтезе пуриновых нуклеотидов. Инозин-5'-фосфат способен окисляться в ксантозин-5'-фосфат.
В результате аминирования инозин-5'-монофосфата синтезируется аденозин-5'-монофосфат (АМФ), а из АМФ при восстановлении — дезоксиаденозин-5'-монофосфат (dАМФ). Ксантозин-5'-монофосфат (КМФ) превращается в гуанозин-5'-монофосфат (ГМФ) путем аминирования.
В процессе синтеза пиримидиновых оснований один атом азота цикла пиримидина происходит из аммиака, атом углерода — из углекислого газа, а второй атом азота и остальные атомы углерода — из аспарагиновой кислоты. В результате последовательных реакций наращивания пиримидинового цикла при дальнейшем участии фосфорилированной рибозы образуется уридин-5'-монофосфат (УМФ) — ключевое соединение в биосинтезе пиримидиновых нуклеотидов.
Уридин-5'-монофосфат далее превращается в цитидин-5'-мо-нофосфат (ЦМФ), а также в дезоксиуридин-5'-монофосфат (dУМФ) и дезокситимидин-5'-монофосфат (dТМФ).
Пуриновые и пиримидиновые нуклеозид-5'-монофосфаты (НМФ и dНМФ) превращаются в макроэргические нуклеозид-5'-дифосфаты (НДФ и dНДФ), которые далее переходят в богатые энергией нуклеозид-5'-трифосфаты (НТФ и dНТФ). Процессы фосфорилирования нуклеотидов идут при их взаимодействии с универсальным источником энергии АТФ при участии специфических фосфотрансфераз (киназ).
Синтез дезоксирибонуклеозид-5'-трифосфатов (dНТФ) осуществляется посредством реакции восстановления рибозы по гидроксильной группе при втором углеродном атоме. Эта реакция свойственна как нуклеозидмонофосфатам, так и нуклеозиддифосфатам.
Биосинтез всех дезоксирибонуклеозид-5'-трифосфатов и рибонуклеозид-5'-трифосфатов регулируется в клетке таким образом, что они возникают зависимо друг от друга в строго определенных соотношениях.
ОБМЕН ЛИПИДОВ
Жиры — основной источник энергии в организме. Жиры значительно превосходят по энергетической ценности углеводы и в значительных количествах могут запасаться в качестве «резервного топлива».
Характерным структурным компонентом большинства липидов являются высшие жирные кислоты. В состав жиров чаще всего входят кислоты с 16— 18 атомами углерода, среди них имеются насыщенные и ненасыщенные высшие жирные кислоты.
КАТАБОЛИЗМ ЛИПИДОВ
Распад жиров (триглицеридов) начинается с их гидролиза, в результате чего образуются глицерин и высшие жирные кислоты. Гидролиз триглицеридов, входящих в состав пищи, у высших животных происходит преимущественно в тонком кишечнике и катализируется липолитическими ферментами — панкреатическими липазами, вырабатываемыми поджелудочной железой.
Эти ферменты бывают двух типов: одни из них специфичны в отношении эфирных связей в a-положении триглицерида, другие гидролизуют связи в b-положении.
Полный гидролиз триглицеридов идет ступенчато: сначала быстро гидролизуются a-связи, а потом уже идет медленный гидролиз b-моноглицерида:
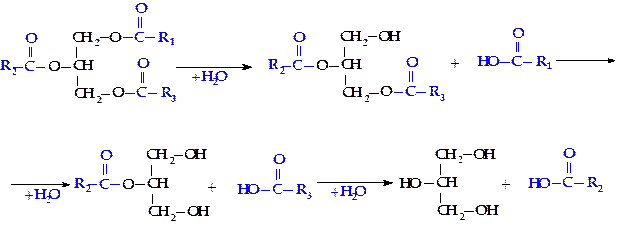
Глицерин независимо от того, поступит ли он на ресинтез жиров или будет претерпевать дальнейший распад, прежде всего фосфорилируется. Донором остатка фосфорной кислоты в этой реакции служит АТФ. Образующийся фосфоглицерин в основном расходуется на синтез новых молекул триглицеридов, но часть его окисляется с образованием диоксиацетонфосфата.
Диоксиацетонфосфат изомеризуется в 3-фосфоглицериновый альдегид, который затем вступает в обменные реакции.
Высшие жирные кислоты распадаются преимущественно путем b-окисления, получившего такое название потому, что в молекуле жирной кислоты оксиление протекает по b-углеродному атому, при этом от кислоты отщепляется двууглеродный фрагмент. Ненасыщенные высшие жирные кислоты (олеиновая, линолевая, линоленовая и др.) предварительно восстанавливаются до предельных кислот. Окисление предельных высших жирных кислот осуществляется ступенчато. Все реакции многостадийного окисления ускоряются специфическими ферментами. b-Окисление высших жирных кислот у млекопитающих происходит во многих тканях, в первую очередь в печени, почках и сердце.
Первым этапом b-окисления высших жирных кислот является их активирование путем образования соединения с коэнзимом А (HS-КоА). Эта реакция протекает в цитоплазме с использованием энергии АТФ и приводит к образованию ацилкоэнзима А (ацил-SКоА). Взаимодействие высших жирных кислот с коэнзимом А ускоряется специфическими лигазами — ацил-SКоА-синтетазами:
С17Н35-СООН + HS-KoA + АТФ ¾¾¾® С17Н35-СО~ S-KoA + АМФ + ФФн
Вторая стадия распада высших жирных кислот состоит в окислении ацилкоэнзима А при посредстве ацил-SКоА-дегидрогеназы, содержащей ФАД+ в качестве кофермента (рисунок 4.14, реакция 1).
Третья стадия окисления высших жирных кислот состоит в присоединении молекулы воды (гидратация) по месту двойной связи дегидроацил-КоА. Эта реакция ускоряется соответствующими гидролиазами (еноил-SКоА-гидратазами) (реакция 2).
Четвертая стадия распада высших жирных кислот заключается в их новом окислении путем отнятия двух атомов водорода (дегидрирование) в b-положении по отношению к карбоксильной группе (реакция 3). Реакция катализируется оксидоредуктазой, но (в отличие от первой стадии окисления) с участием НАД+ в качестве кофермента.
Пятая стадия распада заключается в переносе b-кетоацил-SКоА-ацильной группировки на новую молекулу коэнзима А. Этот процесс ускоряется соответствующей ацилтрансферазой, называемой тиолазой, поскольку реакция по существу представляет расщепление связи -С—С- с присоединением по месту разрыва элементов HS-группы (тиолиз или тиолитическое расщепление) (реакция 4).
В результате описанных выше реакций молекула высшей жирной кислоты (стеариновой в рассматриваемом примере) укорачивается на два углеродных атома, и образуются пальмитиновая и уксусная кислоты в виде производных коэнзима А (пальмитил- и ацетил-SКоА). Этот процесс многократно повторяется. Так, пальмитил-SКоА снова дегидрируется, затем гидратируется, еще раз дегидрируется и расщепляется на С13Н27-CO~S-KoA и новую молекулу ацетил-SКоА. В свою очередь C13H27-CO~S-KoA дает С11Н23-CO~S-КоА и еще молекулу ацетил-SКоА и т.д. (рисунок 4.14).
Окончательным продуктом b-окисления высших жирных кислот в организме является ацетил-SКоА.

| -обозначает повторение реакций 1-4 | |




| тиолитическое расщепление | |
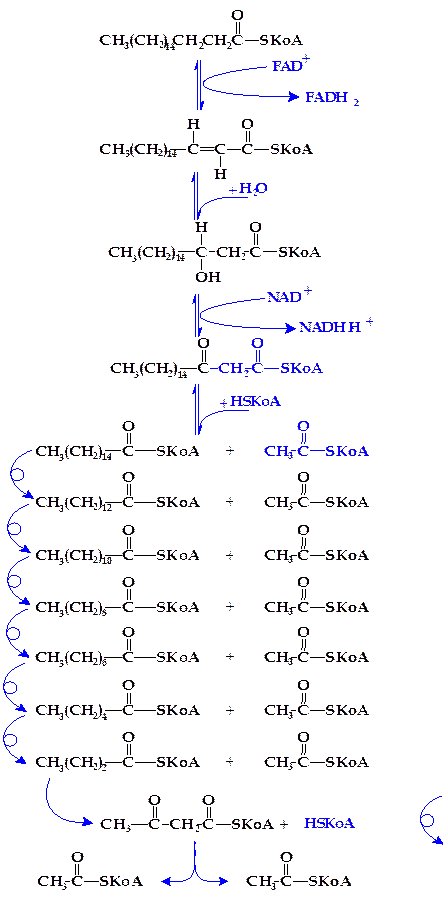
Рисунок 4.14 - Реакции b-окисления жирных кислот
(на примере стеариновай кислоты)
b-Окисление высших жирных кислот протекает в митохондриях, в липопротеидной мембране которых расположены ансамбли ферментов, обеспечивающих ряд индивидуальных реакций, составляющих процесс b-окисления. Поскольку в митохондриях локализованы также ферменты дыхательного цикла, ведущие передачу атомов водорода и электронов на кислород сопряженно с окислительным фосфорилированием, b-окисление высших жирных кислот является источником энергии для синтеза АТФ.
В процессе распада пальмитиновой кислоты проходит 7 циклов b-окисления, в каждом из которых образуются 5 молекул АТФ (посредством восстановленных ФАДН2 и НАДН.Н+).
При окислении пальмитата до ацетил-SКоА образуются 35 молекул АТФ. Восемь молекул ацетил-SКоА дают в результате полного сгорания в цикле Кребса 8 . 12 = 96 молекул АТФ. Одна молекула АТФ затрачивается на активирование пальмитата. Следовательно, энергетический эффект составляет 130 молекул АТФ.
Если бы ацетил-SКоА накапливался в организме, то запасы HS-КоА быстро исчерпались бы, и окисление высших жирных кислот остановилось. Этого не происходит, так как HS-КоА быстро освобождается из состава ацетил-SКоА в результате следующих процессов:
¾ ацетил-SКоА включается в ЦТК, где окисляется до СО2 и Н2О;
¾ ацетил-SКоА используется для синтеза полициклических спиртов (стеролов) и соединений, содержащих изопреноидные группировки;
¾ ацетил-SКоА является универсальным донором ацетильных групп для реакций ацетилирования (синтез ацетилхолина, N-ацетилглюкозамина и т.п.).
Основная масса природных липидов содержит жирные кислоты с четным числом атомов углерода. Однако в липидах растений инекоторых морских организмов присутствуют жирные кислоты с нечетным числом атомов углерода в цепи. Кроме того, у жвачных животных, в процессе переваривания углеводов в рубце образуется большое количество пропионовой кислоты, которая содержит три атома углерода. Жирные кислоты с нечетным числом атомов углерода окисляются таким же образом, что и кислоты с четным числом атомов, с той лишь разницей, что на последнем этапе b-окисления образуется одна молекула ацетил-SКоА и одна молекула пропионил-SКоА. Последний затем карбоксилируется и включается в дальнейшее окисление в форме сукцинил-SКоА (рисунок 4.15).
Расщепление ненасыщенных жирных кислот в ходе b-окисления происходит через дополнительные стадии гидратации по месту двойной связи между вторым и третим атомами углерода.
Обязательным условием в таком случае является наличие транс-двойной связи. В случае цис-изомера жирной кислоты необходим дополнительный фермент – цис-транс-изомераза. D-изомер, образующийся в ходе гидратации цис-связи, преобразуется ферментом эпимеразой в L-форму жирной кислоты. После таких преобразований цикл b-окисления продолжается как обычно (рисунок 4.16).
| катаболизм некоторых аминоксилот (триптофан, изолейцин, метионин) | |

| жирная кислота (n-нечетное число) | |
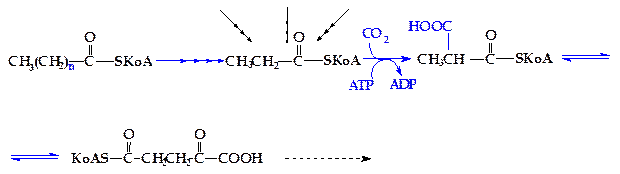
Рисунок 4.15 - b-Окисление жирных кислот с нечетным числом