Оксираны: получение, взаимодействие с водой, аммиаком и аминами, магнийорганическими соединениями.
Оксиранами(эпоксиды) называют трехчленные циклические соединения, содержащие один атом кислорода в цикле. Оксираны обладают высокой реакционной способностью в реакциях раскрытия трехчленного цикла под действием различных нуклеофильных агентов. ПОЛУЧЕНИЕ ОКСИРАНОВ Алкены окисляются перкислотами в неполярной среде с образованием эпоксидов.
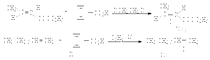
Простейший и наиболее важный из оксиранов - окись этилена получается в промышленности каталитическим окислением этилена.
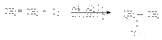
СВОЙСТВА ОКСИРАНОВ:
В отличии от простых эфиров для оксиранов характерны реакции расщепления напряженного трехчленного цикла под действием разнообразных нуклеофильных агентов. Это можно проиллюстрировать на примере раскрытия оксиранового кольца циклогексеноксида под действием гидроксид-иона с образованием исключительно транс-изомера 2-оксициклогексанола.
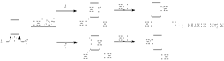
При наличии в оксирановом кольце алкильного или арильного заместителя атака нуклеофильного агента направляется преимущественно по незамещенному, пространственно более доступному атому углерода.
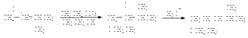
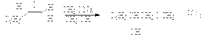
Механизм гидролиза и алкоголиза оксиранов может полностью измениться при проведении реакции в кислой среде или в присутствии электрофильного катализатора. В быстрой и обратимой первой стадии происходит протонирование оксирана по атому кислорода с образованием оксониевого катиона. Во второй медленной стадии протонированная форма подвергается нуклеофильной атаке водой, спиртом или галогенид-ионом. Протонирование оксирана ускоряет раскрытие кольца при взаимодействии с нуклеофильными агентами.
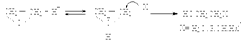
В зависимости от строения оксирана механизм расщепления трехчленного цикла может изменяться от SN2 до SN1. Если в результате раскрытия цикла образуется относительно устойчивый третичный карбокатион, катализируемый кислотой сольволиз оксирана протекает по SN1-механизму. Направление раскрытия оксиранового кольца при SN1-механизме полностью противоположно тому, которое наблюдается при SN2-механизме. Если реализуется SN1-механизм, нуклеофильная атака направляется по наиболее замещенному атому углерода. При конкуренции SN2 и SN1-механизмов раскрытие цикла не отличается высокой региоселективностью и приводит к образованию смеси двух изомерных продуктов сольволитического расщепления кольца оксирана.
Взаимодействие оксиранов с магнийорганическими соединениями следует рассматривать как бимолекулярное нуклеофильное замещение у насыщенного атома углерода оксирана под действием карбоаниона металлоорганического соединения. Раскрытию цикла способствует образование координационого донорно-акцепторного комплекса между атомами кислорода и магния, которое можно рассматривать как электрофильный катализ в реакции нуклеофильного замещения. Как следует из приведенного уравнения продуктами этой реакции являются спирты. Оксирановый цикл размыкается также под действием диалкилкупратов, причем замещение происходит при наименее замещенном атоме углерода.
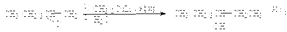
55. Краун-эфиры: комплексообразование с ионами металлов, применение.
КРАУН-ЭФИРЫ (краун-соединения), макрогетероциклические полиэфиры,содержащие несколько атомов кислорода в цикле, в названиях краун-эфиров первая цифра указывает на размер цикла, а вторая определяет число атомов кислорода в цикле.
Краун-эфиры образуют макроциклические комплексные соединения как с катионами, так и с нейтральными молекулами. В комплексах краун-эфира с катионами металлов (щелочных, щёлочноземельных и др.) катион включается во внутримолекулярную полость краун-эфира и удерживается там благодаря ион-дипольному взаимодействию с гетероатомами .Селективность связывания и устойчивость образуемых краун-эфиром комплексов зависит от ряда факторов – геометрического соответствия размеров внедряющейся частицы и полости макроцикла, природы растворителя, хелатного и макроциклических эффектов, заряда внедряющейся частицы, природы противоиона и пр. За счёт комплексообразования краун-эфиры повышают растворимость солей щелочных и щёлочноземельных металлов в малополярных растворителях; пример - образование малинового бензола и оранжевого бензола (окислительных реагентов) при растворении в бензоле соответственно KMnО4 или К2Cr2О7 в присутствии краун-эфира. Щелочные металлы в присутствии краун-эфира растворяются в координирующих органических растворителях; интенсивный синий цвет образующихся растворов объясняется присутствием в них сольватированной формы свободных электронов (получаемый раствор является восстановительным реагентом). Краун-эфиры способны селективно экстрагировать ионы металлов и некоторые органические соединения (амины, аминокислоты и др.) из водной фазы в органическую, энантиоспецифически связывать хиральные молекулы (в частности, протонированные формы аминокислот). За счёт влияния на ионную и субстратную проницаемость биологических мембран, на ферментные системы и другие биохимические процессы краун-эфиры проявляют различные виды биологической активности.
Краун-эфир широко используют в научных исследованиях как доступные и разнообразные модели при изучении сложных природных супрамолекулярных систем. С помощью краун-эфира можно избирательно выводить из организма ионы тяжёлых металлов или вводить малые количества нужных ионов или молекул. Краун-эфиры применяют для концентрирования, разделения, очистки и регенерации металлов, в том числе лантаноидов, для разделения нуклидов, энантиомеров; для создания ионоселективных датчиков и мембран; в межфазном катализе и для ускорения реакций, проходящих с участием анионов; как лекарственные препараты, пестициды, антидоты.
56. Тиолы. Кислотность тиолов. Нуклеофильные свойства тиолов, тиолятов и органических сульфидов. Окисление тиолов. Образование дисульфидов и их роль в биохимических процессах. Тио́лы (меркапта́ны) — сернистые аналоги спиртов общей формулы RSH, где R — углеводородный радикал, например, метантиол (метилмеркаптан) (CH3SH), этантиол (этилмеркаптан) (C2H5SH) и т. д. Тиолы в номенклатуре ИЮПАК имеют окончание тиол. Наиболее важным физическим свойством тиолов является отвратительный запах. Человеческий нос распознает запах тиола в концентрации 107-l0 8 моль/л (т.е. 1 мл тиола в 50 биллионах миллилитров воздуха), не доступной для многих спектральных и хроматографических методов. Тиолы в очень низкой концентрации вводят в природный гaз для того, чтобы поих запаху можно было определить утечки газа в помещении. Известный своим противным запахом хорек скунс выделяет два простых тиола: З-метил-1-бутантиол и 2-бутен-1-тиол. Тиолят-ионы являются более сильными нуклеофильными агентами, чем алкоголят-ионы, и скорость образования тиоэфиров в 103-104 раза превышает скорость реакции для их кислородных аналогов. Это позволяет осуществлять реакцию в мягких условиях. Метод межфазного катализа исключительно эффективен для синтеза сульфидов:

Сульфиды могут быть также получены в результате прямого взаимодействия сульфида натрия с двумя молями алкилирующего агента. Высокая нуклеофильность атома серы в сульфидах открывает возможность для получения солей сульфония в результате алкилирования сульфидов:
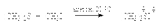
Окисление тиолов резко отличается от окисления спиртов. В зависимости от природы окислителя продуктами окисления тиолов являются дисульфиды R-S-S-R, сульфиновые RSO2H или сульфоновые RSO3H кислоты. При действии таких окислителей, как йод, бром, пероксид водорода, МпО3, тиолы окисляются до дисульфидов Дисульфиды легко восстанавливаются обратно до тиолов цинком в уксусной кислоте или лучше всего раствором щелочного металла в жидком аммиаке:
Сильные окислители - азотная кислота или перманганат калия - окисляют тиолы до сульфоновых кислот (продуктов исчерпывающего окисления органических соединений серы):
