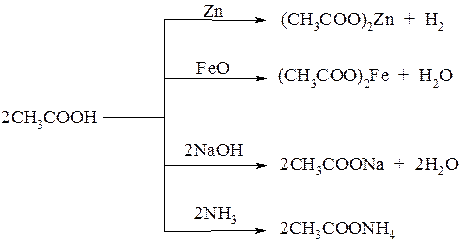Глава 17. Карбоновые кислоты и их функциональные производные
Карбоновые кислоты – это производные углеводородов, содержащие карбоксильную группу – СООН.
По числу карбоксильных групп различают монокарбоновые, дикарбоновые, трикарбоновые и т.д. По строению углеводородного радикала их классифицируют на алифатические, алициклические, ароматические и гетероциклические кислоты.
Гомологический ряд предельных одноосновных кислот имеет общую формулу CnH2n+1 COOH.
Способы получения
Некоторые способы получения карбоновых кислот были рассмотрены в предыдущих главах:
окисление алканов (разд. 5.3);
окисление алкенов (разд. 6.3.5);
окисление алкиларенов (разд. 10.3.5);
из первичных спиртов (разд. 12.3.4);
из альдегидов и кетонов (разд. 16.3.3);
галоформным расщеплением метилкарбонильных соединений (разд. 16.3.5).
Кроме перечисленных реакций большое значение имеют и приведённые ниже способы.
Реакции карбонилирования
Данный метод широко используют для промышленного получения карбоновых кислот (металлокомплексный катализ). Из алкенов получают предельные кислоты:
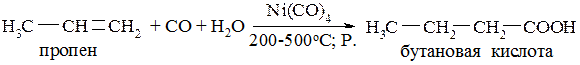
Из представленной схемы видно, что конечный продукт реакции содержит на один углеродный атом больше, чем исходный алкен.
Из алкинов таким путём можно получить α-β-непредельные кислоты:
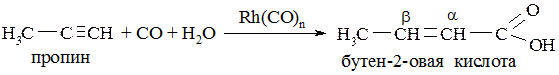
Из метанола в аналогичных условиях получают уксусную кислоту:
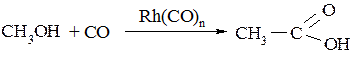
Карбоксилирование реактивов Гриньяра
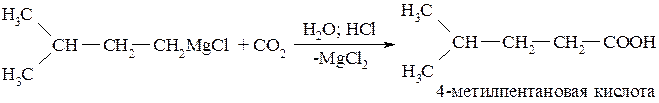
Реакции гидролиза
Реакции гидролиза используются для получения карбоновых кислот из следующих исходных соединений:
- из тригалогенопроизводных,в которых все три атома галогена связаны с первичным углеродным атомом (трихлорметильная группа)
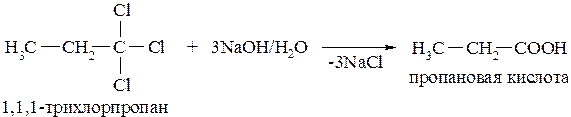
- из нитрилов в щелочной или кислой среде
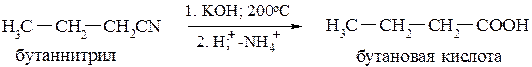
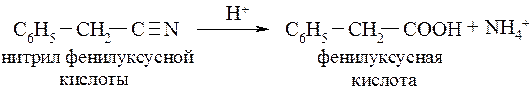
- гидролизом природных сложных эфиров (в том числе и жиров) с целью получения некоторых высших кислот (см. ниже, раздел 17.4.1).
Физические свойства
Четыре первых представителя гомологического ряда предельных монокарбоновых кислот представляют собой летучие жидкости, смешивающиеся с водой в любых соотношениях.
Кислоты – изомасляная, а также С5-С9 представляют собой маслянистые жидкости, плохо растворимые в воде.
Кислоты С10 и выше в воде практически не растворяются.
Ароматические кислоты – кристаллические вещества, по-разному растворимы в воде.
Карбоновые кислоты образуют межмолекулярные водородные связи, причём они гораздо прочнее, чем в спиртах.
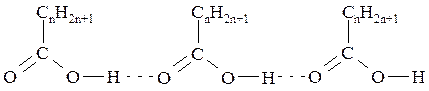
В твёрдом и жидком состояниях для карбоновых кислот более характерны ассоциаты-димеры:
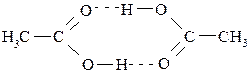
Температуры кипения карбоновых кислот значительно выше, чем у соответствующих спиртов и альдегидов, что объясняется более прочными межмолекулярными водородными связями.
Химические свойства
В карбоксильной группе атом углерода находится в состоянии sp2-гибридизации и он связан двойной связью с атомом кислорода, а простой связью с гидроксигруппой и с водородом (муравьиная кислота) или углеводородным радикалом (остальные кислоты).
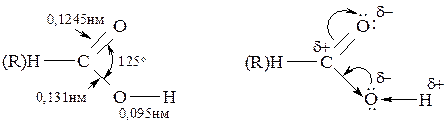
В карбоновых кислотах длина связи С=О больше, чем в кетонах, а связь С–ОН короче, чем в спиртах. Это свидетельствует о взаимодействии электронных пар атома кислорода ОН-группы и С=О за счёт мезомерного и индуктивного эффектов. С одной стороны это приводит к увеличению полярности связи Н–О, но с другой стороны способствует уменьшению положительного заряда на атоме углерода по сравнению с альдегидами и кетонами.
Таким образом, за счёт указанных электронных эффектов в карбоксильной группе формируются два электрофильных центра – водород гидроксигруппы и атом углерода. Атомы кислорода являются нуклеофильными центрами. Понижение электронной плотности на карбоксильном углероде приводит к смещению электронного облака от α-углеродного атома к карбоксилу.
Высокая полярность и лёгкая поляризуемость связи Н–О способствуют отрыву протона и образованию карбоксилат-аниона. Исходя из особенностей электронного строения карбоксильной группы, можно говорить о многосторонней реакционной способности карбоновых кислот, обусловленной: лёгкостью отрыва протона (ОН-кислотность); наличием нуклеофильных центров; наличием электрофильного центра; СН-кислотным центром в α-положении.
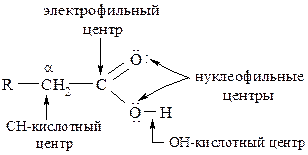
Кислотность
Карбоновые кислоты в водных растворах диссоциированны, что доказывается индикаторами. Они являются более сильными кислотами, чем спирты и фенолы, что объясняется делокализацией отрицательного заряда в образующемся карбоксилат-анионе:
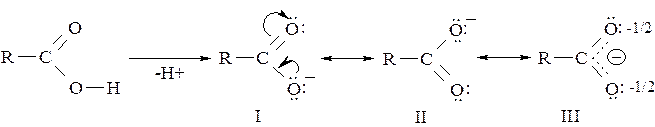
В структуре III длина обеих связей С–О одинаковая и составляет примерно 0,127нм, что является средней между С=О связью (0,1245нм) и С–ОН (0,131нм).
Степень диссоциации карбоновых кислот зависит от различных факторов:
наибольшая степень диссоциации характерна для водных растворов;
в апротонных неполярных растворителях карбоновые кислоты практически недиссоциированы;
наличие электроноакцепторных заместителей в α-положении увеличивает кислотность (сравните для СН3СООН рКα = 4,76, а для Cl3C–COOH рКα = 0,64).
Карбоновые кислоты значительно сильнее угольной и вытесняют её из соответствующих солей:
2СН3СООН + Na2CO3 → 2CH3COONa + H2O + CO2
Они образуют соли под действием алкоголятов:
CH3COOH + C2H5ONa → CH3COONa + C2H5OH
Как протонные кислоты, взаимодействуют с активными металлами, их оксидами и гидроксидами, а также аммиаком с образованием солей: