Опыт № 1. Приготовление раствора хлорида натрия заданной концентрации разбавлением
Рассчитайте, какие объемы исходного раствора и воды необходимы для приготовления 100 мл раствора хлорида натрия заданной концентрации (пример расчета см. ниже). Отмерьте рассчитанный объем исходного раствора мерным цилиндром; последние порции исходного раствора прибавляйте по каплям из капельницы. Затем в этот же цилиндр долейте дистиллированной воды до метки 100 мл; последние порции воды прибавляйте по каплям из соответствующей капельницы. Уровень жидкости определите по нижнему краю мениска.
Полученный раствор слейте в коническую колбу и тщательно перемешайте круговыми движениями. Чтобы установить точную концентрацию приготовленного раствора, налейте его в мерный цилиндр и измерьте его плотность с помощью ареометра.
По измеренной плотности найдите процентную концентрацию хлорида натрия в растворе (см. табл. 1). В случае отклонения плотности полученного раствора, определенной ареометром, от табличного значения, используйте метод интерполяции. Составьте отчет по проделанной работе, включив в него:
- расчет и методику приготовления раствора;
- рисунки ареометра и использованной посуды (рис. 1-4);
- результат определения плотности и процентной концентрации (массовой доли) приготовленного раствора;
- сравнение полученного значения процентной концентрации раствора с заданной;
- в случае отклонения полученного значения процентной концентрации от заданной, выполните расчет абсолютной и относительной ошибки приготовления раствора по формулам:
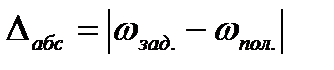 ;
; 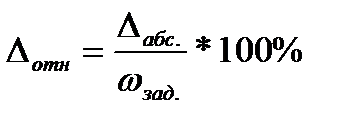 ;
;
- расчет молярной и нормальной концентрации полученного раствора;
- вывод.
Пример расчета.
Какие объемы воды и 18%-ного (по массе) раствора NaClнужно взять для приготовления 100 мл 5%-ного (по массе) раствора NaCl.
| Дано: | Решение: |
| w1 (NaCl) = 18% Vр-ра2= 100 мл w2 (NaCl) = 5% | 1. Найдем массу 100 мл 5%-ного раствора NaCl. Для этого по табл. 1 определим плотность 5%-ного раствора: ρр-ра2 = 1,034 г/см3. mр-ра2= ρр-ра2 * Vр-ра2= 1,034 г/мл ∙ 100 мл = 103,4 г |
| 2. Определим массу NaCl, содержащуюся в 103,4 г 5%-ного раствора. w2 (NaCl) = m2(NaCl)/ mр-ра2* 100%, следовательно, m2(NaCl) = mр-ра2* w2 (NaCl) / 100% = 103,4 г * 5% / 100%= = 5,17 г. | |
| 3. Найдем массу 18% раствора, содержащего 5,17 г NaCl. m1(NaCl) = m2(NaCl) = 5,17 г; w1 (NaCl) = m1(NaCl)/ mр-ра1* 100%, следовательно, mр-ра1= m1(NaCl) * 100% / w1 (NaCl) = = 5,17г*100 % / 18 % = 28,72 г. | |
| Найти: Vр-ра1= ? V(Н2О) = ? | 4. Рассчитаем объем 18% раствора, предварительно определив по табл. 1 плотность исходного раствора ρр-ра1=1,132 г/см3. Vр-ра1= mр-ра1/ ρр-ра1 = 28,72 г /1,132 г/мл ≈ 25,4 мл (расчет выполняем до второго знака после запятой и округляем до первого знака после запятой). |
| 5. Найдем объем воды, необходимый для приготовления 100 мл 5% раствора NaCl. V(Н2О) = Vр-ра2- Vр-ра1= 100-25,4 ≈ 74,6 мл. | |
| Ответ: для приготовления 100 мл 5% раствора NaClтребуется 25,4 мл 18% раствора NaClи 74,6 мл воды. |
Таблица 1 – Плотность водного раствора хлорида натрия при 20°С
| Концентрация, % | ||||||||||||||
| Плотность, г/см3 | 1,005 | 1,013 | 1,020 | 1,027 | 1,034 | 1,041 | 1,049 | 1,056 | 1,063 | 1,071 | 1,086 | 1,101 | 1,116 | 1,132 |
Перечень вариантов лабораторной работы
| № варианта | Концентрация хлорида натрия, % | Контрольные вопросы | ||
| В исходном растворе, w1 | заданная,w2 | Для специальностей химического профиля | Для специальностей нехимического профиля | |
Контрольные вопросы и задачи
1. Сколько граммов хлорида аммония необходимо для приготовления 0,2 М раствора объемом 500 мл? Рассчитайте нормальность этого раствора.
2. Смешали 300 г 20 %-ного раствора и 500 г 40 %-ного раствора хлорида натрия. Чему равны массовая и мольная доли полученного раствора?
3. Какой объем 12 %-ного раствора гидроксида калия (r = 1,1 г/мл) можно приготовить из 2 л 44 %-ного раствора (r = 1,5 г/мл)? Рассчитайте нормальность и моляльность этого раствора.
4. Смешаны 800 мл 3 н раствора и 1,2 л 12 %-ного раствора гидроксида калия (r = 1,1 г/мл). Вычислите молярность и моляльность полученного раствора.
5. Сколько граммов 32 %-ного раствора азотной кислоты следует добавить к 600 г 80 %-ного раствора той же кислоты для получения 64 %-ного раствора?
6. К 1 л 25 % - ной азотной кислоты, плотность которой 1,173 г/см3, добавили 1 л воды. Вычислите массовую и мольную доли (%) азотной кислоты в полученном растворе.
7. Рассчитайте массовую долю растворенного вещества и молярную концентрацию эквивалента в 3 М растворе сернистой кислоты (r = 1,15 г/мл).
8. Рассчитайте молярность и нормальность раствора с массовой долей серной кислоты 20% (ρ = 1,15 г/мл).
9. В воде объемом 450 мл растворили 50 г гидроксида натрия. Плотность полученного раствора ρ = 1,05 г/мл. Рассчитайте массовую долю (%), молярность и нормальность полученного раствора.
10. Рассчитайте массовую долю растворенного вещества и молярную концентрацию эквивалента в 0,1 М растворе фосфата натрия (r = 1,01 г/мл).
11. Рассчитайте молярную концентрацию 0,6 н раствора нитрата бария.
12. Рассчитайте молярную концентрацию раствора, содержащего в 1 л 0,6 моль эквивалента нитрата меди (II).
