Определение осмотической концентрации и осмотического давления раствора хлорида натрия».
1. Установить по термометру Бекмана значение точки замерзания чистого растворителя (Н2О).
а. Настроить термометр Бекмана таким образом, чтобы значение температуры замерзания (точка замерзания) растворителя соответствовало положению столбика ртути в верхней части шкалы.
б. В пробирку криоскопа пипеткой на 10 мл точно отмерить и внести столько растворителя, чтобы уровень его был на 0,5-1 см выше шарика термометра Бекмана.
Нижний конец шарика не должен касаться дна пробирки .Пробирку поместить в воздушную рубашку и погрузить в охладительную смесь. При равномерном перемешивании охлаждают воду в пробирке. При появлении кристаллов температура быстро поднимается, приближаясь к температуре замерзания.
Произвести отсчет точки замерзания чистой воды по максимальной и постоянной высоте столбика ртути термометра.
Отсчет произвести, пользуясь лупой, с точностью до 0,0050
в. Вынуть пробирку из охладительной смеси, кристаллы расплавить, нагревая пробирку рукой, опыт повторить.
г. По двум измерениям вычислить среднее значение точки замерзания растворителя – t0 (расхождение не должно превышать 0,0050).
2. Установить по термометру значение точки замерзания исследуемого раствора NaCl.
а. Воду из пробирки криоскопа слить, пробирку сполоснуть испытуемым раствором, затем налить в нее такой же объем этого раствора как в п.1 и определить точку замерзания этой жидкости – t (см. пункт 1).
3. Вычислить депрессию замерзания раствора, рассчитать его осмотическую концентрацию и осмотическое давление.
а. Депрессию раствора Dt определить как
Dt = t0 – t
б. Осмотическую концентрацию раствора рассчитать по уравнению:
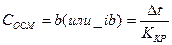 (моль/дм3)
(моль/дм3)
Ккр – криоскопическая постоянная воды
в. Осмотическое давление раствора NaCl вычислить по уравнению.
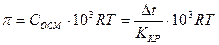 (Н\м2)
(Н\м2)
Лабораторная работа № 12
«Определение молярной массы мочевины».
1. Используя термометр Бекмана, определить точку замерзания чистого растворителя – воды (t0).
2. Приготовить раствор мочевины заданного состава и термометром Бекмана определить его точку замерзания (t).
3. Рассчитать депрессию раствора
Dt = t0 - t
4. Молярную массу мочевины рассчитать по уравнению:
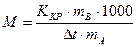 , где
, где
Kkp – криоскопическая постоянная воды;
mB - навеска (масса, г) мочевины;
mA - навеска (масса, г) воды,
Навески mA и mB, взятые для приготовления раствора, указываются преподавателем.
СПРАВОЧНЫЕ ВЕЛИЧИНЫ:
Ккр(Н2О) = 1,86
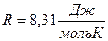
Приложение
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ЗАМЕРЗАНИЯ ТЕРМОМЕТРОМ БЕКМАНА
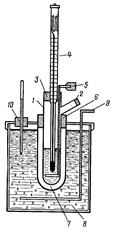 рис. 1 рис. 1 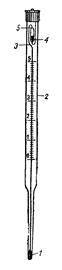 | Прибор для измерения температуры замерзания по Бекману (криоскоп) (рис.1) состоит из толстостенного стакана (8) с крышкой В. В крышке имеются два отверстия: одно для мешалки (9), другое для широкой трубки(6), в которую вставлена пробирка (1) с боковым тубусом (2). В пробирку наливают раствор и вставляют на пробке термометр Бекмана (4). Через эту же пробку проходит мешалка (5). Стакан (8) заполняют охладительной смесью. Температура смеси должна быть на несколько градусов ниже температуры замерзания растворителя Криометрические наблюдения проводятся с разбавленными растворами, для которых только и применимо уравнение Т = Ккр*b. Депрессия таких растворов не превышает 0, 20-0, 30, поэтому отсчет температуры замерзания раствора и растворителя надо производить с большой точностью. Ошибка в отсчете температуры на 0, 002-0, 003 дает ошибку в 1% от измеряемой величины. Такой точности можно добиться, пользуясь термометром Бекмана (рис.2). Отличие термометра Бекмана от обычного термометра заключается в том, что он имеет условную шкалу, т.к. количество ртути в шарике (1) термометра можно изменять. Для этой цели верхняя часть капилляра заканчивается резервуаром, содержащим запас ртути. Ртуть из шарика можно переводить в верхний резервуар, нагревая шарик рукой до тех пор, пока ртуть не заполнит весь капилляр и капелька ее не появится в верхней части резервуара. |
(рис.2).
Перевертывая термометр и постукивая пальцем, можно заставить ртуть оторваться. Для того, чтобы перевести ртуть из верхнего резервуара в нижний, надо, нагревая шарик термометра рукой, соединить ртуть, находящуюся в шарике (а) со ртутью в верхнем резервуаре, а затем охлаждать шарик, тогда ртуть будет засасываться в шарик термометра.
Изменение количества ртути в шарике приводит к тому, что показания термометра при одной и той же температуре могут быть различными и одно и то же показание термометра может соответствовать различным температурам.
Термометр при криометрических измерениях настраивают таким образом, чтобы ртуть в капилляре оставалась на каком-нибудь делении в верхней части его шкалы.
Шкала термометра Бекмана поделена на сотые доли градуса. Тысячные доли градуса отсчитывают при помощи лупы.
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ЗАМЕРЗАНИЯ ВОДЫ.
Заполняют стакан А охладительной смесью. Наливают в пробирку g воду в таком количестве, чтобы после погружения термометра уровень жидкости был выше ртути в шарике термометра примерно на 0,5-1 см. Затем вставляют в пробирку термометр (термометр не должен касаться дна пробирки) и мешалку (Г). Мешалка должна ходить вверх и вниз совершенно свободно, не задевая термометр и стенок пробирки.
Наблюдают за перемещением ртути в капилляре и записывают положение мениска ртути в течение опыта. Ртуть в капилляре сначала медленно снижается, а затем начинает повышаться. Повышение вызвано тем, что вода, охлажденная до температуры замерзания (переохлаждение), начинает кристаллизоваться и освобождается скрытая теплота плавления. Температура поднимается до значения, соответствующего температуре замерзания. Отмечают максимальную температуру, которая устанавливается после переохлаждения. Эта температура и будет температурой замерзания (точкой замерзания) воды.
Температуру отмечают с точностью до 0, 0050.
Опыт повторяют. Для этого вынимают пробирку (g) из рубашки, обогревают ее рукой, помешивая мешалкой до полного растворения кристаллов, и вставляют на прежнее место. Теперь, когда температура замерзания найдена, перемешивают жидкость до тех пор, пока температура не будет на 0, 5-1, 0 выше, чем в первом опыте. Затем энергичным перемешиванием вызывают кристаллизацию и отмечают максимальную температуру. Найденная в двух опытах температура замерзания не должна отличаться больше, чем на 0, 0050. Если расхождение превышает 0, 0050, то опыт повторяют еще раз. Вычисляют среднее значение температуры замерзания.
Задание для самостоятельной работы:
