III. Реакции отщепления галогеноводорода
1. При нагревании
СH3-CH2Cl 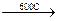 HCl + CH2=CH2
HCl + CH2=CH2
2. Под действием спиртового раствора щелочи
СH3-CH3-Cl + KOHспиртовый 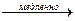
A B
 +///
+/// 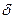 +//
+// 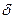 +/
+/ 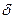 -
-
H H
H  C
C  C
C  Cl
Cl 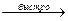 CH2=CH2 + H2o + KCl
CH2=CH2 + H2o + KCl
HO- H H K+
R=k[A][B]
Реакция нуклеофильного отщепления протекает по механизму ЕN2.
У третичных галоидных алкилов идет, в основном, по механизму ЕN1.
H CH3 H CH3 CH3
H-C-C-Cl 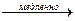 H-C-C+
H-C-C+ 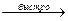 H+ + H2C=C
H+ + H2C=C
H CH3 H CH3 CH3
А изобутилен
r=k[A]
Такие реакции обычно сопутствуют реакциям нуклеофильного замещения.
ЛЕКЦИЯ 7
ГАЛОГЕНОПРОИЗВОДНЫЕ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ
Подразделяются на три типа.
I. Галогенопроизводные винилового типа: атом галогена находится у непредельного атома углерода.
СН2=СНCl хлористый винил
СН2=ССl2 хлористый винилиден
СН2=С-СН=СН2 хлорпрен
Cl
II. Галогенпроизводные аллильного типа (галоген в 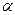 -положении к двойной связи).
-положении к двойной связи).
СН2=СН-СН2-Сl хлористый аллил
СН3-СН=СН-СН2Cl хлористый кротил
III. Галогенпроизводные с изолированным расположением двойной связи и Hal.
СН2=СН-СН2-СН2-Cl 4-хлор-1-бутен
В этом случае галоген не подвергается влиянию 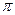 -связи и ведет себя так же, как в предельных галогеноводородах.
-связи и ведет себя так же, как в предельных галогеноводородах.
I. Галогенопроизводные винильного типа.
Получение
1) Присоединение одной молекулы ННal к ацетиленовым углеводородам.
СН 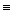 СН + HCl
СН + HCl  СН2=СНCl
СН2=СНCl
хлористый винил
СН2=СН-С 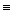 СН + HCl
СН + HCl  СН2=СН-С=СН2
СН2=СН-С=СН2
Cl
1,3-бутадиенин хлорпрен
2) Пиролиз полигалогенопроизводных
СН2-СН2 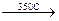 HCl + СН2=СН-Cl
HCl + СН2=СН-Cl
Cl Cl
хлористый хлористый
этилен винил
3) Действие недостатка спиртового раствора КОН на полигалогенопроизводные
Cl Cl
СН-СН 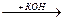 СНCl=CCl2
СНCl=CCl2
Cl Cl -HCl
тетрахлорэтан трихлорэтилен
Особенности свойств
1. Соединения винильного типа проявляют инертность в реакциях нуклеофильного замещения. Причина заключается в особенности электронного строения. Графически это можно показать следующим образом:
..
СН2=СН-Cl:
..
или
Н Сl
C - C p- 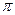 -сопряжения
-сопряжения
H H
Хлор расположен через одну простую связь от двойной и имеет 3 неподеленных пары электронов. Наблюдается эффект p- 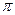 -сопряжения, т.е. перекрытие р-электронной орбитали хлора с
-сопряжения, т.е. перекрытие р-электронной орбитали хлора с 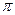 -орбиталями атома углерода. В результате часть электронного облака хлора оттягивается в сторону двойной связи и дипольный момент связи C-Сl уменьшается.
-орбиталями атома углерода. В результате часть электронного облака хлора оттягивается в сторону двойной связи и дипольный момент связи C-Сl уменьшается.
2. Реакции присоединения по двойной связи идут в соответствии с правилом Марковникова, т.к.
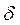 -
- 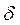
 + ..
+ ..
СН2=СН  Сl + HCl CН3-СНCl2
Сl + HCl CН3-СНCl2
этилиденхлорид
/+М/</-I/, по p- 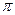
+ +
СН3  СН-Cl (1) СН2-СН2
СН-Cl (1) СН2-СН2  Cl (2)
Cl (2)
Более устойчив катион (1), т.к. электродонорная метильная группа частично компенсирует положительный заряд.
3. Очень легко полимеризуются.
n СН2=СНCl  (-CН2-СНCl-)n
(-CН2-СНCl-)n
винилхлорид ПВХ-самые массовые пластмассы
Полимеры на основе винилхлорида находят широчайшее применение для изготовления пленок, пластмассовых изделий. Они устойчивы к действию влаги, кислот, щелочей, нефтепродуктов, обладают хорошими электроизоляционными свойствами.
II. Соединения аллильного типа
Получение
1) Реакция Шешукова – высокотемпературное хлорирование
СН2=СН-СН3 + Сl2 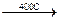 CН2=СН-СН2Сl
CН2=СН-СН2Сl
-HCl
Особенности свойств
1. Обладают высокой активностью в реакциях нуклеофильного замещения. Реагируют только по механизму SN1. Объясняется это исключительно большой устойчивостью образующегося промежуточного аллильного катиона.
14 12 14 +
СН2=СН-СН2-Сl  CН2=СН-СН2 + Cl-
CН2=СН-СН2 + Cl-
граничные структуры
+ 12 аллильного катиона
CН2-СН=СН2
т.е. в этом катионе положительный заряд распределен равномерно между крайними атомами углерода.
Фактическое строение мезомерного аллильного катиона следующее:
+
CН2-СН-СН2
Это подтверждено исследованием строения продуктов реакции замещения хлора в хлористом аллиле методом меченых атомов,
 14 12
14 12 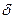 +
+ 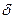 + +ОН- 50% СН2=СН-СН2-ОН
+ +ОН- 50% СН2=СН-СН2-ОН

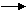 СН2=СН-СН2-Cl
СН2=СН-СН2-Cl  Cl- + CН2-СН-СН2 50% 14
Cl- + CН2-СН-СН2 50% 14
СН2=СН-СН2-ОН
аллиловый спирт
присоединение реагента происходит в равной мере по обоим концам катиона.
2. Способны к реакциям электрофильного присоединения.
Реакции присоединения ННal к хлористому аллилу происходят в соответствии с правилом Марковникова.
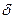 -
-
СН2=СН 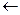 СН2-Сl + HCl
СН2-Сl + HCl  CН3-СН2-СН2
CН3-СН2-СН2
Cl Cl
1,2-дихлорпропан
Перечисленные реакции используются в промышленном органическом синтезе, в частности, для получения глицерина из хлористого аллила.

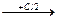 CН2-СН-СН2
CН2-СН-СН2  CН2-СН-СН2
CН2-СН-СН2
Cl Cl Cl -3HCl ОН ОН ОН
CН2=СН-СН2-Сl 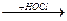 CН2-СН-СН2
CН2-СН-СН2 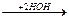 CН2-СН-СН2
CН2-СН-СН2
Cl Cl Cl -2HCl ОН ОН ОН
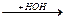 СН2=СН-СН2ОН
СН2=СН-СН2ОН 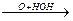 CН2-СН-СН2
CН2-СН-СН2
-HCl ОН ОН ОН
Фторпроизводные предельных углеводородов
Получение
Обычные методы непригодны из-за большой активности фтора.
1) Замещение других галогенов в галогенопроизводных углеводородов на фтор при действии различных соединений фтора. Реакция Финкельштейна.
C5H11Br + AgF  C5H11F + AgBr (Реакция Финкельштейна)
C5H11F + AgBr (Реакция Финкельштейна)
бромистый менее растворим, чем AgF
амил
3ССl4 + 2SbF3 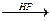 3CCl2F2 + 2SbCl3 (реакция Сваартса)
3CCl2F2 + 2SbCl3 (реакция Сваартса)
фреон 12
(дихлордифторметан)
SbCl3 + 3HF  SbF3 + 3HCl
SbF3 + 3HCl
(практически расходуется HF, а SbF3 играет роль переносчика фтора)
СНCl3 + 2HF  CНClF2 + 2HCl
CНClF2 + 2HCl
Фреон 22
(монохлордифторметан)
2) Прямое фторирование предельных углеводородов, разбавленных азотом или СCl4, действием фтора в присутствии катализаторов – переносчиков фтора. Образование продуктов полного фторирования – перфторуглеводородов.
2AgF + F2  2AgF2
2AgF2
CH4 (+NH2) + 8AgF2  CF4 + 4HF + 8AgF (+N2)
CF4 + 4HF + 8AgF (+N2)
перфторметан
3) электрохимическое фторирование (Саймонс) – электролиз органических соединений, растворенных в безводной плавиковой кислоте.
С7Н16 + 16HF 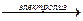 C7F16 + 16H2
C7F16 + 16H2
С4Н9COOH + 10HF 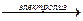 C4F10 + CO2 + 10H2
C4F10 + CO2 + 10H2
Условия электролиза – угольный анод, стальная ванна. На аноде происходит образование свободных атомов фтора
F- - 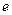
 F.,
F.,
которые действуют далее на углеродный радикал или углеводород.
4) Получение ненасыщенных полифторпроизводных путем отщепления HHal от фреонов.
СНClF2 + CHClF2 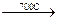 CF2=CF2
CF2=CF2
-2HCl
фреон тетрафторэтилен
Это соединение легко полимеризуется, образуя полимерные перфторуглеводороды.
nCF2=CF2  (-CF2-CF2)n
(-CF2-CF2)n
политетрафторэтилен
(тефлон)
