Электролиз расплава хлорида натрия
Сначала, при расплавлении соли, происходит её ионизация (электролитическая диссоциация):
Na+С1– → Nа+ + С1–.
ионная пара
Далее, под действием электрического тока к катоду направляется положительно заряженный атом натрия – катион и получает с катода электрон, т. е. происходит восстановление:
К(–): Nа+ + е– = Nа.
К аноду направляется отрицательно заряженный атом хлора – анион. Поскольку на аноде постоянно создаётся недостаток электронов, атом хлора отдаёт электрон, т. е. окисляется. Образующиеся электронейтральные атомы хлора образуют молекулу хлора:
А (+): 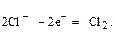
Суммарное, или общее, уравнение реакции электролиза получают, складывая уравнения полуреакций окисления и восстановления, для этого, если необходимо, умножают каждое из уравнений на коэффициент, уравнивающий число электронов, участвующих в катодном и анодном процессах.
2NaCl = 2Na + Cl2↑.
Восстановительное и окислительное действие электрического тока может быть во много раз сильнее химических восстановителей и окислителей. Не существует химического окислителя, который отнял бы у отрицательно заряженного атома (иона) фтора его электрон. Это осуществляется, однако, при электролизе расплава смеси безводного жидкого фтороводорода HF с фторидом калия KF или фторида состава KF * 2HF.
На графитовом аноде выделяется фтор:
2F– – 2е– = F2,
а на катоде – водород:
2Н+ + 2е– = Н2
2HF 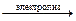 H2↑ + F2↑.
H2↑ + F2↑.
Электролиз расплава гидроксида калия
КОН → К+ + ОН–
| К (–): К+ + е– = К А (+): 4ОН– – 4е– = О2 + 2Н2О | 4 (процесс восстановления) 1 (процесс окисления) | ||
4К+ + 4OН– = 4К + O2 + 2Н2O
4КОН = 4К + O2↑ + 2Н2O.
Если электролизу подвергается расплав, содержащий несколько различных катионов, то последовательность их восстановления определяется соответствующими электродными потенциалами. Чем выше электродный потенциал катиона, тем раньше он начнёт восстанавливаться.
ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
В электролизе водных растворов электролитов принимает участие и вода. В растворе находятся гидратированные ионы металла и кислотные остатки, а также молекулы воды и продукты её электролитической диссоциации.
Таблица 4
Ряд стандартных электродных потенциалов металлов
(металлы располагаются по возрастанию алгебраической
величины их нормальных электродных потенциалов)
| Электрод | Окислительная форма | Усиление окислительных свойств  | |||||||||
| Fe2+ | Ni2+ | Sn2+ | Pb2+ | 2H+ | Cu2+ | Ag+ | Pt2+ | Au | |||
| Восстановительная форма | Fe | Ni | Sn | Pb | 2H | Cu | Ag | Pt | Au | ||
Усиление восстановительных свойств  | |||||||||||
| Е0, В | –0,44 | –0,25 | –0,14 | –0,13 | +0,34 | +0,80 | +1,20 | +1.52 | |||
| Электрод | Окислительная форма | Усиление окислительных свойств  | |||||||||
| Li+ | K+ | Ca2+ | Na+ | Mg2+ | Al3+ | Mn2+ | Zn2+ | Cr3+ | |||
| Восстановительная форма | Li | K | Ca | Na | Mg | Al | Mn | Zn | Cr | ||
Усиление восстановительных свойств  | |||||||||||
| Е0, В | –3,04 | –2,92 | –2,87 | –2,71 | –2,37 | –1,66 | –1,18 | –0,76 | –0,74 | ||
