Некоторые стандартные начала С2
Задача 8.1 Смесь гидросульфата и сульфата натрия обработали избытком гидроксида натрия…. Такую же смесь обработали избытком гидроксида бария…
Задача 8.2 Смесь порошков меди и оксида меди (II) нагрели с избытком концентрированной серной кислоты…
Задача 8.3 Смесь порошков меди и оксида меди (II) нагрели с избытком соляной кислоты…
Задача 8.4 Смесь сульфида цинка и оксида цинка обработали избытком соляной кислоты…
Задача 8.5 Смесь порошков меди (I) и оксида меди (II) нагрели с избытком концентрированной серной кислоты…
Ответы внизу
Разложение нитратов
В целом разложение нитратов происходит согласно известной схеме, и состав продуктов зависит от расположения металла в ряду активности. Но есть сложные ситуации:
Задача 9.1 Какие продукты получатся при разложении нитрата железа (II)? Запишите уравнение реакции.
Задача 9.2 Какие продукты получатся при разложении нитрата меди (II)? Запишите уравнение реакции.
Ответы внизу
Какие неметаллы реагируют с щелочью, а какие – нет?
Нам надо знать, что из неметаллов, упоминаемых в школьном курсе:
C, N2, O2 – не реагируют с щелочами
Si, S, P, Cl2, Br2, I2, F2 – реагируют:
Si + 2KOH + H2O = K2SiO3 + 2H2,
3S + 6KOH = 2K2S + K2SO3 + 3H2O,
Cl2 + 2KOH (холодный)= KCl + KClO + H2O,
3Cl2 + 6KOH (горячий) = 5KCl + KClO3 + 3H2O
(аналогично бром и иод)
4P + 3NaOH + 3H2O = 3NaH2PO2 + PH3
Органическая химия
Тривиальные названия
Надо знать, какие органические вещества соответствуют названиям:
изопрен, дивинил, винилацетилен, толуол, ксилол, стирол, кумол, этиленгликоль, глицерин, формальдегид, уксусный альдегид, пропионовый альдегид, ацетон, первые шесть предельных одноосновных кислот (муравьиная, уксусная, пропионовая, масляная, валериановая, капроновая), акриловая кислота, стеариновая кислота, пальмитиновая кислота, олеиновая кислота, линолевая кислота, щавелевая кислота, бензойная кислота, анилин, глицин, аланин. Не путайте пропионовую кислоту с пропеновой!! Соли важнейших кислот: муравьиной – формиаты, уксусной – ацетаты, пропионовой – пропионаты, масляной – бутираты, щавелевой – оксалаты. Радикал –CH=CH2 называется винил!!
Заодно и некоторые неорганические тривиальные названия:
Поваренная соль (NaCl), негашеная известь (CaO), гашеная известь (Ca(OH)2), известковая вода (раствор Ca(OH)2), известняк (CaCO3), кварц (он же кремнезем или диоксид кремния – SiO2), углекислый газ (CO2), угарный газ (CO), сернистый газ (SO2), бурый газ (NO2), питьевая или пищевая сода (NaHCO3), кальцинированная сода (Na2CO3), аммиак (NH3), фосфин (PH3), силан (SiH4), пирит (FeS2), олеум (раствор SO3 в концентрированной H2SO4), медный купорос (CuSO4∙5H2O).
Некоторые редкие реакции
1) Образование винилацетилена:
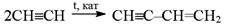
Винилацетилен далее способен вступать в реакции присоединения и, в частности. Является сырьем для получения хлоропрена, из которого делают хлоропреновый каучук:
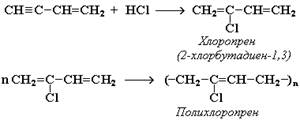
2) Реакция прямого окисления этилена в уксусный альдегид:

Эта реакция коварна тем, что мы хорошо знаем, как ацетилен превращается в альдегид (реакция Кучерова), а если в цепочке встретится превращение этилен → альдегид, то это может нас поставить в тупик. Так вот, имеется в виду эта реакция!
3) Реакция прямого окисления бутана в уксусную кислоту:
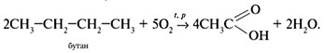
Эта реакция лежит в основе промышленного производства уксусной кислоты.
4) Реакция Лебедева:
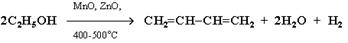
Отличия фенолов от спиртов
Огромное количество ошибок в таких заданиях!!
1) Следует помнить, что фенолы более кислотны, чем спирты (связь О-Н в них более полярна). Поэтому спирты не реагируют с щелочью, а фенолы реагируют и с щелочью, и некоторыми солями (карбонаты, гидрокарбонаты).
Например:
Задача 10.1
Какие из этих веществ реагируют с литием:
а) этиленгликоль, б) метанол, в) фенол, г) кумол, д) глицерин.
Задача 10.2
Какие из этих веществ реагируют с гидроксидом калия:
а) этиленгликоль, б) стирол, в) фенол, г) этанол, д) глицерин.
Задача 10.3
Какие из этих веществ реагируют с гидрокарбонатом цезия:
а) этиленгликоль, б) толуол, в) пропанол-1, г) фенол, д) глицерин.
2) Следует помнить, что спирты реагируют с галогеноводородами (эта реакция идет по связи С-О), а фенолы нет (в них связь С-О из-за эффекта сопряжения малоподвижна).
Дисахариды
Основные дисахариды: сахароза, лактоза и мальтоза имеют одинаковую формулу C12H22O11.
О них следует помнить:
1) что они способны гидролизоваться на те моносахариды, из которых состоят: сахароза – на глюкозу и фруктозу, лактоза – на глюкозу и галактозу, мальтоза – на две глюкозы.
2) что лактоза и мальтоза обладают альдегидной функцией, то есть являются восстанавливающими сахарами (в частности, дают реакции «серебряного» и «медного» зеркала), а сахароза – невосстанавливающий дисахарид, не имеет альдегидной функции.
Механизмы реакций
Будем надеяться, что достаточно следующих знаний:
1) для алканов (в том числе в боковых цепях аренов, если эти цепи предельные) характерны реакции свободнорадикального замещения (с галогенами), которые идут по радикальному механизму (инициирование цепи – образование свободных радикалов, развитие цепи, обрыв цепи на стенках сосуда или при соударении радикалов);
2) для алкенов, алкинов, аренов характерны реакции электрофильного присоединения, которые идут по ионному механизму (через образование пи-комплекса и карбокатиона).
Особенности бензола
1. Бензол в отличие от других аренов не окисляется перманганатом калия.
2. Бензол и его гомологи способны вступать в реакцию присоединения с водородом. Но только бензол способен также вступать в реакцию присоединения с хлором (только бензол и только с хлором!). При этом все арены способны вступать в реакцию замещения с галогенами.
Реакция Зинина
Восстановление нитробензола (или аналогичных ему соединений) в анилин (или другие ароматические амины). Эта реакция в одном из ее видов почти обязательно встретится!
Вариант 1 – восстановление молекулярным водородом:
C6H5NO2 + 3H2 → C6H5NH2 +2H2O
Вариант 2 – восстановление водородом, полученным при реакции железа (цинка) с соляной кислотой:
C6H5NO2 + 3Fe + 7HCl → C6H5NH3Cl +3FeCl2 + 2H2O
Вариант 3 – восстановление водородом, полученным при реакции алюминия с щелочью:
C6H5NO2 + 2Al + 2NaOH + 4H2O → C6H5NH2 +2Na[Al(OH)4]
Свойства аминов
Почему-то свойства аминов запоминаются хуже всего. Возможно, это связано с тем, что амины изучаются в курсе органической химии последними, и их свойства не удается повторить, изучая другие классы веществ. Поэтому рецепт такой: просто выучить все свойства аминов, аминокислот и белков.
