Экспериментальные доказательства генетической роли нуклеиновых кислот.
Известно, что бактерия Pneutnococcus pneumoniae имеет несколько форм. Вирулентность бактерии определяется наличием мукополисахаридной капсулы, расположенной па поверхности клетки. Эта капсула защищает бактерию от воздействий со стороны организма-хозяина. В результате, размножившиеся бактерии убивают зараженное животное. Бактерии этого штамма (S-штамм) образуют гладкие колонии. Авирулентные формы бактерий не имеют защитной капсулы и образуют шероховатые колонии (R-штамм). Микробиолог Фредерик Гриффитс в 1928 году инъецировал мышам живого пневмококка R-штамма вместе с S-штаммом, убитым высокой температурой (65°С). Спустя некоторое время ему удалось выделить из заражённых мышей живых пневмококков, обладающих капсулой. Таким образом, оказалось, что свойство убитого пневмококка - способность образовывать капсулу - перешло к живой бактерии, т.е. произошла трансформация. Поскольку признак наличия капсулы является наследственным, то следовало предположить, что какая-то часть наследственного вещества от бактерий штамма S перешла к клеткам штамма R.
В 1944 году О.Т. Эвери, К.М. Маклеод и М. Маккарти показали, что такое же превращение типов пневмококков может происходить в пробирке, т.е. in vitro. Эти исследователи установили существование особой субстанции -"трансформирующего принципа", -экстракта из клеток штамма S, обогащенного ДНK. Как далее выяснилось, ДНK, выделенная из клеток S-штамма добавленная в культуру R-штамма, трансформировала часть клеток в S-форму, Клетки стойко передавали это свойство при дальнейшем размножении. Обработка "трансформирующего фактора"ДНК-азой, ферментом разрушающим ДНK, блокирована трансформацию. Эти данные впервые показали, что именно ДНК, а не белок, как полагали до тех пор, является наследственным материалом.
2. 1952г. Эксперимент Альфреда Херши и Марты Чейз.
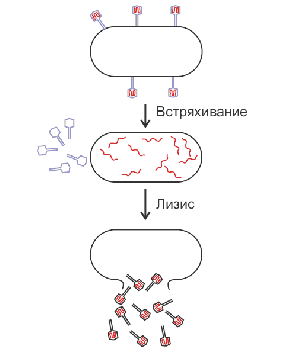 Как известно, фаг Т2 является вирусом, инфицирующим бактерию E. coli. фаговые частицы абсорбируются на наружной поверхности клетки, их материал проникает внутрь и примерно через 20 минут бактерия лизируется, освобождая большое количество фаговых частиц - потомков. В 1952 году Альфред Херши и Марта Чейз инфицировали бактерии фагами Т2, которые были мечены радиоактивными соединениями: ДНК - с помощью 32P. Белковая часть фага - 35S. После инфекции бактерии фагами, с помощью центрифугирования удалось выделить две фракции: пустые белковые оболочки фага и бактерии, инфицированных фаговой ДНК. Оказалось, что 80% метки 35S осталась в пустых фаговых оболочках, а 70% метки 32P - в инфицированных бактериях. Фаги-потомки получили только около 1% исходного белка, меченного 35S, однако они же обнаружили около 30% метки 32P.
Как известно, фаг Т2 является вирусом, инфицирующим бактерию E. coli. фаговые частицы абсорбируются на наружной поверхности клетки, их материал проникает внутрь и примерно через 20 минут бактерия лизируется, освобождая большое количество фаговых частиц - потомков. В 1952 году Альфред Херши и Марта Чейз инфицировали бактерии фагами Т2, которые были мечены радиоактивными соединениями: ДНК - с помощью 32P. Белковая часть фага - 35S. После инфекции бактерии фагами, с помощью центрифугирования удалось выделить две фракции: пустые белковые оболочки фага и бактерии, инфицированных фаговой ДНК. Оказалось, что 80% метки 35S осталась в пустых фаговых оболочках, а 70% метки 32P - в инфицированных бактериях. Фаги-потомки получили только около 1% исходного белка, меченного 35S, однако они же обнаружили около 30% метки 32P.
Результаты этого эксперимента прямо показали, что ДНК родительских фагов проникает в бактерии и затем становиться составляющей развившихся новых фагов частиц.
3. 1957г. Опыты Френкеля - Конрата
Френкель-Конрат работал с вирусом табачной мозаики (ВТМ). В этом вирусе содержится РНК, а не ДНК. Было известно, что разные штаммы вируса вызывают разную картину поражения листьев табака. После смены белковой оболочки "переодетые"вирусы вызывали картину поражения, характерную для того штамма, чья РНК была покрыта чужим белком.
Следовательно, не только ДНК, но и РНК может служить носителем генетической информации.
На сегодняшний день существуют сотни тысяч доказательств генетической роли нуклеиновых кислот. Приведенные три являются классическими.
12.Химическая организация гена. Классификация генов по структуре и функциям.
Структура генов
Ген представляет собой последовательность нуклеотидов ДНК размером от нескольких сотен до миллиона пар нуклеотидов, в которых закодирована генетическая информация о первичной структуре белка (число и последовательность аминокислот). Для регулярного правильного считывания информации в гене должны присутствовать: кодон инициации, множество смысловых кодонов и кодон терминации. Три подряд расположенных нуклеотида представляют собой кодон, который и определяет, какая аминокислота будет располагаться в данной позиции в белке. Например, в молекуле ДНК последовательность оснований ТАС является кодоном для аминокислоты метионина, а последовательность ТТТ кодирует фенилаланин. В молекуле иРНК вместо тимина (Т) присутствует основание урацил (У). Таблица генетического кода во всех руководствах представлена именно символами иРНК. Из 64 возможных кодонов смысловыми являются 61, а три триплета — УАА, УАГ, УГА — не кодируют аминокислоты и поэтому были названы бессмысленными, однако на самом деле они представляют собой знаки терминации трансляции.
Для прокариот характерна относительно простая структура генов. Так, структурный ген бактерии, фага или вируса, как правило, контролирует одну ферментативную реакцию. Специфичным для прокариот является оперонная система организации нескольких генов. Гены одного оперона (участка генетического материала, состоящего из 1, 2 и более сцепленных структурных генов, которые кодируют белки (ферменты), осуществляющие последовательные этапы биосинтеза какого-либо метаболита; в оперон эукариот входит, как правило, 1 структурный ген; оперон содержит регуляторные элементы) расположены в кольцевой хромосоме бактерии рядом и контролируют ферменты, осуществляющие последовательные или близкие реакции синтеза (лактозный, гистидиновый и др. опероны).
Структура генов у бактеориофагов и вирусов в основном схожа с бактериями, но более усложнена и сопряжена с геномом хозяев. Например, у фагов и вирусов обнаружено перекрывание генов, а полная зависимость вирусов эукариот от метаболизма клетки-хозяина привела к появлению экзон-интронной структуры генов.
Эукариотические гены, в отличие от бактериальных, имеют прерывистое мозаичное строение. Кодирующие последовательности (экзоны) перемежаются с некодирующими (интронами). Экзон [от англ. ex(divssi)on — выражение, выразительность] - участок гена, несущий информацию о первичной структуре белка. В гене экзоны разделены некодирующими участками — интронами. Интрон (от лат. inter — между) - участок гена, не несущий информацию о первичной структуре белка и расположенный между кодирующими участками — экзонами. В результате структурные гены эукариот имеют более длинную нуклеотидную последовательность, чем соответствующая зрелая иРНК, последовательность нуклеотидов в которой соответствует экзонам. В процессе транскрипции информация о гене списывается с ДНК на промежуточную иРНК, состоящую из экзонов и интронов. Затем специфические ферменты — рестриктазы — разрезают эту про-иРНК по границам экзон-интрон, после чего экзонные участки ферментативно соединяются вместе, образуя зрелую иРНК (так называемый сплайсинг). Количество интронов может варьировать в разных генах от нуля до многих десятков, а длина — от нескольких пар оснований до нескольких тысяч.
Ген может кодировать различные РНК-продукты путем изменения инициирующих и терминирующих кодонов, а также альтернативного сплайсинга. Альтернативная экспрессия гена осуществляется и путем использования различных сочетаний экзонов в зрелой иРНК, причем полипептиды, синтезированные на таких иРНК, будут различаться как по количеству аминокислотных остатков, так и по их составу.
Наряду со структурными и регуляторными генами обнаружены участки повторяющихся нуклеотидных последовательностей, функции которых изучены недостаточно, а также мигрирующие элементы (мобильные гены), способные перемещаться по геному. Найдены также так называемые псевдогены у эукариот, которые представляют собой копии известных генов, расположенные в других частях генома и лишенные интронов или инактивированные мутациями.
3. Классификация генов
Накопленные знания о структуре, функциях, характере взаимодействия, экспрессии, мутабильности и других свойствах генов породили несколько вариантов классификации генов.
По месту локализации генов в структурах клетки различают расположенные в хромосомах ядра ядерные гены и цитоплазматические гены, локализация которых связана с хлоропластами и митохондриями.
По функциональному значению различают структурные гены, характеризующиеся уникальными последовательностями нуклеотидов, кодирующих свои белковые продукты, которые можно идентифицировать с помощью мутаций, нарушающих функцию белка, и регуляторные гены — последовательности нуклеотидов, не кодирующие специфические белки, а осуществляющие регуляцию действия гена (ингибирование, повышение активности и др.).
По влиянию на физиологические процессы в клетке различают летальные, условно летальные, супервитальные гены, гены-мутаторы, гены-антимутаторы и др.
Следует отметить, что любые биохимические и биологические процессы в организме находятся под генным контролем. Так, деление клеток (митоз, мейоз) контролируется несколькими десятками генов; группы генов осуществляют контроль восстановления генетических повреждений ДНК (репарация). Онкогены и гены — супрессоры опухолей участвуют в процессах нормального деления клеток. Индивидуальное развитие организма (онтогенез) контролируется многими сотнями генов. Мутации в генах приводят к измененному синтезу белковых продуктов и нарушению биохимических или физиологических процессов.
Гомеозисные мутации у дрозофилы позволили открыть существование генов, нормальной функцией которых является выбор или поддержание определенного пути эмбрионального развития, по которому следуют клетки. Каждый путь развития характеризуется экспрессией определенного набора генов, действие которых приводит к появлению конечного результата: глаза, голова грудь, брюшко, крыло, ноги и т. д. Исследования генов комплекса bithorax дрозофилы американским генетиком Льюисом показали, что это гигантский кластер тесно сцепленных генов, функция которых необходима для нормальной сегментации груди (thorax) и брюшка (abdomen). Подобные гены получили название гомеобоксных. Гомеобоксные гены расположены в ДНК группами и проявляют свое действие строго последовательно. Такие гены обнаружены и у млекопитающих, и они имеют высокую гомологию (сходство).
4. Функции генов
В процессе реализации наследственной информации, заключенной в гене, проявляется целый ряд его свойств. Определяя возможность развития отдельного качества, присущего данной клетке или организму, ген характеризуется дискретностью действия (от лат. discretus — разделенный, прерывистый), прерывностью (интроны и экзоны). Дискретность наследственного материала, предположение о которой высказал еще Г. Мендель, подразумевает делимость его на части, являющиеся элементарными единицами, - гены. В настоящее время ген рассматривают как единицу генетической функции. Он представляет собой минимальное количество наследственного материала, которое необходимо для синтеза тРНК, рРНК или полипептида с определенными свойствами. Ген несет ответственность за формирование и передачу по наследству отдельного признака или свойства клеток, организмов данного вида. Кроме того, изменение структуры гена, возникающее в разных его участках, в конечном итоге приводит к изменению соответствующего элементарного признака.
Ввиду того что в гене заключается информация об аминокислотной последовательности определенного полипептида, его действие является специфичным. Однако в некоторых случаях одна и та же нуклеотидная последовательность может детерминировать синтез не одного, а нескольких полипептидов. Это наблюдается в случае альтернативного сплайсинга у эукариот и при перекрывании генов у фагов и прокариот. Очевидно, такую способность следует оценить как множественное, или плейотропное, действие гена (хотя традиционно под плейотропным действием гена принято понимать участие его продукта – полипептида – в разных биохимических процессах, имеющих отношение к формированию различных сложных признаков). Например, участие фермента в ускорении определенной реакции (см. рис.), которая является звеном нескольких биохимических процессов, делает зависимыми результаты этих процессов от нормального функционирования гена, кодирующего этот белок. Нарушение реакции A→B, катализируемой белком α, в результате мутации гена ведет к выключению последующих этапов формирования признаков D и E.

 α D
α D

 A B
A B
 C
C
Определяя возможность транскрибирования мРНК для синтеза конкретной полипептидной цепи, ген характеризуется дозированностью действия, т.е. количественной зависимостью результата его экспрессии от дозы соответствующего аллеля этого гена. Примером может служить зависимость степени нарушения транспортных свойств гемоглобина у человека при серповидно-клеточной анемии от дозы аллеля НЬS. Наличие в генотипе человека двойной дозы этого аллеля, приводящего к изменению структуры β-глобиновых цепей гемоглобина, сопровождается грубым нарушением формы эритроцитов и развитием клинически выраженной картины анемии вплоть до гибели. У носителей только одного аллеля НЬS при нормальном втором аллеле лишь незначительно изменяется форма эритроцитов и анемия не развивается, а организм характеризуется практически нормальной жизнеспособностью.
