Реакции синтеза аммонийных солей
Пути превращений аспартата и глутамата
В организме аспартат и глутамат используются всеми клетками для синтеза пуриновыхи пиримидиновыхоснований. Амидные производные этих аминокислот являются транспортными формамиаммиака из тканей в почки и печень. Кроме этого, глутаминовая кислота входит в состав глутатиона– вещества, выполняющего две различные функции – перенос аминокислот через мембрану и ключевое звено в антиоксидантной системе клетки. Также глутамат и его производное γ-аминомасляная кислота являются медиаторамив ЦНС.
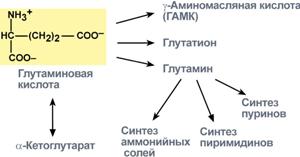 | 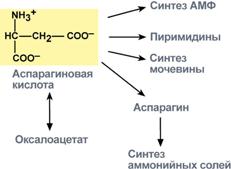 |
| Пути использования глутамата | Пути использования аспартата |
Серин и глицин превращаются друг в друга
Роль реакции превращения серина в глицин состоит в образовании активной формы тетрагидрофолиевой кислоты – N5,N10-метилен-ТГФК.
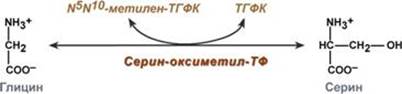
Реакция взаимопревращения глицина и серина
Одновременно данная реакция является первой на пути катаболизма серина.
Несмотря на простоту строения, глицин и серин являются весьма востребованными аминокислотами в клетках. Благодаря взаимопревращению перечень возможных путей метаболизма этих аминокислот еще больше расширяется.
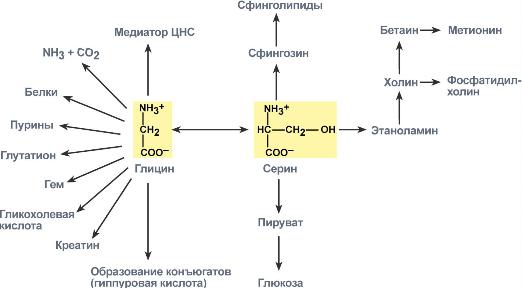
Пути использования серина и глицина
Обмен некоторых аминокислот тесно связан
Образованный в реакции распада серина до глицина N5,N10-метилен-тетрагидрофолат (активная форма витамина В9) при участии фермента метилен-ТГФК-редуктазы превращается в N5-метил-ТГФК. Его метильный остаток участвует в метионин-синтазной реакцииреметилирования гомоцистеина в метионин. В печени, кроме метил-ТГФК, источником метильной группы может быть вещество бетаин (триметилглицин).
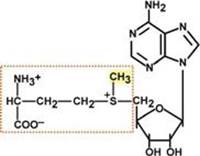
Строение S-аденозилметионина
Метионин впоследствии присоединяет аденозильный остаток и превращается в активную форму метионина – S-аденозилметионин, участвующий во многих реакциях метилирования, в частности, при синтезе креатина, карнитина, фосфатидилхолина, адреналина. В результате перемещения метильной группы и отщепления аденозина остается гомоцистеин, имеющий два пути метаболизма:
Первый путь превращений гомоцистеина – реметилирование до метионина и вновь участие в реакциях метилирования и синтезе веществ.
Второй путь – взаимодействие с серином при участии цистатионин-синтазы, превращение в цистатионин с последующим распадом в цистеин и гомосерин.
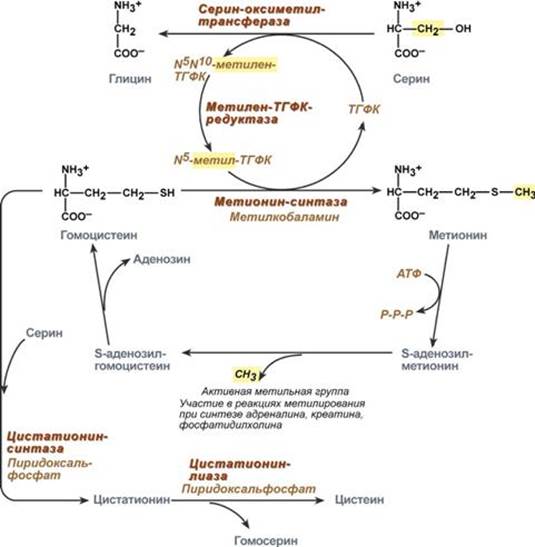
Взаимосвязь обмена серина, глицина, метионина и цистеина
Пути метаболизма цистеина
Цистеин является чрезвычайно важной аминокислотой в связи с тем, что это единственный источник органической серы для клеток организма. В результате реакций метаболизма эта сера переходит в состав других серусодержащих веществ – фосфоаденозинфосфосерная кислота (ФАФС), коэнзим А, глутатион, сульфированные производные углеводов (хондроитинсульфат, кератансульфат, дерматансульфат) или выводится почками в виде сульфатов.
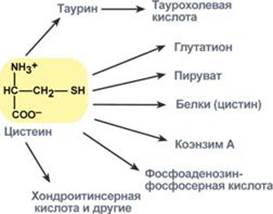
Пути использования цистеина
Одним из производных цистеина является таурин, обладающий следующими функциями:
· является обязательным компонентом желчных кислот
· играет роль внутриклеточного антиоксиданта,
· есть данные о функции таурина как тормозного нейромедиатора.
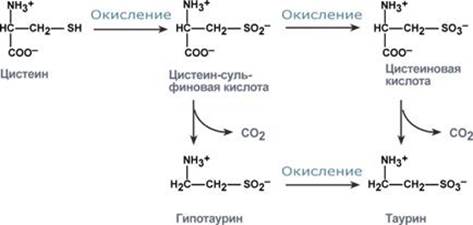
Реакции синтеза таурина
Обмен фенилаланина и тирозина
В организме фенилаланин используется только в синтезе белков. Весь неиспользованный запас аминокислоты превращается в тирозин. В этом непосредственно участвует ферментфенилаланин-4-монооксигеназа (фенилаланингидроксилаза), обеспечивающий окисление ароматического кольца. Кофермент тетрагидробиоптерин в реакции окисляется до дигидроформы. Восстановление кофермента осуществляет дигидробиоптерин-редуктаза с своим коферментом НАДФН.
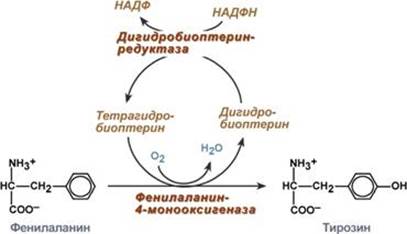
Реакция превращения фенилаланина в тирозин
Тирозин, помимо участия в синтезе белков, является предшественником гормона надпочечниковадреналина, медиаторов норадреналина и дофамина, гормонов щитовидной железы тироксина и трийодтиронина и пигментов.
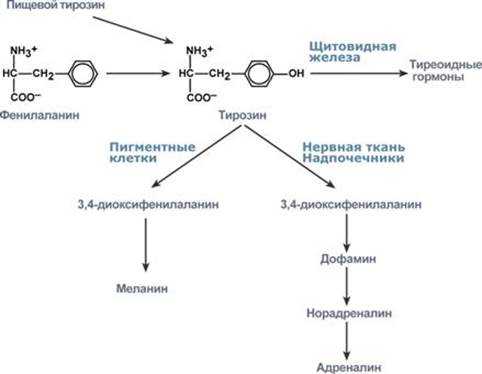
Пути превращения тирозина
