Раздел 4. фазовые равновесия в гетерогенных системах
Диаграмма состояния двухкомпонентных систем сводится к двухмерному графику, где по оси абциссе откладывают концентрацию одного из компонентов, по оси координат – температуру фазовых превращений. Примером такой диаграммы является диаграмма состояния двухкомпоентной системы, компоненты которой образуют простую эвтектику (рис. 1).
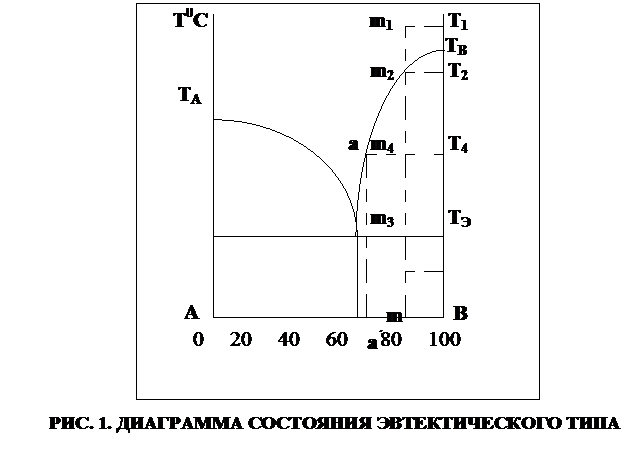
Анализируя диаграмму возможно определить природу и количество образующихся в системе фаз, области их существования и особенности взаимодействия.
Решение типовых задач
Задача 1. Определите качественный и количественный состав системы, обозначенной на рис. 1 точкойm4.
Решение.Данная фигуративная точка находится в области ограниченной линиями ТВ э(линия ликвидус – геометрическое место точек, отвечающих температурам начала кристаллизации расплава и ТЭ э ( линия солидус – линия, отвечающая температурам конца кристаллизации).
Качественный состав любой области диаграммы определяется линиями, ограничивающими эту область. Система, обозначенная на диаграмме т. m4 будет состоять из двух фаз – расплава (на это указывает линия ликвидус ТВэ) и твердый фазы, предоставленной кристаллами компонента В (указывает линия солидус эТЭ и ось состава В).
Количественный состав системы в т.m4 можно определить, если провести горизонтальную линию – конноду до пересчения с линиями, ограничивающими рассматриваемую область Т4а и проходящуючерез т. m4. Точки пересечения конноды укаывают составы двух равновесных при данной температуре фаз. Точка а определяет соста расплава (проектируем ее ось состава а') и отвечает 100% расплава; в точке Т4 – 100% твердой фазы. Для того чтобы определть количество твердой фазы и расплава, весь отрезок (а) принимаем за 100%, точка m4делит его наотрезок m4а и m4Т4. Согласно правилу рычага отрезки обратно пропорциональны массам фаз, на которые распадается равновесная система:
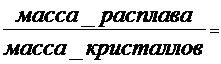 m4Т4 / а m4.
m4Т4 / а m4.
Таким образом, отрезок, прилегающий к линии ликвидус, определяет количество твердой фазы, а отрезок, прилегающий к линии 100% В, определяет количество жидкой фазы.
Задача 2.Рассмотрите фазовые превращения, происходящие при охлаждении расплава данной исходной смеси состоящий из 20% компонентаА и 80% - В.
Решение. Для того чтобы рассмотреть фазовые изменения при охлаждении расплава данной исходной смеси, нужно из фигуративной точки, отвечающей исходному составу, восстановить перпендикуляр так, чтобы попасть в область расплава. Затем необходимо описать процессы, происходящие при температурах, отвечающих точкам пересечения перпендикуляра с линиями диаграммы, т. е. рассмотреть процессы, происходящие при охлаждении данного расплава.
Рассмотрим последовательность фазовых изменений при охлаждении исходной смеси, состоящей из 20% компонентаА и 80% компонента В, нагретой до температуры Т1 (фигуративная точка m1 на рис. 1)
При температуре, отвечающей точке m1, исходная смесь составаm представляет собой расплав. При охлаждении расплава до температуры Т2 ( точка m2 ) из него выпадают первые кристаллы компонента В, при дальнейшем охлаждении количество выпавших кристаллов В будет увеличиваться. При достижении температуры ТЭ из расплава одновременно кристализуются компоненты А иВ.
Процесс одновременной кристаллизации двух компонентов называется эвтектическим, а температура при которой это происходит называется температурой эвтектики.
Ниже температуры эвтектики система будет представлять собой твердую фазу, состоящую из крупных, ранее выпавших, кристаллов В и мелких кристаллов эвтектики ( мелкокристаллическая смесь А и В).
Задачи
для самостоятельного решения
101. Схематически изобразите фазовую диаграмму «состав – температура» бинарной системы А-В, компоненты которой образует простую эвтектику. Укажите состав всех областей диаграммы.
102. Твердая фаза состоит из 20% кристаллов эвтектики и 80% кристаллов компоненита В (рис. 2а). Укажите при какой температуре начнет плавится и какого состава должна быть исходная смесь компонентов АиВ для получения данной твердой фазы.
103.Определите качественный и количественный состав системы, отвечающий точке с диаграммы, изображенной на рис. 2а. Укажите процентное содержание компонентов АиВ в расплаве.
104. Схематически изобразите фазовую диаграмму «состав –температура» бинарной системы А-В, компоненты которой образуют химическое соединение, плавящееся конгруентно. Укажите состав всех областей диаграммы и состав эвтектик.
105.Схематически изобразите фазовую диаграмму «состав –температура» бинарной системы А-В, компоненты которой образуют химическое соединение, плавящиеся инконгруентно. Укажите состав всех областей диаграммы и состав эвтектик.
 |
а
 |
б
 |
в
Рис. 2. Диаграммы состояния двухкомпонентных
Систем различного типа
106. На диаграмме, изображенной на рис. 2а, определите при какой температуре начнет плавиться исходная смесь состоящая из 20% компонента А и 80% компонента В и при какой температуре она полностью расплавится. Укажите состав первых капель расплава.
107. При какой температуре появляются первые кристаллы при охлаждении расплава, отвечающего точке d (рис. 2а), при какой температуре расплав закристаллизуется полностью. Определите состав исходной смеси.
108. На диаграмме, изображенной на рис. 2б определите при какой температуре начнет плавиться исходная смесь, состоящая из 45%А и 55% В и при какой температуре она полностью расплавится. Укажите состав расплава для данной смеси при температуре Т1.
109.Определите при какой температуре появляются первые кристаллы при охлаждении расплава, отвечающего точке d (рис.2б) и температуру при которой расплав полностью закристаллизуется. Укажите какой компонент кристаллизуется первым.
110.На диаграмме, изображенной на рис. 2 в, определите при какой температуре начнет плавится смесь, состоящая из 80 % В и 20 % А и при какой температуре она полностью расплавится. Укажите состав расплава при температуре Т1.
111.Определите какой состав исходной смеси компонентов А и В необходимо взять, чтобы получить сплав, состоящий из 35 % эвтектики и 65 % В. Диаграмма состояния А и В имеет вид представленный на рис. 2а.
112.Опишите процессы, происходящие при охлаждении расплава исходной смеси, состоящей из 10 % компонента В и 90 %, компонента А (рис. 2 в). Укажите состав эвтектики (Э1).
113. Определите качественный и количественный состав системы, отвечающий точке n, изображенной на диаграмме рис.2а. Укажите процентное содержание компонентов А и В в расплаве.
114.Определите качественный и количественный состав эвтектик на диаграме состояния представленной на рис.2б. Укажите состав исходной смеси при охлаждении расплава которой можно получить сплав, состоящий из 15% эвтектики и 85% А.
115. Опишите процессы, происходящие при охлаждении расплава исходной смеси, отмеченной т. С на рис.2в. Укажите температуру при которой исчезают последние капли расплава.
116.Определите качественный и количественный состав системы, обозначенной точкой d на диаграмме рис. 2в. Укажите при какой температуре исчезнут последние капли раствора.
117.Укажите состав исходной смеси, необходимый для получения сплава, состоящего из 40% химического соединения и 6о% компонента В (рис.2в).
118. Опишите процессы, происходящие при охлаждении расплава исходной смеси, состоящей из 50 % компонента В и 50 % компонента А (рис.2в). Определите состав системы при температуре Т2.
119. Какой компонент выкристаллизовывается первым при охлаждении расплава исходной смеси, состоящей из 50 % В и 50 % А (рис.2а). Укажите состав системы при температуре Т1.
120. Определите фазовое состояние системы в каждой области диаграммы, представленной на рис.2в. Укажите температуру, при которой появятся первые капли раствора при нагревании исходной смеси, состоящей из 40 % А и 60 % В.
библиографический список рекомендуемой литературы
Основная
1. Киреев В. А. Курс физической химии. М., 1975.
2. Киселева Е. В., Каретников Г. С., Кудряшов И. В. Сборник примеров и задач по физической химии. М., 1983.
3. Краткий справочник физико – химических величин / Под. ред. А. А. Равделя, А. М. Пономаревой. Л., 1983.
Дополнительная
1. Киреев В. А. Курс физической химии. М., 1978.
2. Справочник химика. Л., 1971.
основные вопросы для подготовки к экзамену
1. Первое начало термодинамики. Функции состояния процесса. Понятие о внутренней энергии.
2. Термодинамические процессы. Энтальпия. Связь qp с qv.
3. Термохимия. Закон Г. Гесса. Теплоемкость.
4. Зависимость теплового эффекта от температуры.
Закон Крихгофа.
5. Второе начало термодинамики.
6. Энтропия. Необратимые процессы.
7. Вычисление абсолютной энтропии.
8. Направленность процессов. Термодинамические потенциалы.
9. Фазовые равновесия. Понятие о фазе, компоненте, степени свободы.
10. Правило фаз Гиббса.
11. Давление пара над раствором. Закон Ф. Рауля.
12. Повышение температуры кипения и понижение температуры замерзания растворов.
13. Сплавы. Диаграммы состояния систем: с простой эвтектикой, с инконгруэнтно - и конгруэнтноплавящимися соединениями.
14. Характеристика силикатов.
15. Термодинамика и термохимия силикатов. Процессы гидратации клинкерных составляющих цементов.
16. Силикатные системы: SiO2 – CаО. Пути кристаллизации.
17. Минералы, образуемые данными оксидами, важнейшие составляющие портландцементов.
18. Поверхностные явления. Поверхностно-активные и поверхностно- неактивные вещества.
19. Улучшение свойств цементов и бетонных растворов за счет применения ПАВ.
Таблица 1
