Скорость гетерогенной химической реакции
В гетерогенной химической реакции взаимодействие реагентов происходит на поверхности раздела фаз.
Скорость гетерогенной реакции измеряется изменением количества какого-либо из веществ, вступающих в реакцию или образующихся в результате ее, за единицу времени на единице поверхности раздела фаз
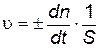 , , | (2.13) |
где n – количество вещества какого-либо компонента реакционной системы, моль; t – время, с; S – площадь поверхности раздела фаз, м2.
Из уравнения (2.13) следует, что скорость гетерогенной химической реакции имеет единицу измерения [моль∙ м -2 ∙с -1]. Гетерогенные химические реакции являются сложными, многостадийными процессами. В ходе гетерогенной реакции можно выделить три характерные стадии.
1. Подвод реагирующих веществ к поверхности раздела фаз.
2. Химическая реакция на поверхности раздела фаз.
3. Отвод продуктов реакции из реакционной зоны.
Скорость суммарного гетерогенного процесса определяется наиболее медленной (лимитирующей) стадией.
Если наиболее медленно протекающими являются первая или третья стадии, связанные с переносом вещества, то скорость такого процесса определяется конвекцией (переносом массы газа или жидкости) или диффузией (самопроизвольным выравниванием концентраций) и практически не зависит от скорости протекания самой химической реакции.
При усилении конвекции скорость возрастает. Так, реакция горения угля протекает тем быстрее, чем интенсивнее подается к углю кислород
C (тв) + O2 (г) = CO2 (г).
При отсутствии конвекционного потока процесс может лимитироваться диффузией. Толщина диффузионного слоя уменьшается при перемешивании. Интенсивное перемешивание увеличивает скорость общего процесса. Например, растворение солей в водных растворах кислот
MgCO3 (тв) + 2 HNO3 (ж) = Mg(NO3)2 (р-р) + H2O (ж) + CO2 (г).
Если скорость переноса веществ больше, чем скорость химического превращения, т.е. наиболее медленной стадией является вторая стадия, то скорость протекания всего процесса определяется собственно химической реакцией и можно применить закон действующих масс.
При этом надо иметь в виду, что реакция протекает на поверхности раздела фаз, поэтому общая скорость химической реакции будет зависеть от концентрации жидкого или газообразного вещества, а также от площади соприкосновения фаз. Концентрация твердого вещества не входит в выражение для скорости реакции.
При измельчении твердого вещества скорость реакции будет возрастать из-за увеличения площади поверхности. Например, скорость реакции
CaCO3 (тв) + 2HCl (р-р) = CaCl2 (р-р) + H2O (ж) + CO2 (г)
зависит от концентрации соляной кислоты и площади поверхности раздела фаз. Скорость реакции порошкообразного карбоната кальция с кислотой выше скорости взаимодействия мраморной крошки с кислотой из-за увеличения площади контакта. Уравнение скорости в общем виде
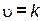 [HCl]m ·S,
[HCl]m ·S,
где m – порядок реакции по кислоте; S – площадь поверхности, м2.
Порядок реакции m может совпадать со значением стехиометрического коэффициента, если лимитирующей стадией процесса является собственно простая химическая реакция.
Зависимость скорости химической реакции
От температуры
Уравнение Аррениуса
В большинстве случаев скорость химической реакции увеличивается при повышении температуры.
Зависимость константы скорости реакции от температуры выражается уравнением Аррениуса
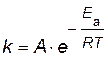 , , | (2.14) |
где k - константа скорости реакции;
A - константа, называемая предэкспоненциальным
множителем;
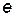 - основание натурального логарифма;
- основание натурального логарифма;
Еa - энергия активации, Дж/моль;
Т - температура, К;
R - газовая постоянная, 8,31 Дж/моль×К.
Энергия активации
Для того чтобы произошла реакция, необходимо преодолеть отталкивание электронных оболочек молекул и разорвать или ослабить связи между атомами. На это надо затратить определенную энергию.
Энергия активации в элементарных реакциях – минимальная энергия реагентов (атомов, молекул и др. частиц), достаточная для того, чтобы они вступили в химическую реакцию, т. е. для преодоления барьера на поверхности потенциальной энергии, отделяющего реагенты от продуктов реакции.
Потенциальный барьер – максимум потенциальной энергии, через который должна пройти система в ходе элементарного акта химического превращения.
В ходе реакции вещества переходят в неустойчивое промежуточное состояние, характеризующееся большим запасом энергии. Это состояние называется активированным комплексом или переходным состоянием. Именно для его образования необходима энергия активации (рис. 4, 5).
Число частиц, входящих в активированный комплекс, определяет молекулярность данной стадии реакции.
Неустойчивый активированный комплекс существует очень короткое время ( 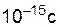 ). Он распадается с образованием исходных веществ или продуктов реакции.
). Он распадается с образованием исходных веществ или продуктов реакции.
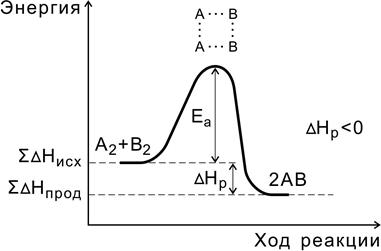
Рис. 4. Энергетическая диаграмма экзотермической реакции
Переходное состояние возникает в ходе как прямой, так и обратной реакций (рис. 6). Разность энергий активации прямой и обратной реакций равна изменению внутренней энергии (тепловому эффекту) реакции
DНр = Еа(пр) - Еа (обр).
В макроскопической химической кинетике энергия активации – параметр Еa, входящий в уравнение Аррениуса (2.14). В общем случае сложных реакций параметр Еa является функцией энергий активации отдельных стадий, и определяемая энергия активации называется эффективной (эмпирической, кажущейся).
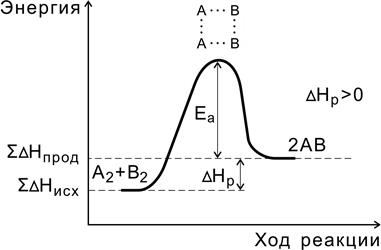
Рис. 5. Энергетическая диаграмма эндотермической реакции
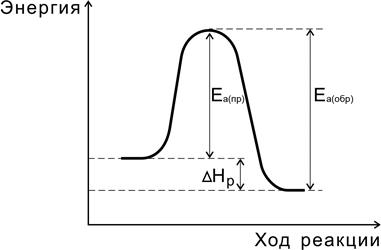
Рис.6. Соотношение между энергиями активации прямой
и обратной реакций и теплового эффекта
2.6.3. Распределение молекул по энергиям
Элементарный акт химической реакции происходит не при любом столкновении молекул, а только при столкновении молекул, которые обладают повышенным запасом кинетической энергии. Молекулы, обладающие такой энергией, называются активными молекулами.
Если сталкивающиеся молекулы не обладают такой энергией, то столкновение будет неэффективным – не приведет к образованию новой молекулы. Если же кинетическая энергия сталкивающихся молекул достаточна, то столкновение может привести к перестройке атомов и образованию молекулы нового вещества.
На рис. 7 показано распределение молекул идеального газа по кинетической энергии согласно статистическому закону Максвелла-Больцмана при двух разных температурах.
Доля молекул с энергией, превышающей энергию активации Еа (доля активных молекул), с повышением температуры резко возрастает (площадь заштрихованной области).
Величина 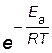 в уравнении Аррениуса (2.14) численно равна доле активных молекул.
в уравнении Аррениуса (2.14) численно равна доле активных молекул.
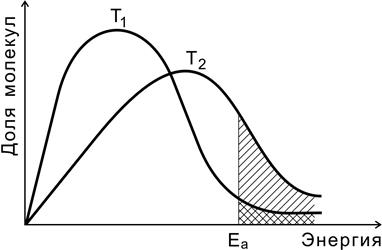
Рис. 7. Распределение молекул по энергиям
при двух разных температурах (Т2 > Т1)
Чем выше температура, тем больше в системе активных молекул, тем выше скорость реакции.
