Упрощенный вывод основного уравнения МКТ
Пусть имеется 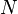 частиц массой
частиц массой 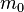 в некотором кубическом сосуде.
в некотором кубическом сосуде.
Так как молекулы движутся хаотически, то события, состоящие в движении в одном из шести независимых направлений пространства, совпадающих с осями декартовой системы координат, равновероятны.
Поэтому, в каждом из этих направлении движется 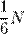 частиц.
частиц.
Пусть все частицы обладают одинаковой скоростью 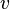 .
.
Каждая из частиц, сталкивающихся со стенкой, передаёт ей импульс 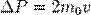 .
.
Если площадь стенки 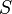 , а концентрация -
, а концентрация - 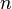 , то количество частиц, сталкивающихся со стенкой за время
, то количество частиц, сталкивающихся со стенкой за время 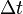 равно
равно 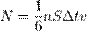 .
.
Так как 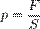 , а
, а 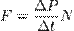 - суммарная сила взаимодействия частиц со стенкой, то подставив соответствующие значения получим
- суммарная сила взаимодействия частиц со стенкой, то подставив соответствующие значения получим 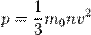 ,
,
так как 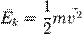 , то
, то 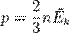 .
.
Уравнение состояния идеального газа (уравнениеМенделеева — Клапейрона) — формула, устанавливающая зависимость между давлением,молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
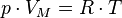 ,
,
где
-
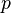 — давление,
— давление, -
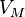 — молярный объём,
— молярный объём, -
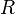 — универсальная газовая постоянная
— универсальная газовая постоянная -
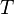 — абсолютная температура, К.
— абсолютная температура, К.
Так как 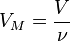 , где
, где 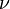 — количество вещества, а
— количество вещества, а  , где
, где 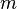 — масса,
— масса, 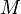 — молярная масса, уравнение состояния можно записать:
— молярная масса, уравнение состояния можно записать:
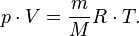
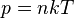 где
где 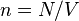 - концентрация атомов,
- концентрация атомов, 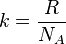 - постоянная Больцмана.
- постоянная Больцмана.
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
Уравнение, выведенное Клапейроном, содержало некую неуниверсальную газовую постоянную  , значение которой необходимо было измерять для каждого газа:
, значение которой необходимо было измерять для каждого газа:
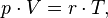
Менделеев же обнаружил, что  прямо пропорциональна
прямо пропорциональна 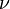 , коэффициент пропорциональности
, коэффициент пропорциональности 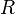 он назвал универсальной газовой постоянной.
он назвал универсальной газовой постоянной.

Законы идеальных газов:
Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным.
1. Изохорический процесс. Закон Шарля. V = const.
Изохорическим процессом называется процесс, протекающий при постоянном объёме V. При постоянном объёме и неизменных значениях массы газа и его молярной массы, отношение давления газа к его абсолютной температуре остаётся постоянным: P/Т = const.
График изохорического процесса на РV-диаграмме называется изохорой. Уравнение изохоры:
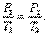 | (1.4.1) |
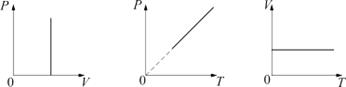
2. Изобарический процесс. Закон Гей-Люссака. Р = const.
Изобарическим процессом называется процесс, протекающий при постоянном давлении Р. Поведение газа при изобарическом процессе подчиняется закону Гей-Люссака:
При постоянном давлении и неизменных значениях массы и газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const.
График изобарического процесса на VT-диаграмме называется изобарой.
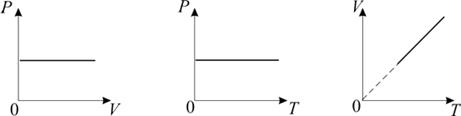
Уравнение изобары:
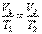 | (1.4.3) |
3. Изотермический процесс. Закон Бойля – Мариотта. T = const.
Изотермическим процессом называется процесс, протекающий при постоянной температуре Т.
Поведение идеального газа при изотермическом процессе подчиняется закону Бойля – Мариотта:
При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const.
График изотермического процесса на РV-диаграмме называется изотермой.
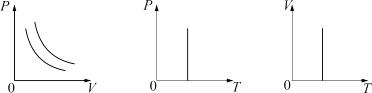
Уравнение изотермы:
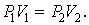 | (1.4.5) |
4. Адиабатический процесс (изоэнтропийный):
Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой.(Q=0)
5. Политропический процесс. Процесс, при котором теплоёмкость газа остаётся постоянной. Политропический процесс – общий случай всех перечисленных выше процессов.(c=const)
6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA=6,02·1023молекул (число Авогадро).
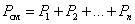 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов:
7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов:
| (1.4.6) |
Парциальное давление Pn – давление, которое оказывал бы данный газ, если бы он один занимал весь объем.
При 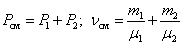 , давление смеси газов:
, давление смеси газов:
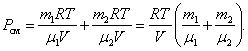 | (1.4.7) |
8. Объединённый газовый закон (Закон Клапейрона).
В соответствии с законами Бойля – Мариотта (1.4.5) и Гей-Люссака (1.4.3) можно сделать заключение, что для данной массы газа
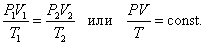 |
21)
Термодинамической системой называется совокупность макроскопических тел, которое могут обмениваться энергией между собой и с внешней средой(т.е. с другими телами).
Термодинамическая система может находиться в различных состояниях, отличающихся температурой, давлением, объемом, плотностью и т.д. Подобные величины, характеризующие состояние системы, называются термодинамическими параметрами состояния.
Состояние термодинамической системы будет равновесным, если все параметры состояния имеют определенные значения, не изменяющиеся с течением времени(неравновесным – если хотя бы один из параметров не имеет определенного значения).
Термодинамическим процессом называется переход системы из одного состояния в другое. Данный переход связан с изменением равновесия системы.
При бесконечно медленном сжатии давление газа будет иметь в каждый момент времени определенное значение. Следовательно, состояние газа все время будет равновесным , так что бесконечно медленный процесс окажется состоящим из последовательности равновесных состояний. Такой процесс называется равновесным или квазистатическим.
При изменении направления равновесного процесса система будет проходить через те же равновесные состояния, что и при прямом ходе, но в обратной последовательности. Поэтому равновесные процессы называют также обратимыми.
Процесс, при котором система после ряда изменений возвращается в исходное состояние, называется круговым процессом или циклом.
Исходя из определения идеального газа, в нем отсутствует потенциальная составляющая внутренней энергии (отсутствуют силы взаимодействия молекул). Таким образом, внутренняя энергия идеального газа представляет собой только кинетическую энергию движения его молекул.
Энергия одной молекулы равна E=ikT/2, соответственно энергия всего газа будет равна энергии одной молекулы, умноженной на количество всех частиц: U=NikT/2
Рассмотрим газ, который находится под поршнем в цилиндрическом сосуде.
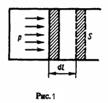
Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние dl, то он осуществляет над ним работу
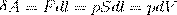
где S — площадь поршня, Sdl=dV— изменение объема газа. Таким образом,
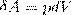 (1)
(1)
Полную работу А, которую совершает газ при изменении его объема от V1 до V2, найдем интегрированием формулы (1):
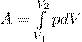 (2)
(2)
Найденное для работы выражение (2) справедливо при любых изменениях объема твердых, жидких и газообразных тел.
Энергия, которую получает или теряет тело в процессе теплообмена с окружающей средой, называется количеством теплоты(обозначается Q).
Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами.
Первый закон термодинамики: Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и совершение системой работы над внешними телами. (т.е. Q=∆U+A)
Воображаемое устройство, совершающее работу в цикле и не заимствуя энергию извне, называется вечным двигателем 1 рода. Первый закон термодинамики заключается в том, что невозможно существование вечного двигателя 1 рода.
22)
Теплоёмкость
Теплоёмкость тела (обычно обозначается латинской буквой C) — физическая величина, определяемая отношением бесконечно малого количества теплоты δQ, полученного телом, к соответствующему приращению его температуры δT:
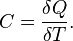
[C]=Дж/К
Удельной теплоёмкостьюназывается теплоёмкость, отнесённая к единичному количеству вещества. Количество вещества может быть измерено в килограммах, кубических метрах и молях. В зависимости от того, к какой количественной единице относится теплоёмкость, различают массовую, объёмную и молярную теплоёмкость.
Объёмная теплоёмкость (С′) — это количество теплоты, которое необходимо подвести к единице объёма вещества, чтобы нагреть его на единицу температуры. В СИ измеряется в джоулях на кубический метр на кельвин (Дж·м−3·К−1).
Молярная теплоёмкость (Сμ) — это количество теплоты, которое необходимо подвести к 1 молю вещества, чтобы нагреть его на единицу температуры. В СИ измеряется в джоулях на моль на кельвин (Дж/(моль·К)).
