Окислительно-восстановительное титрование: иодометрия, хлориодометрия, иодатометрия, нитритометрия, перманганатометрия, дихроматометрия, цериметрия. Применение в фармацевтическом анализе.
Основано на окислительных или восстановительных свойствах анализируемых веществ и титрантов. В процессе титрования происходит изменение окислительно-восстановительных потенциалов взаимодействующих систем. Если разность этих потенциалов большая, то возможно прямое титрование.В фармацевтическом анализе применяется перманганатометрия, йодометрия, хлориодометрия, йодатометрия, броматометрия, дихроматометрия, цериметрия.
ПЕРМАНГАНАТОМЕТРИЯ основана на реакции: МnО4- + 8Н+ + 5е → Мn2+ + 4Н20. При прямом титровании индикатор не добавляют, им является титрант, избыток которого придает раствору розовое окрашивание. Прямое титрование используется для определения восстановленного железа, препаратов пероксида водорода. В случае медленного протекания ок.-восст. процесса применяется обратное титрование. Например, при определении нитрита натрия, левомицетина. Избыток титранта оттитровывают йодометрически.
ИОДОМЕТРИЯ основана на использовании окислительных свойств свободного йода и восстановительных свойств йодид-ионов: I2 + 2е → 2I-
Методом йодометрии количественно определяют неорганические и органические ЛВ, способные окисляться или восстанавливаться, а также образовывать с йодом продукты замещения. Свободный йод, образовавшийся в избытке при обратном йодометрическом титровании, оттитровывают тиосульфатом натрия:
I2 + 2Nа2S2О3 → 2NаI + Nа2S4О6.
Индикатор − раствор крахмала, образующий с йодом синее соединение. Прямое титрование йодом применяют для определения тиосульфата натрия и препаратов мышьяка (III), хлоралгидрата, формальдегида, никодина, метазида, фурацилина, изониазида, метионина, анальгина и др.
ХЛОРИОДОМЕТРИЯ используют раствор йодмонохлорида, получаемый из йода и йодата калия в кислой среде. Согласно ГФ РБ рекомендуют для количественного определения лактата этакридина, можно определять фенолы, сульфаниламиды и другие первичные ароматические амины. Избыток титранта раствора йодмонохлорида оттитровывают йодометрически: IСl + КI →I2 + КСl.
ИОДАТОМЕТРИЮ используют для определения фтивазида, апрессина, аскорбиновой кислоты. Метод основан на использовании в качестве титранта раствора йодата калия КIO3, который в кислой среде является сильным окислителем. В основе метода лежит химическая реакция:IO3-+ 6H+ +6e →I-+ 3H2O.
ДИХРОМАТОМЕТРИЯ использует в качестве титранта раствор дихромата калия. Титрование выполняется в среде серной, соляной или фосфорной кислот. Применение этого метода основано на реакции:
2 (R3N • Н)+Сl- + К2Сr2О7 → [R3N • Н]2Сг2O7↓ + 2КС1.
После отделения осадка фильтрованием избыток титранта в фильтрате опр-ют йодометрическим методом: К2Сr2О7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 3I2 + 4K2SO4 + 7Н20.
Выделившийся йод титруют раствором тиосульфата натрия.
ЦЕРИМЕТРИЯ основана на применении титрованного раствора солей церия (IV), которые в кислой среде восстанавливаются до церия (III): Се4+ + е = Се3+
Метод предложен для определения содержания неорганических соединений, таких, как железо (II), мышьяк (III), и органических лекарственных веществ (углеводов, органических кислот, викасола, производных фенотиазина).
НИТРИТОМЕТРИЯ использует в качестве титранта раствор нитрита натрия. Метод применяется гл. обр. для определения органических лекарственных веществ. Основана на реакциях диазотирования или нитрозирования. Первичные ароматические амины образуют с нитритом натрия в среде соляной кислоты диазосоединение Ar—NH2 + NaNO2 + 2HCl → [Ar—N+≡N)C1- + NaCl + 2H20.
Вторичные ароматические амины в таких же условиях образуют нитрозоамины
ТЭ устанавливают с помощью внешних (йодкрахмальной бумаги) и внутренних (тропеолина ОО, нейтрального красного) индикаторов, потенциометрически. Для ускорения прибавляют катализатор — кристаллический бромид калия. Область применения нитритометрии—определение сульфаниламидных препаратов, производных п-аминобензоиной кислоты.
39.Комплексометрия. Комплексометрическое титрование – группа титриметрических методов анализа, основанных на реакциях образования растворимых комплексных соединений. Комплексонометрия - титриметрический метод, основанный на реакциях комплексонообразования ионов металлов с комплексонами. Комплексонами назыв-ся органические соединения в мол-лах кот имеются основные и кислотные группы, обеспечив-х образование прочных растворимых в воде комплексов (хелатов) с ионами различных металлов. Титрант- комплексон III, трилон Б, ЭДТА-динатриевая соль кислоты этилендиаминотетрауксусной кислоты. Точку эквивалентности устанавливают с помощью металлоиндикаторов ( это органич-е красители, образующие с ионами титруемого металла окрашенные комплексы).Применяют индикатор- эриохром черный Т. Комплексы металлов с эриохромом черным имеют красный цвет, поэтому для получения четкого перехода цвета (красный-синий) необходимо проводить титрование с эриохромом в щелочной среде(рН 7-11). Меркуриметрическое титрование – титриметрический метод анализа, основанный на образовании растворимых комплексных соединений ртути (II). Основная область применения меркуриметрического титрования - определение галогенид-ионов. В качестве титранта в меркуриметрическом титровании используют Hg(NO3)2. Стандартный раствор этого вещества является вторичным. Исходным веществом для его приготовления служит Hg(NO3)2⋅H2O. Данное вещество плохо растворимо в воде, поэтому его растворяют в небольшом количестве азотной кислоты. После того как соль растворится, раствор разбавляют водой до нужного объёма. Для стандартизации используют NaCl или стандартный раствор NH4SCN. ИНДИКАТОРЫ, ИСПОЛЬЗУЕМЫЕ В МЕРКУРИМЕТРИИ: Дифенилкарбазон, Нитропруссид натрия, Меркуриметрия является альтернативным (по отношению к аргентометрии) методом определения галогенидов и достаточно широко используется в фармацевтическом анализе, в особенности при контроле качества лекарственных средств непосредственно в аптеках. Этот метод, во-первых, более дешёвый, а, во-вторых, позволяет использовать прямое титрование для анализа кислых растворов. Основной его недостаток заключается в токсичности титранта.
39 Осадительное титрование - группа титриметрических методов анализа, основанных на реакциях образования малорастворимых соединений, выделяющихся из раствора в виде осадка. Аргентометрическим титрованием называется титриметрический метод анализа, основанный на образовании малорастворимых соединений серебра. Основным титрантом в аргентометрии является AgNO3. Аргентометрия используется для определения галогенидов, тиоцианатов, цианидов, фосфатов и других ионов. Способы обнаружения конечной точки титрования Для обнаружения конечной точки титрования в аргентометрии могут быть использованы визуальные или инструментальные методы. Визуальные методы традиционно называют по их авторам. Метод Мора:В данном методе в качестве индикатора для обнаружения конечной точки титрования используется хромат калия. Хромат калия в
аргентометрии представляет собой осадительный индикатор. Осадительными индикаторами называются вещества, выделяющиеся из раствора в виде осадка в хорошо заметной форме в точке эквивалентности или вблизи неё.
Метод Мора не используется для определения иодид- и тиоцианат ионов. Осадки AgI и AgSCN адсорбируют большое количество хромат- ионов, поэтому чёткое обнаружение конечной точки титрования становится невозможным. При использовании метода Мора в растворе не должны присутствовать катионы (например, Ba2+), образующие малорастворимые окрашенные хроматы. Метод Фольгарда: В методе Фольгарда в качестве индикатора применяют железоаммонийные квасцы. Титрование по Фольгарду проводят в сильнокислой среде для того, чтобы препятствовать образованию окрашенных гидроксокомплексов Fe(III) из бесцветного аква-комплекса [Fe(H2O)6]3+. Для создания кислой среды используют HNO3 (или H2SO4). Концентрация HNO3 в титруемом растворе должна быть не менее 0,3 моль/л.
Метод ФаянсаВ данном методе для обнаружения конечной точки титрования используют адсорбционные индикаторы. Адсорбционными индикаторами называются вещества, адсорбция или десорбция которых осадком сопровождается изменением окраски в точке эквивалентности или вблизи неё. В качестве адсорбционных индикаторов в аргентометрическом титровании чаще всего используют флуоресцеин и его галогенопроизводные (дихлорфлуоресцеин, эозин, флоксин, эритрозин), а также сульфофталеины (бромфеноловый синий), родамины (родамин 6G). Применение в фармацевтическом анализе: аргентометрия по экономическим соображениям применяется в фармацевтическом анализе не слишком широко. В фармакопейном анализе количественное определение органических лекарственных веществ, содержащих галогенид-ионы, обычно проводят методом кислотно-основного титрования в среде уксусной кислоты. В аптечном анализе такие вещества чаще определяют меркуриметрически. Аргентометрию применяют для количественного определения галогенидов натрия и калия и некоторых органических галогенпроизводных (после их гидролиза в соответствующих условиях). Аргентометрия может быть использована также для определения органических веществ, образующих малорастворимые серебряные соли, например, барбитуратов, сульфаниламидов, теофиллина и др.
40. Атомно-эмиссионная спектрометрия. Применение в фармацевтическом анализе.
Атомно-эмиссионная спектроскопия (АЭС) - спектроскопический метод анализа, основанный на измерении электромагнитного излучения оптического диапазона, испускаемого термически возбуждёнными свободными атомами или одноатомными ионами.
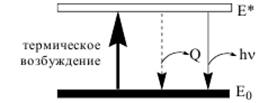 При действии на атом тепловой энергии один из электронов переходит на более высокий энергетический уровень, а затем (через ~ 10-8 с), возвращаясь в основное состояние, испускает поглощённую энергию в виде кванта электромагнитного излучения определённой длины волны либо отдаёт её в виде теплоты при столкновении с другими атомами
При действии на атом тепловой энергии один из электронов переходит на более высокий энергетический уровень, а затем (через ~ 10-8 с), возвращаясь в основное состояние, испускает поглощённую энергию в виде кванта электромагнитного излучения определённой длины волны либо отдаёт её в виде теплоты при столкновении с другими атомами
Атомный спектр испускания, также как и спектр поглощения, состоит из множества отдельных линий различной интенсивности, соответствующих различным возможным электронным переходам. Наиболее вероятными являются испускательные переходы с ближайшего к основному электронного уровня. Такие переходы называются резонансными. Соответствующие им линии в спектре имеют самую большую интенсивность и чаще всего используются для практических целей.
 Приборы, используемые в атомно-эмиссионной спектроскопии, имеют следующие основные узлы
Приборы, используемые в атомно-эмиссионной спектроскопии, имеют следующие основные узлы
Роль атомизатора заключается не только в получении свобод-
ных атомов, но и в переводе атомов в возбуждённое состояние. Вследствие этого атомизация в АЭС проводится в более жёстких условиях, чем в ААС. В качестве атомизаторов используют:
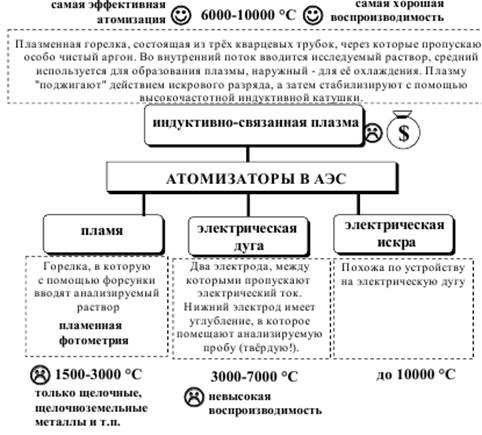 В качестве устройства для выделения необходимого спектраль-
В качестве устройства для выделения необходимого спектраль-
ного интервала из получаемого спектра испускания используют мо-
нохроматоры: дифракционные решётки или призмы. В пламенной
фотометрии получаемые спектры содержат мало линий, поэтому для
выделения требуемого спектрального интервала используют светофильтры. АЭС используется для обнаружения и количественного опре-
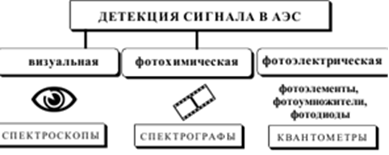 деления различных элементов, обычно металлов. В качественном анализе используется наличие характерных линий в получаемых спектрах испускания. Наиболее подходящий атомизатор для качественного анализа - дуговой разряд, так как пламя даёт спектры бедные спектральными линиями, атомизатор с ИСП - наоборот, очень сложные спектры, которые можно расшифровать только с помощью компьюте-
деления различных элементов, обычно металлов. В качественном анализе используется наличие характерных линий в получаемых спектрах испускания. Наиболее подходящий атомизатор для качественного анализа - дуговой разряд, так как пламя даёт спектры бедные спектральными линиями, атомизатор с ИСП - наоборот, очень сложные спектры, которые можно расшифровать только с помощью компьюте-
ра. Количественный анализ в АЭС основан на зависимости интенсивности испускания от концентрации данного элемента в анализируемой пробе.
Предел обнаружения в АЭС при определении хорошо атомизируемых и легковозбудимых элементов с использованием пламенного атомизатора составляет 10-7-10-2%, других элементов (ИСП-атомизатор) - 10-8 - 10-2%.
41. Молекулярную абсорбционную спектроскопию в УФ- и видимой областях спектра называют спектрофотометрией либо фотометрией.
При поглощении электромагнитного излучения УФ- или видимого диапазона молекула переходит из некоторого колебательного и вращательного состояния основного электронного уровня в некоторое колебательное и вращательное состояние следующего электронного уровня. Группы, обуславливающие появление полос поглощения в молекулярных спектрах, называются хромофорами. Атомы или группы атомов, которые сами по себе не обуславливают появление полос поглощения, но влияют на характер поглощения хромофоров, называются ауксохромами. Объектами исследования в фотометрии обычно являются растворы. Принцип измерения аналитического сигнала заключается в сравнении интенсивности двух световых потоков, один из которых проходит через исследуемый раствор, а второй - через раствор сравнения. В спектрофотометрии используют следующие приёмы анализа: прямая фотометрия, основанная на измерении собственного поглощения вещества; определение, основанное на проведении фотометрических реакций, в том числе экстракционная фотометрия; дифференциальная фотометрия; многоволновая спектрофотометрия; производная спектрофотометрия; фотометрическое титрование. Практическое применение и основные приёмы фотометрического анализа Спектрофотометрия является одним из самых широко применяемых и наиболее разработанных инструментальных методов анализа. К её достоинствам относятся достаточно высокая чувствительность (НГОС для хорошо оглощающих веществ составляет примерно 10-6 - 10-7 моль/л), универсальность, простое аппаратурное оформление, возможность автоматизации анализа и т.д.
42 ИК-спектроскопия. Если молекула поглощает ИК-излучение, то она переходит изодного колебательного состояния в другое. При обычной температуре химические связи в молекуле не являются жёсткими, а, в результате взаимодействия молекулы с другими молекулами, испытывают постоянные колебания.
ИК-спектр поглощения представляет собой зависимость степени поглощения (А или Т) электромагнитного излучения от его волновой характеристики (как правило, волнового числа). ИСТОЧНИКИ ИК-ИЗЛУЧЕНИЯ штифт Нернста и глобар. Принцип детектирования ИК-излучения заключается в измерении изменения температуры зачернённого материала, расположенного на пути потока.
Практическое применениеИК-спектроскопия используется преимущественно для установления строения и идентификации органических (реже неорганических) соединений, в том числе и лекарственных веществ. В плане качественного анализа ИК-спектры являются значительно более информативными, чем спектры поглощения в УФ- или видимой области. Большинство функциональных групп (OH-, NH2 и т.п.) не обладают собственным поглощением в УФ- и видимой области. Напротив, в ИК-спектрах они имеют собственные полосы поглощения. Кроме того, в УФ-спектре отдельные полосы поглощения часто сливаются друг с другом, что затрудняет его интерпретацию. Обнаружение и идентификация веществ методом ИК-спектроскопии может проводиться следующим образом: обнаружение отдельных функциональных групп по характеристическим полосам поглощения, сравнение ИК-спектров исследуемого соединения и стандартного образца, идентификация неизвестного соединения с помощью атласа или компьютерной библиотеки ИК-спектров. В количественном анализе ИК-спектроскопия используется значительно реже, чем спектроскопия в УФ- и видимой области. Это связано с тем, что чувствительность данного метода анализа существенно ниже (величины обычно составляют 1-1103), а воспроизводимость хуже.
