Повреждение эндоплазматической сети
Реакции ЭПС на повреждение
ü Гипертофия/гиперплазия ЭПС – увеличение его количества, расширение канальцев с появлением необычного содержимого;
ü Вакуольная дегенерация (лизис ЭПС);
ü Атрофия/гипоплазия – упрощение структуры, появление аномальных рибосомально-пластических комплексов.
Последствия повреждения ЭПС
Повреждение ЭПС, независимо от его причины, вызывает ряд типовых патогенетических последствий (рис. 11):
ü Дезинтеграция гранулярной ЭПС (отсоединение рибосом от мембраны);
ü Нарушение внутриклеточного транспорта белков;
ü Белковая дистрофия клеток (мутное набухание, зернистая дистрофия);
ü Активация ОСФ;
ü Гипертрофия гладкой ЭПС;
ü Усиление дезинтоксикационных возможностей клетки;
ü Аутоокисление.
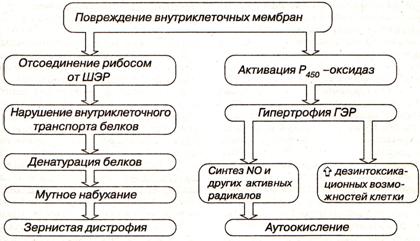
Рис. 11 – последствия повреждения ЭПС
Повреждение пластинчатого комплекса
(аппарат Гольджи)
Реакции пластинчатого комплекса на повреждение
1. Гиперплазия/гипертрофия пластинчатого комплекса – увеличение площади его мембран и количества секреторных гранул.
Причины: болезни печени, гипертрофия ЭПС.
2. Атрофия пластинчатого комплекса – редукция (уменьшение) вакуолей и потеря секреторных гранул.
Причины: токсикозы, белковое голодание.
Последствия повреждения пластинчатого комплекса
ü Повышение секреторной функции и синтеза белка, повреждение мембран, накопление белка в цитоплазме;
ü Патология лизосом (лизосомные болезни).
Повреждение лизосом
Патологическая активность лизосом зависит в основном от двух факторов: состояния (стабилизации) мембран лизосом и активности их ферментов.
А) Дестабилизация (лабилизация) мембран лизосом – повышение проницаемости, появление трещин и разрывов.
Причины: ▪ ионизирующая радиация;
▪ шок;
▪ гиповитаминозы;
▪ бактериальные эндотоксины.
Патогенез: выход гидролаз в цитоплазму ведет к аутолизу и некрозу клетки.
Б) Стабилизация мембран лизосом – уменьшение проницаемости.
Причины: противовоспалительные и антибактериальные препараты; антиоксиданты.
Патогенез: повышение резистентности клеток к патогену (анормальные и растянутые лизосомы).
В) Недостаток лизосомальных ферментов (лизосомные болезни, болезни накопления) – замедление или остановка разрушения метаболитов при их нормальном синтезе: гликогенозы, липидозы, гепатозы.
Общая черта лизосомных болезней: нарушение психомоторного развития и иммунитета.
Повреждение пероксисом
Увеличение их числа в гепатоцитах описано при применении медикаментов, снижающих уровень липидов в крови, вирусном гепатите, лептоспирозе, в кардиомиоцитах при длительном воздействии этанола. Уменьшение числа пероксисом и снижение синтеза их ферментов наблюдается в печени при воспалении, а также при опухолевом росте. Разрушение пероксисом отмечается при гиперлипидемии и гиперхолестеринемии
Последствия повреждения пероксисом
1. Наследственный дефект, связанный с отсутствием пероксисом, абсолютно смертелен и приводит к гибели молодняка через несколько месяцев при явлениях иммунодефицита и гипоксии.
2. Альтерация пероксисом способствует образованию свободных радикалов => нарушение утилизации жирных кислот (формирование детергентов) => омыление клетки и разрушение мембран (эндогенный детергентный эффект).
Набор заданий для проверки достижения конкретных целей обучения:
Тестовые задания:
- Укажите последствия увеличенного содержания внутриклеточного кальция при ишемическом повреждении клетки:
a) активация фосфолипаз, интенсификация перекисного окисления липидов, нарушение энергетической функции митохондрий;
b) повышение резистентности клетки к патогену, замедление разрушения метаболитов
- Денатурация белков и белково-липидных комплексов клетки специфична для повреждения …
a) термическим фактором;
b) химическим фактором;
c) механическим фактором;
d) лучевым фактором.
- Блокирование клеточных рецепторов и угнетение активности клеточных ферментов специфично для повреждения…
a) термическим фактором;
b) химическим фактором;
c) механическим фактором;
d) лучевым фактором.
- Укажите последствия выраженного ацидоза при ишемическом повреждении кардиомиоцитов:
a) угнетение Ca++-транспортирующей функции саркоплазматического ретикулума, активация перекисного окисления липидов, снижение сократительной функции миофибрилл;
b) активация Na+/K+-АТФ-азы и ферментов креатинкиназной системы, инактивация лизосомальных протеаз и фосфолипаз.
- Механизмы повреждения клетки:
a) повышение сопряженности окислительного фосфорилирования и активности ферментов системы репарации ДНК;
b) усиление свободнорадикального окисления липидов, выход лизосомальных ферментов в гиалоплазму, экспрессия онкогена
- Прямыми последствиями снижения pH в поврежденной клетке являются:
a) активация лизосомальных фосфолипаз и протеаз, снижение синтеза ДНК, повышение проницаемости и лизосомальных мембран, изменение конформационных свойств мембранных белков;
b) повышение сопряженности окислительного фосфорилирования и активности ферментов системы репарации ДНК.
- Назовите главные механизмы повреждения клетки при чрезмерном действии УФ-лучей:
a) активация фосфолипаз, интенсификация перекисного окисления липидов, нарушение генетического аппарата клетки;
b) гиперполяризация цитоплазматической мембраны, образование ковалентных сшивок между липидными и белковыми молекулами
- Какое действие на мембраны клеток оказывают амфифильные соединения в высоких концентрациях:
a) повышают проницаемость мембраны клетки, агрегируют в мицеллы и внедряются в мембрану, вытесняют ионы кальция из мембраны, разрушают липидный бислой мембраны клетки;
b) понижают проницаемость клеточной мембраны и внутриклеточный рН, стабилизизуют мембрану органоидов клетки.
- Назовите основные причины активации фосфолипаз при повреждении клетки:
a) повышение внутриклеточного содержания ионов кальция, снижение внутриклеточного pH, интенсификация перекисного окисления липидов;
b) активация Na+/K+-АТФ-азы и ферментов креатинкиназной системы, инактивация лизосомальных протеаз и фосфолипаз.
- Укажите органеллы, защищающие клетку от чрезмерного накопления в ней ионизированного кальция:
a) митохондрии, саркоплазматический ретикулум;
b) рибосомы, лизосомы;
c) центриоли и вакуоли.
- Какими ионами, главным образом, активируются в поврежденной клетке мембраносвязанные фосфолипазы:
a) Ca++;
b) H+;
c) Na+
12. Какими ионами, главным образом, активируются в поврежденной клетке фосфолипазы и протеазы лизосом
a) Ca++;
b) H+;
c) Na+
- Какие из перечисленных веществ ослабляют повреждающее действие свободных радикалов на клетку:
a) глютатионпероксидаза, супероксиддисмутаза, препараты селена, витамин Е;
b) ионол, убихиноны, радикалы липидов, нитроксиды.
- Какие из перечисленных ниже веществ обладают свойствами антиоксидантов:
a) токоферолы, каталаза, глютатионпероксидаза, препараты селена;
b) нитроксиды, убихиноны, фосфолипиды, агликозидазы.
- Чем сопровождается увеличение содержания свободного ионизированного кальция в клетке:
a) активацией фосфолипазы А2, активацией перекисного окисления липидов, увеличением выхода K+ из клетки, гипергидратацией клетки;
b) снижением проницаемости клеточной мембраны и внутриклеточного рН, стабилизизацией мембраны органоидов клетки.
- Назовите последствия активации перекисного окисления липидов (ПОЛ) клеточных мембран:
a) уменьшение гидрофобности липидов, изменение конформации рецепторных белков, увеличение внутриклеточного содержания ионов кальция, нарушение структурной целостности цитоплазматической мембраны,
b) повышение сопряженности окислительного фосфорилирования и активности ферментов системы репарации ДНК.
- Укажите «неспецифические» проявления повреждения клетки:
a) денатурация молекул белка, усиление перекисного окисления липидов, инактивация мембраносвязанных ферментов;
b) лабилизация мембран лизосом, ацидоз, выделение медиаторов, нарушение барьерной функции мембраны клетки.
- Способствует ли усиление процессов перекисного окисления липидов в поврежденной клетке улучшению ее энергообеспечения:
a) нет;
b) да.
- Могут ли ионы кальция влиять на процессы перекисного окисления липидов:
a) нет;
b) да.
Ситуационные задачи:
Задача 1.
С целью моделирования гемолитической анемии мышам ввели фенилгидразин, который избыточно активирует в клетках свободнорадикальные реакции. Через полчаса после введения фенилгидразина в крови животных обнаружено снижение количества эритроцитов, присутствие свободных форм Hb и метгемоглобина.
Вопрос. Каковы возможные механизмы повреждения мембран эритроцитов?
Ответ. Фенилгидразин активирует генерацию избытка активных форм кислорода (супероксидного радикала и его производных) с последующим образованием липидных радикалов и гидроперекисей. Возникающие при этом повреждения бимолекулярного фосфолипидного слоя мембран характеризуются образованием в них брешей (кластеров повышенной проницаемости) и снижением эффективности работы мембранных ионных насосов. Это ведёт к накоплению избытка Nа+ в эритроцитах с увеличением внутриклеточного осмотического давления. В результате происходит гипергидратация и гемолиз эритроцитов.
Задача 2.
В лаборатории исследовали клеточные эффекты вещества, входящего в состав отходов одного из химических производств. Вещество вносили в монокультуру нормальных эпителиальных клеток в токсической концентрации. Наличие признаков повреждения клеток оценивали каждые 30 мин на протяжении 3 ч. Через 3 ч инкубации выявили гибель 85% клеток.
Вопросы и задание:
1. Какие морфологические и биохимические критерии Вы можете предложить для оценки обратимого («А») и необратимого («Б») повреждения эпителиальных клеток в данном эксперименте?
2. Назовите последовательность патологических изменений в клетке и их механизмы (основываясь на предложенных Вами критериях оценки повреждения клеток.
Ответы
1.А. Признаками обратимого повреждения клетки (и методами их выявления) являются:
· умеренное увеличение объёма клеток (определяется морфологически),
· накопление лактата во внеклеточной среде (выявляется биохимическими методами),
· увеличение концентрации К+ во внеклеточной среде (выявляется пламенной фотометрией),
· снижение мембранного потенциала (определяется электрофизиологическими методами),
· распад полисом (выявляется морфологически),
· снижение активности митохондриальных ферментов (определяется био- и гистохимически).
1.Б. К признакам необратимого повреждения клеток тносят:
· нарушение целостности плазматических мембран,
· распад ядер,
· деструкцию митохондрий,
· повышение рН клетки с развитием внутриклеточного алкалоза,
· увеличение сорбционных свойств клеток (определяется радиоактивным методом — обычно используется радиоактивный технеций 99),
· накопление в клетках белков внеклеточного происхождения (выявляется гистофлюоресцентным методом),
· наличие в инкубационной среде ферментов цитозольного (лактатдегидрогеназа) и митохондриального (креатинфосфокиназа) происхождения.
2. Нарушение энергетического обмена в клетках сопровождается накоплением избытка К+ и лактата в инкубационной среде. Это обусловлено снижением эффективности работы ионных насосов, активацией гликолиза, уменьшением ингибирующего действия АТФ на ключевые ферменты гликолиза.
Снижение содержания гликогена свидетельствует о стимуляции гликогенолиза. Одновременно с этими процессами происходит набухание клеток вследствие их гипергидратации, вызванной аккумуляцией в клетках Na+, фосфата и лактата. Уменьшение мембранного потенциала связано с накоплением в клетках Na+ и Са2+.
Активность митохондриальных ферментов подавлена вследствие их прямого повреждения или альтерации мембран токсичным агентом. Эти процессы обратимы и могут прекращаться после отмывки токсичного препарата.
В дальнейшем могут происходить необратимые изменения, которые характеризуются деструкцией плазматических мембран. Это приводит к выходу из клеток ферментов и накоплению в них экстраклеточных белков.
О необратимом повреждении клеток могут свидетельствовать также накопление в них технеция, распад митохондрий и ядер, повышение внутриклеточного рН вследствие накопления избытка азотистых оснований.
