Опыт 3. Количественное определение активности аланинаминотрансферазы (АлАТ) в сыворотке крови.
1. В две пробирки внесите реактивы согласно следующей таблице:
| Контрольная проба | Опытная проба | |
| Реагент 1 (АлАТ, субстрат), мл | 0,25 | 0,25 |
| Дистиллированная вода, мл | 0,05 | – |
| Сыворотка, мл | – | 0,05 |
| Перемешать и инкубировать 30 мин | ||
| Реагент 2 (динитрофенилгидразин), мл | 0,25 | 0,25 |
| Перемешать и оставить при комнатной температуре на 20 мин | ||
| NaOH (С = 0,4 моль/л), мл | 2,5 | 2,5 |
2. Перемешайте и через 10 минут измерьте оптическую плотность пробы против контрольной пробы при длине волны 540 нм, кювета с толщиной слоя 5 мм.
3. Активность АлАТ в опытной пробе определите по калибровочному графику в нмоль/с×л.
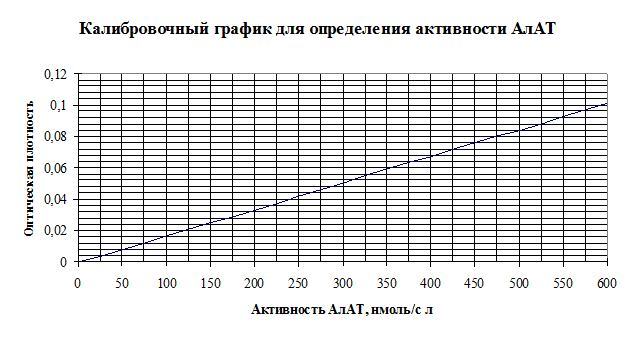
Сравните полученный результат с физиологическими величинами и сделайте вывод. Опишите механизм работы кофермента трансаминаз.
Опыт 2. Белки как противоядие от ионов тяжелых металлов.
Взаимодействие ионов металлов с белками лежит в основе использования молока как противоядия при отравлении тяжелыми металлами.
Приборы. 1. Штатив с пробирками.
2. Набор пипеток.
3. Водяная баня.
Реактивы. 1. Амилаза, раствор.
2. Крахмал, 1%-ный раствор.
3. Ацетат свинца, 1%-ный раствор.
4. Молоко.
5. Дистиллированная вода.
6. Йод, 1%-ный раствор.
1. В опытную пробирку налейте по 1 мл раствора амилазы, 1%-ного раствора крахмала, 1%-ного раствора ацетата свинца (II) и молока.
2. В контрольную пробирку налейте по 1 мл растворов амилазы, крахмала, ацетата свинца (II) и воды.
3. Пробирки встряхните и выдержите 20 минут при температуре 30°С.
4. Добавьте в обе пробирки по 1 капле 1%-ного раствора йода.
Объясните полученные результаты.
Расчетные методы определения биологической ценности белка.
Продукция животноводства в целом, в первую очередь, представляет ценность как источник белка в рационе человека. Основным фактором, определяющим биологическую ценность белков пищи, является их аминограмма, т.е. количественное соотношение содержащихся в белке аминокислот, в первую очередь восьми незаменимых для человека – лизина, лейцина, изолейцина, метионина, триптофана, фенилаланина, валина и треонина.
Один из способов определения биологической ценности (БЦ) белков пищи основан на коэффициенте различия аминокислотного скора (КРАС, %). Он показывает среднюю величину избытка аминокислотного скора незаменимых аминокислот по сравнению с наименьшим уровнем скора какой-либо незаменимой аминокислоты. Аминокислотный скор определяют по формуле:
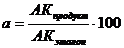
где АКпродукт – содержание незаменимой аминокислоты в 1 г исследуемого белка, мг; АКэталон – содержание той же аминокислоты в 1 г «идеального» (эталонного) белка, мг; 100 – коэффициент пересчета в проценты.
На базе данных, полученных рядом исследователей в ходе обменных опытов, международной организацией ФАО/ВОЗ (ФАО - продовольственная и сельскохозяйственная организация ООН; ВОЗ - Всемирная организация здравоохранения) был предложен следующий
ЭТАЛОН
содержания незаменимых аминокислот в пищевом белке:
| Аминокислота | Содержание в г на 100 г белка |
| Изолейцин | 4,0 |
| Лейцин | 7,0 |
| Лизин | 5,5 |
| Серосодержащие аминокислоты (метионин + цистеин) | 3,5 |
| Ароматические аминокислоты (фенилаланин + тирозин) | 6,0 |
| Треонин | 4,0 |
| Триптофан | 1,0 |
| Валин | 5,0 |
Лимитирующей биологическую ценность аминокислотой считается та, скор которой наименьший.
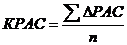
где ∆РАС – избыток скора аминокислоты; n – количество незаменимых аминокислот.
∆РАС = Сi - Сmin
где Сi – избыток скора аминокислоты;
Сmin - минимальный из скоров незаменимых аминокислот исследуемого белка по отношению к эталону, %.
Биологическую ценность (БЦ) пищевого белка (%) определяют по формуле:
БЦ = 100 – КРАС
Содержание незаменимых (для человека) аминокислот
