Повышение невосприимчивости населения
Мероприятия III группы направлены на увеличение «иммунной прослойки» популяции. Наиболее эффективный метод - широкомасштабная активная иммунопрофилактика (вакцинация) различных инфекционных болезней.
В соответствии с эффективностью проводимых мероприятий по предупреждению инфекционных заболеваний выделяют управляемые инфекции (для их предупреждения эффективно используют вышеуказанные мероприятия) и неуправляемые инфекции (меры предупреждения отсутствуют).
Введение вакцины (иммунопрофилактика) - мероприятие, направленное на повышение невостприимчивости населения. По интенсивности эпидемических процессов выделяют спорадическуюзаболеваемость, эпидемии и пандемии.
Спорадическая заболеваемость - единичные, как бы не связанные между собой случаи болезни (не более 10 на 100 тыс. населения).
Эпидемическая заболеваемость (эпидемия) - групповая заболеваемость ( 20-100 на 100 тыс. населения).
Пандемия- массовое распространение инфекционной болезни на большие территории.
В соответствии с распространенностью инфекционные заболевания также выделяют повсеместные(убиквитарные) и эндемичные инфекции,выявляемые на определенных, нередко небольших территориях.
Экзотические болезни - не свойственные данной территории. Они могут быть следствием завоза возбудителей инфицированными людьми или животными, с пищевыми продуктами или различными изделиями.
Конвенционные(карантинные) болезни - наиболее опасные болезни, склонные к быстрому распространению, например, чума, холера, оспа, желтая лихорадка. Система информации и меры профилактики в этих случаях обусловлены международными соглашениями (конвенцией).
Факторы неспецифической защиты. Антигены и их свойства.ФАКТОРЫ НЕСПЕЦИФИЧЕСКОЙ ЗАЩИТЫ (ВРОЖДЕННЫЕ) Под неспецифическим иммунитетомподразумевают систему предсуществующих защитных факторов организма, присущих данному виду как наследственно обусловленноесвойство.Так, собаки никогда неболеют чумой человека, а куры - сибирской язвой. Иммунитет, создаваемый анатомическими, физиологическими, клеточными и молекулярными факторами, которые являются естественными составляющими элементами организма, иначе называют конституционным. Такие факторы защищают организм от разных экзогенных и эндогенных агрессий, они передаются наследственно, их защитные функции лишены избирательности и они не способны сохранять память от первичного контакта с чужеродностью.
Условно факторы неспецифической защиты можно разбить на четыре типа: физические (анатомические); физиологические; клеточные, осуществляющие эндоцитоз или прямой лизис чужеродных клеток; молекулярные (факторы воспаления). Физические (анатомические) барьеры
Кожа. Неповрежденная кожа представляет собой обычно непроницаемый барьер для микроорганизмов. Лишь при некоторых инфекционных болезнях, например, лептоспирозах, прямое проникновение возбудителя через неповрежденную кожу, возможно, является первичным путем заражения. Здоровая неповрежденная кожа обладает отчетливой бактерицидной активностью в отношении тех микроорганизмов, которые не являются представителями ее нормальной микрофлоры.
Слизистые оболочки. На уровне слизистых оболочек существует множество разных механизмов защиты внутренней среды организма, в том числе от проникновения в нее м/о (слизь, реснички мерцательного эпителия, лизоцим, пероксидазы, секреторные антитела, фагоцитирующие клетки, лимфоциты).
Нормальная микрофлора организма. Микроорганизмы, которые населяют кожу и слизистые оболочки, сообщающиеся с внешней средой, составляют нормальную микрофлору организма. Эти микроорганизмы способны противостоять действию патогенных микроорганизмов и губительно действовать на них, тем самым участвуя в защите организма. Физиологические барьеры
Этот тип защиты включает температуру тела, рН и напряженность кислорода в районе колонизации микроорганизмами, а также различные растворимые факторы, воспаление. Клеточные факторы
К клеточным факторам неспецифической защиты относятся фагоцитирующие клетки и натуральные киллеры.
Фагоцитирующие клетки. Одним из мощных факторов резистентности являетсяфагоцитоз. И.И.Мечников установил, что фагоцитарными свойствами обладают зернистые лейкоциты крови и лимфы, главным образом полиморфноядерные нейтрофилы (микрофаги - нейтрофилы, эозинофилы и базофилы) и по-другому обозначаются как полиморфноядерные лейкоциты, или гранулоциты, а также моноциты и различные клетки ретикулоэндотелиальной системы, которую он назвал макрофагами. В настоящее время под макрофагами понимают клетки, которые обладают высокой фагоцитарной активностью. Они различаются по форме и размерам, в зависимости от тканей, где они обнаруживаются. По классификации ВОЗ все макрофаги объединены всистему мононуклеарных фагоцитов (СМФ).
Фагоцитам присущи трифункции:
- Защитная. Фагоцитозом уничтожаются чужеродные объекты, т.е. происходит очистка организма от инфекционных агентов, продуктов распада, отмирающих клеток, неметаболизируемых органических веществ.
- Секреторная. Взаимодействие объекта фагоцитоза с фагоцитом стимулирует бактерицидные системы последнего. К основным системам бактерицидности относят окислительную (О2-зависимую) и неокислительные (ферментные). Окислительная бактерицидная система убивает микроб за счет прямого действия продуцируемых фагоцитом О2, ОН и Н2О2 или галогенизацию. Из ферментных систем самым сильным бактериологическим потенциалом обладают лизоцим и катепсин.
Кроме того фагоциты синтезируют и секретируют множество цитокинов - биологически активных веществ, необходимых для поддержания иммунного ответа организма на чужеродное вещество.
- Представляющая. Переработка антигена (процессинг) и представление его иммунокомпетентным клеткам, принимающим участие в формировании иммунного ответа.
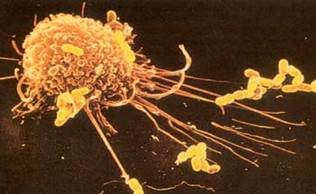 Рис. 1. Фагоцитирующая клетка захватывает бактерии (электронная микрофотография).Процесс фагоцитоза складывается из следующих стадий:
Рис. 1. Фагоцитирующая клетка захватывает бактерии (электронная микрофотография).Процесс фагоцитоза складывается из следующих стадий:
- Хемотаксис - продвижение фагоцита к объекту фагоцитоза, осуществляется с помощью псевдоподий.
- Адгезия (прикрепление). На мембране фагоцитов размещены различные рецепторы для захвата микроорганизмов.
- Эндоцитоз (поглощение). Принципы поглощения бактерий идентичны таковым у амеб: захваченные частицы погружаются в протоплазму и в результате образуетсяфагосома с заключенным внутри объектом.
- Внутриклеточное переваривание. К фагосоме устремляются лизосомы, затем оболочки фагосомы и лизосомы сливаются и ферменты лизосом изливаются в фаголизосому. Фагоцитированные микроорганизмы подвергаются атаке комплекса различных микробицидных факторов.
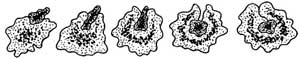
Рис. 2. Последовательность фагоцитоза.
Завершенность фагоцитарных реакций. Микробицидный потенциал фагоцитирующих клеток эффективен против большей части патогенных микроорганизмов (завершенный фагоцитоз), но некоторые возбудители резистентны к его действию и способны длительно существовать внутри фагоцитов. Многие факультативные и облигатные внутриклеточные паразиты не только сохраняют жизнеспособность, но и способны размножаться внутри клеток. В этом случае фагоцитоз остаетсянезавершенным.
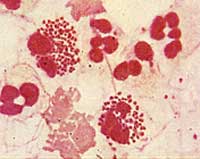 Рис. 3. Незавершенный фагоцитоз. Менингококки (мелкие диплококки) в большом количестве находятся внутри фагоцитов в жизнеспособном состоянии.Для полноценного фагоцитоза нужен фагоцитарный стимул определенной силы:
Рис. 3. Незавершенный фагоцитоз. Менингококки (мелкие диплококки) в большом количестве находятся внутри фагоцитов в жизнеспособном состоянии.Для полноценного фагоцитоза нужен фагоцитарный стимул определенной силы:
А. Микробные факторы. При низком соотношении микроб/ фагоцит (1:1) реакция почти отсутствует. Увеличение соотношения до 25:1 несколько стимулирует процесс, при соотношении до 60:1 фагоцитируется около 80% микробов, но дальнейшее увеличение соотношения резко подавляет фагоцитоз.
Б.Универсальными стимуляторами фагоцитов являются опсонизированные частицыи иммунные комплексы.
Опсонизация - процесс, облегчающий фагоцитоз. Обусловлен связыванием опсонинов (антител и компонента С3b комплемента) с поверхностными антигенами бактерий.
В.Лимфокины, гамма-интерферон - медиаторы, продуцируемые активированными Т-лимфоцитами в местном клеточно-опосредованном иммунном ответе, активируют макрофаги и привлекают другие провоспалительные клетки.
Для характеристики активности фагоцитоза введен фагоцитарный показатель. Для определения его подсчитывают под микроскопом число бактерий, поглощенных одним фагоцитом.Натуральные киллеры.
Натуральные киллеры (НК или NK)или естественные киллеры (ЕК) представляют собой популяцию лимфоидных клеток, лишенных признаков Т- и В-лимфоцитов. Их участие в неспецифическом иммунном ответе состоит в способности оказывать прямое цитотоксическое действие на злокачественнотрансформированные и вирусинфицированные клетки, а также клетки, поглотившие некоторые внутриклеточные бактериальные патогены. . В процессе цитолиза различают три основных стадии: распознавание, выделение цитотоксинов («летальный удар») и лизис клетки-мишени.
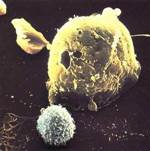 Рис. 4. Клетка-киллер (меньшая клетка внизу) атакует опухолевую клетку. Гуморальные (молекулярные) факторы неспецифической защиты
Рис. 4. Клетка-киллер (меньшая клетка внизу) атакует опухолевую клетку. Гуморальные (молекулярные) факторы неспецифической защиты
В неспецифическом иммунитете против микробов участвуют белки острой фазы воспаления: С-реактивный протеин (белок), сывороточный амилоид, альфа2-макроглобулин, фибриноген, b-лизины, интерфероны, система комплемента, лизоцим и др. Система комплемента.
Система комплемента это комплекс растворимых белков и белков клеточной поверхности, взаимодействие которых опосредует разные биологические эффекты:
- разрушение (лизис) клеток,
- привлечение лейкоцитов в очаг инфекции или воспаления (хемотаксис),
- облегчение фагоцитоза (опсонизация),
- стимуляция воспаления и реакций гиперчувствительности (анафилотоксины).Большая часть компонентов комплемента синтезируются гепатоцитами и мононуклеарными фагоцитами. Компоненты комплемента циркулируют в крови в неактивной форме. При определенных условиях самопроизвольный каскад ферментативных реакций ведет к последовательной активации каждого из компонентов системы комплемента. Компоненты комплемента обозначают латинской буквой С и арабскими цифрами (С1, С2 .... С9).
Существуют два взаимосвязанных пути активации комплемента: классический и альтернативный. В результате формируется мембраноатакующий комплекс, который способен пенетрировать (формирование поры) клеточную мембрану и вызывать лизис микроорганизмов.
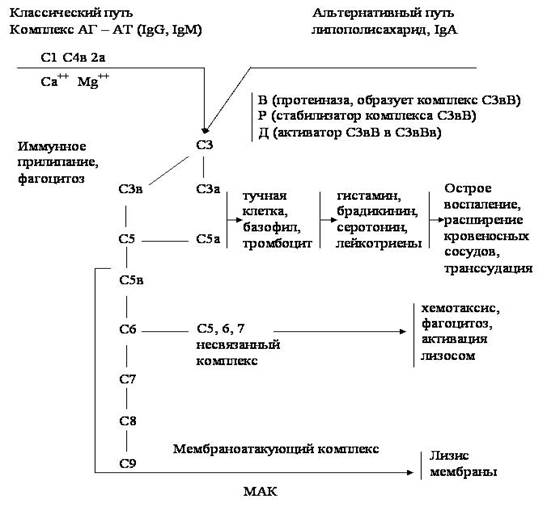
Рис. 5. Активация белков комплемента (схема). Интерфероны.
Интерфероны (ИФН или IFN) представляют собой разновидность специфических гликопротеинов, которые оказывают множество биологических эффектов широкого спектра, вырабатываются многими клетками в ответ на внедрение вируса или сложных биополимеров. Интерферон, образованный клетками человека, функционально активен только в организме человека, но не животных, и наоборот, т.е. обладает видовой специфичностью.
Выделяют три главных класса интерферонов: альфа-интерферон вырабатывают В-лимфоциты, его получают из лейкоцитов крови (лейкоцитарный); бетта-интерферон получают при заражении вирусами культуры клеток фибробластов человека (фибробластный) и гамма-интерферон получают из иммунных Т-лимфоцитов, сенсибилизированных антигенами (иммунный).
Действие интерферона не связано с непосредственным влиянием на вирусы или клетки, т.е. интерферон не действует вне клетки. Адсорбируясь на поверхности клетки или проникая внутрь клетки, он через геном клетки влияет на процессы репродукции вируса или пролиферацию клетки (активирует синтез ферментов и ингибиторов, блокирующих трансляцию вирусных иРНК, тем самым предохраняя соседние клетки от вирусной инфекции).
Значение интерферонов. Интерфероны играют большую роль в поддержании резистентности к вирусам, поэтому его применяют для профилактики и лечения многих вирусных инфекций. Антипролиферативное действие, особенно гамма-интерферона, используют для лечения злокачественных опухолей, а иммуномодулирующее действие - для коррекции работы иммунной системы с целью ее нормализации при различных иммунодефицитах. Лизоцим.
Лизоцим - термостабильный белок типа муколитического фермента. Он содержится в тканевых жидкостях животных и растений, у человека - в слезах, слюне, перитонеальной жидкости, плазме и сыворотке крови, в лейкоцитах, материнском молоке и др. Лизоцим продуцируется моноцитами крови и тканевыми макрофагами. Он вызывает лизис многих сапрофитных бактерий, оказывая менее выраженное литическое действие на ряд патогенных микроорганизмов и неактивен в отношении вирусов.
И другие гуморальные факторы.
АНТИГЕНЫ И ИХ СВОЙСТВА Первоначально термин антиген (от англ. Antibodi generator) применяли для обозначения любой молекулы, индуцирующей образование В-клетками специфических антител. Однако теперь этот термин имеет более широкий смысл, обозначая любую молекулу, которую могут специфически распознавать элементы системы приобретенного иммунитета, т.е. В-клетки или Т-клетки, либо и те и другие.
Антиген - это инициатор и движущая сила всех реакций приобретенного иммунитета. Иммунная система возникла для распознавания и разрушения чужеродных агентов, а также устранения источника их образования - бактерий, инфицированных вирусом клеток и т.п. Когда антиген элиминирован, иммунный ответ прекращается.
Антигены -вещества различного происхождения, несущие признаки генетической чужеродности и вызывающие развитие иммунных реакций (гуморальных, клеточных, состояние иммунной толерантности, индуцирование иммунной памяти). Свойства антигена определяются комплексом признаков: иммуногенность, антигенность, специфичность.
Иммуногенность- способность антигена индуцировать в организме иммунный ответ.
Антигенность- способность антигена взаимодействовать только с гомологичными антителами и лимфоцитами определенного клона.
Специфичность- структурные особенности, отличающие один антиген от другого.
Способность вызывать развитие иммунного ответа и определять его специфичность обладает фрагмент молекулы антигена - антигенная детерминанта (эпитоп), избирательно реагирующая с антигенраспознающими рецепторами и антителами. Молекула антигена может иметь несколько эпитопов, то есть быть поливалентной. Чем сложнее молекула антигена и чем больше у нее эпитопов, тем больше вероятность развития иммунной ответа.
Иммуногены или полные антигены -это вещества, вызывающие полноценный иммунный ответ и обладающие свойствами: иммуногенностью, антигенностью и специфичностью. Иммуногенами являются биополимеры - белки, их комплексы с углеводами (гликопротеиды), а также сложные полисахариды, липополисахариды с высокой молекулярной массой. Чем дальше от человека в эволюционном отношении отстоят организмы, тем бoльшую иммуногенность проявляют их белки.
Гаптены - неполные антигены, относительно простые вещества, способные участвовать в иммунологических взаимодействиях, но не способные самостоятельно индуцировать иммунный ответ. Гаптены обладают свойствами антигенностью и специфичностью, но не обладают иммуногенностью.
Гаптены после присоединения к крупным, обычно белковым молекулам (носителям), могут приобретать свойства полного антигена.
Толерогены - антигены, способные подавлять иммунные реакции с развитием специфической неспособности отвечать на них. АНТИГЕНЫ МИКРООРГАНИЗМОВ Большинство возбудителей инфекционных заболеваний человека, их структуры и токсины - полноценные антигены, вызывающие развитие иммунных реакций. Антигены бактерий.
По расположению в бактериальной клетке выделяют антигены: Капсульный антиген - К Ag Жгутиковый антиген - H Ag Соматический антиген - O AgО-Аг большинства бактерий представлены термостабильным липополисахаридно-полипептидным комплексом; у грамотрицательных бактерий О-Аг представляет эндотоксин.
Н-Аг представлен термолабильным белком флагеллином.
К-Агбольшинства бактерий имеют полисахаридную природу. По чувствительности к температуре К-Аг подразделяются на А-, В- и L-антигены. Наиболее термостабильными являются А-Аг, выдерживающие кипячение более 2 часов. В-Аг выдерживают нагревание при температуре 60°С в течение часа, а L-Аг разрушаются при нагревании до 60°С.
Для идентификации выделенных микроорганизмов в лаборатории применяют внутривидовую или внутриродовую дифференциацию микроорганизмов, основанную на различиях в антигенной структуре. При этом символически отображают антигенную структуру бактерий в виде антигенной формулы. Например, антигенную формулу одного из сероваров E. coli, вызывающую колиэнтериты у детей раннего возраста обозначают как О55:К5:Н21 (серовар, относящийся к серогруппе О55).
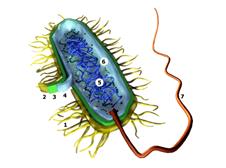 Рис. 1. Антигены бактерий: О-антиген (3 - клеточная стенка); Н-антиген (7 - жгутик); К-антиген (2 - капсула). Антигены вирусов
Рис. 1. Антигены бактерий: О-антиген (3 - клеточная стенка); Н-антиген (7 - жгутик); К-антиген (2 - капсула). Антигены вирусов
В каждом вирионе любого вируса содержатся различные антигены. Одни из них являются вирусспецифическими. В состав других антигенов входят компоненты клетки хозяина (липиды, углеводы), которые включаются в его внешнюю оболочку. Антигены простых вирионов связаны с их нуклеокапсидами. По своему химическому составу они принадлежат к рибонуклеопротеидам или дезоксирибонуклеопротеидам, которые являются растворимыми соединениями и поэтому обозначаются как S-антигены (solutio - раствор). У сложноорганизованных вирионов одни антигенные компоненты связаны с нуклеокапсидами, другие - с гликопротеидами внешней оболочки. Многие простые и сложные вирионы содержат особые поверхностные V-антигены - гемагглютинин и фермент нейраминидазу.
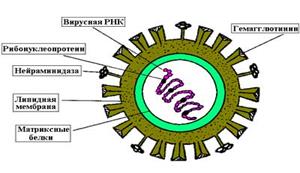
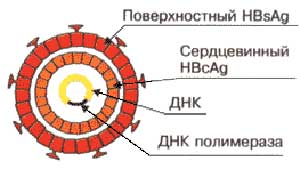
Рис. 2. Антигены вирусов гриппа (слева) и гепатита В (справа) поверхностные (V-антигены) и серцевинные (S-антигены).АНТИГЕНЫ ОРГАНИЗМА ЧЕЛОВЕКА Все ткани и клетки организма человека обладают антигенными свойствами. Одни антигены специфичны для всех млекопитающих, другие видоспецифичны для человека, третьи - для отдельных групп, их называют изоантигенами (например, антигены групп крови). К антигенам, свойственным только данному организму относятся антигены тканевой совместимости Изоантигены
Изоантигены или групповые антигены - это антигены, по которым отдельные индивидуумы или группы особей одного вида различаются между собой.
В эритроцитах, лейкоцитах, тромбоцитах, а также в плазме крови людей открыто несколько десятков изоантигенов.
Изоантигены, генетически связаны, объединены в группы, получившие название: система АВО, резус и др. В основе деления людей на группы по системе АВО лежит наличие или отсутствие на эритроцитах антигенов, обозначенных А и В. В соответствии с этим все люди подразделены на 4 группы. Группа I (О) - антигены отсутствуют, группа II (А) - в эритроцитах содержится антиген А, группа III (В) - эритроциты обладают антигеном В, группа IV (АВ) - эритроциты обладают обоими антигенами. Поскольку в окружающей среде имеются микроорганизмы, обладающие такими же антигенами (их называют перекресно-реагирующими), у человека имеются антитела к этим антигенам, но только к тем, которые у него отсутствуют. К собственным антигенам организм толерантен. При переливании крови или эритроцитов реципиенту, в крови которых содержатся антитела к соответствующему антигену, в сосудах происходит агглютинация перелитых несовместимых эритроцитов, что может вызвать шок и гибель реципиента.
У части людей эритроциты содержат еще особый антиген, получивший название резус-антигена (Rh). По наличию или отсутствию Rh-антигена люди разделяются на две группы - резус (Rh)-положительных и резус (Rh)-отрицательных. При переливании крови Rh-отрицательному реципиенту, если эритроциты донора содержат Rh-антиген, может развиваться гемолитическая желтуха. Факторы специфической защиты. Антитела.ФАКТОРЫ СПЕЦИФИЧЕСКОЙ ЗАЩИТЫСреда организма защищена от проникающих в нее чужеродных макромолекул, в том числе от патогенных микробов, механизмами специфического иммунного ответа. Эти механизмы приобретаются организмом после контакта с конкретным чужеродным веществом, носящим название антиген.Действие этих механизмов строго избирательно и распространяется только на конкретный антиген, который индуцировал иммунный ответ. Реализация иммунного ответа является функцией высоко специализированной иммунной системы организма. Основные защитные функции иммунной системы - распознавание и элиминацию чужеродных макромолекул - осуществляют иммунокомпетентные клетки (лимфоциты), а также продуцируемые и секретируемые ими макромолекулы-антитела (иммуноглобулины).
Специфический иммунный ответ является одним из компонентов общей системы защиты организма, в которой все вышеперечисленные клетки и макромолекулы взаимосвязаны. Местом функциональной кооперации всех перечисленных клеток и макромолекул служат органы и ткани иммунной системы организма. Лимфоциты - это единственные клетки организма, способные специфически распознавать и различать разные антигены и отвечать активацией на контакт с определенным антигеном.
Лимфоциты находятся в состоянии рециркуляции, т.е. постоянно происходит обмен клетками между кровью, лимфой и лимфоидными органами. Это необходимо для реализации специфического иммунного ответа, так как иммунная система должна быть готова ответить на любой из множества чужеродных антигенов, попадающих в любой участок тела. Поскольку каждый отдельный антиген распознается лишь очень небольшой частью популяции лимфоцитов, только постоянная рециркуляция может создать условия для встречи каждого антигена с единичными лимфоцитами, несущими специфические для него антиген-распознающие рецепторы.
Встретив и распознав этот антиген, лимфоциты размножаются (пролиферация) и дифференцируются, благодаря клональной селекции. Большая часть из них принимает непосредственное участие по уничтожению антигена, а меньшая часть остается в виде долгоживущих активированных клеток памяти и в данный момент участие в защите не принимает.Рис. 1. Клональная селекция лимфоцитов (схема). После антигенной стимуляции лимфоциты размножаются и дифференцируются. Большая часть из них активно участвуют в уничтожении антигена, а меньшая остается в виде долгоживущих клеток памяти.При весьма сходной морфологии малые лимфоциты делятся на две популяции, имеющие различные функции и продуцирующие разные белки. В зависимости от места созревания в организме подразделяются на Т-(тимус) иВ- (бурса Фабрициуса, костный мозг) лимфоциты. 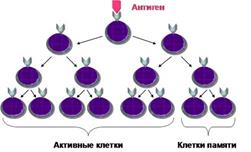 В-лимфоциты
В-лимфоциты
Каждая В-клетка генетически запрограммирована на синтез поверхностного рецептора иммуноглобулиновой природы(иммуноглобулиновые антигенраспознающие рецепторы), специфичного к одному определенному антигену. Встретив и распознав этот антиген, В-клетки размножаются и дифференцируются в плазматические клетки, которые образуют и выделяют в растворимой форме большие количества таких рецепторных молекул, называемых антителами. Антитела представляют собой крупные гликопротеины и содержатся в крови и тканевой жидкости. Благодаря своей идентичности исходным рецепторным молекулам они взаимодействуют с тем антигеном, который первоначально активировал В-клетки.
Рис. 2. В-лимфоциты после антигенной стимуляции размножаются и дифференцируются в плазматические клетки (ПК), которые образуют и выделяют антите. Т-лимфоциты
Другая популяция получила название Т-лимфоциты в связи с их дифференцировкой в тимусе. Имеются несколько субпопуляций Т-клеток с различными функциями. Одни взаимодействуют с мононуклеарными фагоцитами, способствуя разрушению локализованных в них микроорганизмов. Другие взаимодействуют с В-клетками, помогая им размножаться, созревать и образовывать антитела. Обе эти субпопуляции Т-клеток названы хелперными Т-клетками (Тх) и для них характерен поверхностный маркер CD4+. Первые из них обозначаются как Тх1 (Th1)-клетки, они участвуют в реализации реакции гиперчувствительности замедленного типа (ГЗТ) и способны синтезировать ИЛ-2, ИФНg и лимфотоксин, а вторые обозначаются - Тх2 (Th2)-клетки и продуцируют ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-10. Таким образом Т-хелперы являются индукторами (активаторами) иммунных реакций.
Третья субпопуляция Т-клеток осуществляет разрушение клеток организма, зараженных вирусами или иными внутриклеточно размножающимися патогенными микробами. Этот тип активности Т-клеток назван цитотоксичностью, а сами клетки соответственно цитотоксическими Т-лимфоцитами (ТЦТЛ или ТCTLили Тц) или Т-киллерами (Тк), они имеют маркер CD8+.
Свои функции воздействия на другие клетки Т-лимфоциты осуществляют путем выделения растворимых белков - цитокинов, которые передают сигналы другим клеткам, или путем прямых межклеточных контактов. В цитотоксической реакции атакующая клетка направляет содержимое своих гранул наружу, к клетке-мишени. Гранулы цитотоксических Т-клеток содержат соединения, называемые перфоринами, которые способны создавать каналы в наружной мембране клеток-мишеней. (Подобно этому, антитела, связавшись с поверхностью клетки-мишени, могут привлечь комплемент для перфорирования ее цитоплазматической мембраны). Кроме того гранулы содержат лимфотоксины, которыми цитотоксические лимфоциты, путем введения через проделанное отверстие в мембране, лизируют клетку-мишень. Некоторые цитотоксические клетки способны также своим сигналом включать программу саморазрушения клетки-мишени - процесс апоптоза.
Как правило, распознавание антигена Т-клетками происходит только при том условии, что он презентирован на поверхности других клеток в ассоциации (комплексе) с молекулами МНС. В распознавании участвует специфичный к антигену Т-клеточный рецептор(ТкР или TCR), функционально и структурно сходный с той поверхностью молекулы иммуноглобулина, которая у В-клеток служит антигенсвязывающим рецептором. При этом Т-хелперы распознают антиген в ассоциации с МНС II класса, Т- киллеры - с МНС I класса. 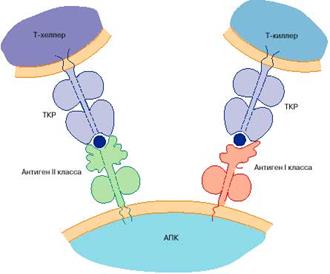 После антигенной стимуляции Т-лимфоциты в результате пролиферативного размножения и дифференцировки могут в виде небольшой группы долгоживущих клеток памяти (как Тх, так и Тц) оставаться в организме в качестве резерва и при повторной встрече с данным антигеном быстро и эффективно уничтожать его.
После антигенной стимуляции Т-лимфоциты в результате пролиферативного размножения и дифференцировки могут в виде небольшой группы долгоживущих клеток памяти (как Тх, так и Тц) оставаться в организме в качестве резерва и при повторной встрече с данным антигеном быстро и эффективно уничтожать его.
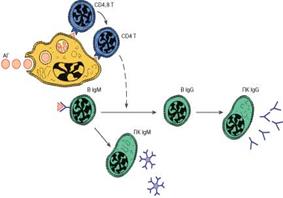 Рис. 3. Рецепторы, встроенные в мембрану эритроцита, являются антигенами организма (изоантигены) в том числе антигены А и В системы АВО и резус фактор. Антигены главного комплекса тканевой (гисто) совместимости.
Рис. 3. Рецепторы, встроенные в мембрану эритроцита, являются антигенами организма (изоантигены) в том числе антигены А и В системы АВО и резус фактор. Антигены главного комплекса тканевой (гисто) совместимости. 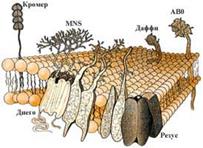
Рис. 2. В-лимфоциты после антигенной стимуляции размножаются и дифференцируются в плазматические клетки (ПК), которые образуют и выделяют антитела.
Помимо антигенов, свойственных всем людям и групповых антигенов, каждый организм обладает уникальным набором антигенов, свойственных только ему самому. Эти антигены кодируются группой генов, находящихся у человека на 6 хромосоме, и называются антигенами главного комплекса тканевой совместимости и обозначаются МНС-антигены (англ. Major histocompatibility complex). МНС-антигены человека впервые были обнаружены на лейкоцитах и поэтому имеют другое название - HLA (Human leucocyte antigens). МНС-антигены относятся к гликопротеинам и содержатся на мембранах клеток организма, определяя его индивидуальные свойства и индуцируют трансплантационные реакции, за что они получили третье название - трансплантационные антигены. Кроме того, МНС-антигены играют обязательную роль в индукции иммунного ответа на любой антиген.
Белки I класса находятся на поверхности практически всех клеток организма. Антигены I класса обеспечивают представление антигенов цитотоксическим CD8+-лимфоцитам, а распознавание этого антигена антигенпредставляющим клеткам другого организма при трансплантации приводит к развитию трансплантационного иммунитета.
МНС-антигены II класса находятся преимущественно на антигенпредставляющих клетках - дендритных, макрофагах, В-лимфоцитах. Основная роль в иммуногенезе антигенов II класса - участие в представлении чужеродных антигенов Т-хелперным лимфоцитам.
Рис. 3. Т-хелперы распознают антиген Т-клеточным рецептором (ТКР) в ассоциации с МНС II класса, Т- киллеры - с МНС I класса. Антигены главного комплекса гистосовместимости I класса представляют антиген (темно-синий круг)Т-киллерам, антигены II класса представляют антиген Т-хелперам.АНТИТЕЛА Антитела (иммуноглобулины) (АТ, Ig) - в большинстве случаев представлены сывороточными гликопротеинами, входящие в состав фракции гамма-глобулинов. АТ образуют один из основных классов белков крови, состояния 20% массы белка плазмы. Молекула АТ состоит из 2 идентичных тяжелых (Н-цепи) и 2 идентичных легких (L-цепи) аминокислотных цепей, соединенных дисульфидными -S-S- связями (рис.3). В цепях различают вариабельную область (V-область) в N-концевой части и постоянную, или константную, область (С-область). V-область у разных АТ варьирует. V-области L- и Н-цепей образуют Аг-связывающий центр(активный центр АТ, паратоп), или Fab-фрагмент. Константная область молекулы имеет Fc-фрагмент.Аг-связывающий центр, образованный вариабельными областями L- и Н-цепей; именно с ним взаимодействует Аг-детерминанта (эпитоп) антигена. Аг-связывающий центр комплементарен эпитопу Аг по приципу «ключ-замок». Молекула Ig как минимум двухвалентна; такие антитела известны как полные АТ,а мономеры с меньшей валентностью - как неполные АТ. Fc-фрагмент определяет специфичность связывания молекулы Ig с клетками-эффекторами (например, макрофагами, полиморфноядерными лейкоцитами, тучными клетками), несущими на своей поверхности рецепторы Fc-фрагмента. 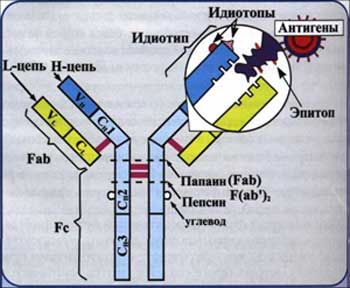
Рис. 6. Структура иммуноглобулина. Классы иммуноглобулинов и свойства антител
В зависимости от структуры Н-цепей выделяют 5 разных классов (изотипов) АТ: IgA, IgD, IgE, IgG и IgM.
1. IgM -пентамер из 5 субъединиц, соединенных дисульфидными связями, имеет 10 Аг-связывающих участков. IgM - наиболее ранний класс АТ, обнаруживаемый при первичном попадании Аг в организм, т.е. наличие IgM к Аг конкретного возбудителя указывает на наличие острого инфекционного процесса. Молекулы IgM опсонизируют, агглютинируют, преципитируют и лизируют содержащие Аг структуры, а также легко активируют систему комплемента.
2. IgG - Основной класс АТ (до 75% всех Ig), защищающих организм от бактерий, вирусов и токсинов. После первичного контакта с Аг синтез IgM обычно сменяется образованием более дифференцированных IgG. Максимальные титры IgG при первичном ответе наблюдаются на 6-8 сутки. Обнаружение высоких титров IgG к Аг конкретного возбудителя указывает на то, что организм находится на стадии реконвалесценции или конкретное заболевание перенесено недавно.
IgG непосредственно участвуют в реакциях иммунного цитолиза, реакциях нейтрализации, а также усиливают фагоцитоз. Только IgG беременной форсируют плацентарный барьер, проходят черезбазальную мембранутрофобласта в соединительную ткань плода и попадает в капилляры плода. Транспорт IgG через плаценту обеспечивает формирование пассивного иммунитета у плода.
3. IgA (в сывороточном пуле Ig составляют 15-20%) секретируются на поверхность эпителиев, присутствуют в слюне, слезах, молоке, выделяются на поверхность слизистых оболочек, где взаимодействуют с Аг, усиливая защитные свойства слизистых оболочек пищеварительного тракта, дыхательных, половых и мочевыделительных путей. В сыворотке IgA циркулируют в виде мономеров, а в секретируемых SIgA преобладают четырехвалентные димеры, содержащие одну J-цепь и дополнительную полипептидную цепь (синтезируемых эпителиальными клетками секреторный компонент).
4. IgE специфически взаимодействуют с тучными клетками и базофильными лейкоцитами; эти клетки содержат многочисленные гранулы с биологически активными аминами. Защитные потенции IgE направлены преимущественно против гельминтов (нематод).
5. IgD. Биологическая роль этого Ig не установлена; IgD обнаруживают на поверхности развивающихся В-лимфоцитов; в сыворотке здоровых лиц он присутствует в крайне низкой концентрации. 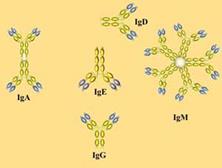
Рис. 7. Антитела разных классов отличаются биологическими свойствами.
Защитные механизмы антител (функции).
АТ помогают предотвратить инфицирование и/или элиминировать возбудитель, активируя при этом несколько механизмов.
