Классификация аминокислот белков
|
| |||||
 |
pI – изоэлектрическая точка * - незаменимые аминокислоты
Таблица 18
Основные виды взаимодействий, фиксирующих вторичную
и третичную структуру пептидов и белков
| Ковалентные | Нековалентные | |
| Дисульфидные связи | Ионные связи | Водородные связи |
| Между простран-ственно сближенными цистеиновыми остатками | Образуются за счет притяжения между разноименно заря-женными группами 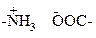 |   |
| Стабилизируют третичную структуру | Стабилизируют вторичную и третичную структуру |
Указания по выполнению самостоятельной работы № 9
Раздел для самостоятельного изучения: Установление первичной структуры пептидов. Определение аминокислотной последовательности.
Актуальность изучаемого раздела: Полиамидные цепи полипептидов построены единообразно. Специфичность пептидов и белков определяется не только аминокислотным составом, но и аминокислотной последовательностью.
План изучения
1. Сущность метода деградации пептидов по Эдману (фенилизотиоцианатный метод).
2. Идентификация полученных ФТГ-производных.
3. Понятие о методе Сенгера (динитрофенилирование).
Вопросы для самоконтроля
1. Напишите схему реакции фенилизотиоцианата с глутаминовой кислотой.
2. Напишите строение ФТГ-производных, образующихся при расщеплении по Эдману трипептида Цис-Асп-Вал.
3. Напишите формулу трипептида и назовите его, если при его деградации по Эдману получены ФТГ-производные в последовательности:
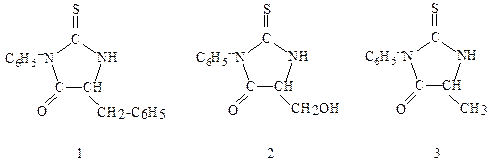 |
Форма контроля. Проверка упражнений, тестовый контроль на занятии.
Приложение
Вопросы для тестового контроля
УКАЖИТЕ СООТВЕТСТВИЯ!
1.
1. гетероциклическая аминокислота а) фенилаланин г) валин
2. алифатическая аминокислота б) тирозин д) аланин
в) триптофан
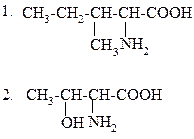 2.
2.
а) валин
б) лейцин
в) изолейцин
г) серин
д) треонин
3.
1. триптофан а) алифатическая аминокислота
2. глютаминовая кислота б) ароматическая аминокислота
3. фенилаланин в) гетероциклическая аминокислота
4.
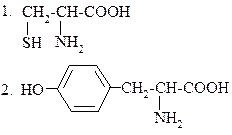 а) тирозин
а) тирозин
б) триптофан
в) серин
г) цистеин
д) цистин
5.
1. нейтральные аминокислоты а) валин г) глутаминовая кислота
2. кислые аминокислоты б) аланин д) лизин
в) аспарагиновая кислота
6.
1. аспарагиновая кислота а) алифатическая аминокислота
2. гистидин б) ароматическая аминокислота
3. фенилаланин в) гетероциклическая аминокислота
7.
1. серин а) кислая аминокислота
2. лизин б) основная аминокислота
в) нейтральная аминокислота
8.
1. триптофан а) алифатическая аминокислота
2. тирозин б) ароматическая аминокислота
3. серин в) гетероциклическая аминокислота
9. 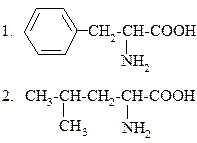
а) фенилаланин
б) тирозин
в) триптофан
г) валин
д) лейцин
е) изолейцин
10.
1. аргинин а) кислая аминокислота
2. цистин б) основная аминокислота
в) нейтральная аминокислота
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
11.
ГИДРОКСИЛСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ:
1. аргинин 3. серин 5. треонин
2. метионин 4. цистеин
12.
СЕРУСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ:
3. метионин 3. серин 5. треонин
4. аргинин 4. цистеин
13. ПРОЕКЦИОННАЯ ФОРМУЛА L-АЛАНИНА:
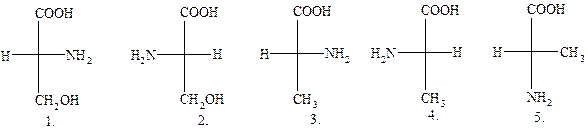 |
14. ПРОЕКЦИОННАЯ ФОРМУЛА ЭНАНТИОМЕРА D-ВАЛИНА:
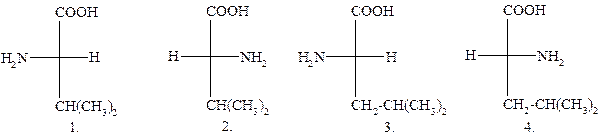 |
15. ПРОЕКЦИОННАЯ ФОРМУЛА L-СЕРИНА:
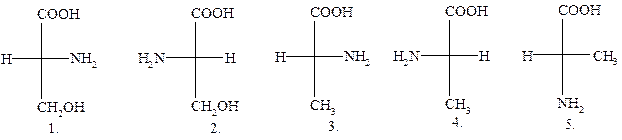
16.
ПРОЕКЦИОННАЯ ФОРМУЛА ЭНАНТИОМЕРА L-ВАЛИНА:
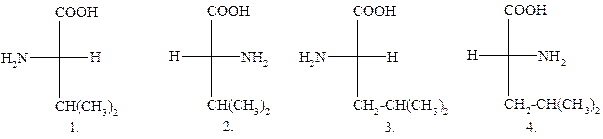 |
17.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА ЛИЗИНА НАХОДИТСЯ:
1. в нейтральной области pH
2. в кислой области pH
3. в щелочной области pH
18.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА ИЗОЛЕЙЦИНА НАХОДИТСЯ:
1. в нейтральной области pH
2. в кислой области pH
3. в щелочной области pH
19.
В СИЛЬНОКИСЛОЙ СРЕДЕ ВАЛИН СУЩЕСТВУЕТ В ВИДЕ:
1. биполярного иона 2. катиона 3. аниона
20.
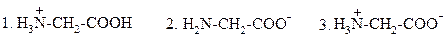 ПРИ pH=3 ГЛИЦИН СУЩЕСТВУЕТ В ВИДЕ:
ПРИ pH=3 ГЛИЦИН СУЩЕСТВУЕТ В ВИДЕ:
21.
ИЗОЭЛЕКТРИЧЕСКАЯ ТОЧКА АСПАРАГИНОВОЙ КИСЛОТЫ НАХОДИТСЯ:
1. в нейтральной области pH
2. в кислой области pH
3. в щелочной области pH
22.
В СИЛЬНОКИСЛОЙ СРЕДЕ АЛАНИН СУЩЕСТВУЕТ В ВИДЕ:
1. биполярного иона 2. катиона 3. аниона
23. ПРИ pH=12 ГЛИЦИН СУЩЕСТВУЕТ В ВИДЕ:
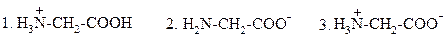 |
24. ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО (БУКВУ)!
МОЛЕКУЛЫ ПЕПТИДОВ ПОСТРОЕНЫ ИЗ ОСТАТКОВ ______-СТЕРЕОИЗОМЕРОВ α-АМИНОКИСЛОТ.
УКАЖИТЕ СООТВЕТСТВИЯ!
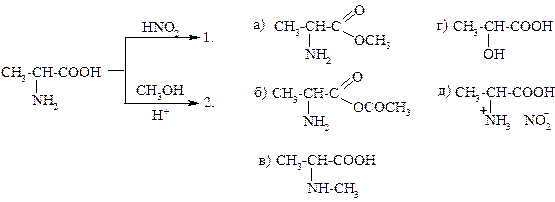 25.
25.
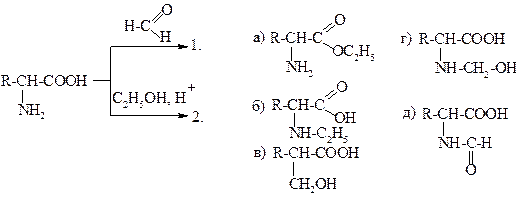 26.
26.
27.
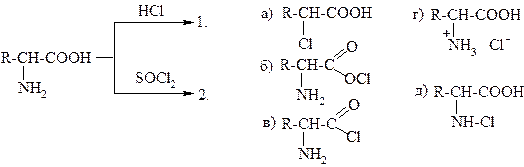 |
28.
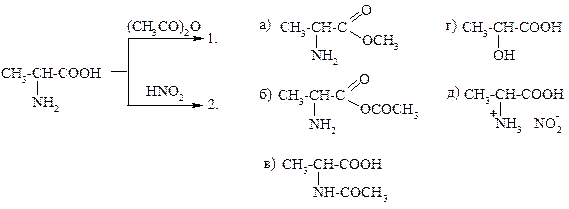
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
29.
КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА АРОМАТИЧЕСКИЕ АМИНОКИСЛОТЫ
ЯВЛЯЕТСЯ РЕАКЦИЯ С:
1. (CH3CO)2Pb 4. конц. HNO3
2. конц. H2SO4 5. разбавленной HNO3
3. (CH3COO)2Pb 6. HNO2
30.
ФЕНИЛАЛАНИН И ТИРОЗИН МОЖНО РАЗЛИЧИТЬ ПО РЕАКЦИИ С:
1. конц. HNO3 3. FeCl3 5. HCl
2. конц. H2SO4 4. HNO2
31.
ПРИ ДЕКАРБОКСИЛИРОВАНИИ ГИСТИДИНА in vitro ОБРАЗУЕТСЯ:
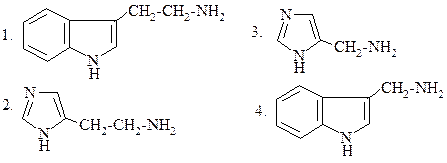 |
32.
ПРИ ДЕЗАМИНИРОВАНИИ ВАЛИНА in vitro ОБРАЗУЮТСЯ:
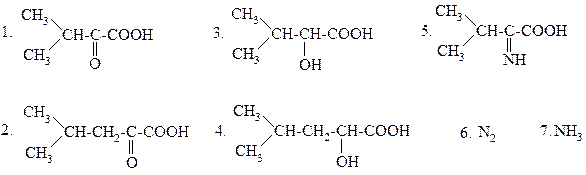 |
33.
КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА СЕРУСОДЕРЖАЩИЕ АМИНОКИСЛОТЫ
ЯВЛЯЕТСЯ РЕАКЦИЯ С:
4. (CH3CO)2Pb 4. конц. HNO3
5. конц. H2SO4 5. разбавленной HNO3
6. (CH3COO)2Pb 6. HNO2
34.
ПРИ ДЕКАРБОКСИЛИРОВАНИИ ТРИПТОФАНА in vitro ОБРАЗУЕТСЯ:
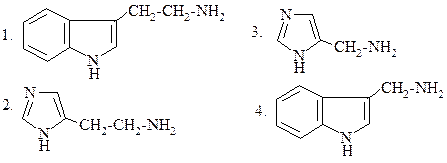 |
35.
ФОРМУЛА ПРОДУКТА ДЕКАРБОКСИЛИРОВАНИЯ ГИСТИДИНА in vivo:
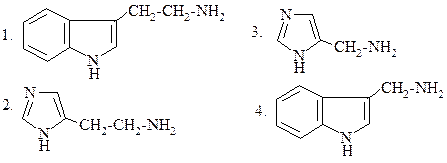 |
36.
ПРИ ОКИСЛИТЕЛЬНОМ ДЕЗАМИНИРОВАНИИ АЛАНИНА in vivo ОБРАЗУЕТСЯ:
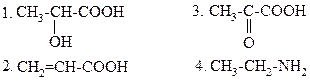 |
37.
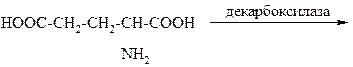 |
В РЕЗУЛЬТАТЕ РЕАКЦИИ ОБРАЗУЕТСЯ
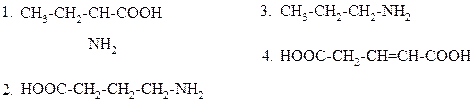 |
38.
ПРИ ОКИСЛИТЕЛЬНОМ ДЕЗАМИНИРОВАНИИ АСПАРАГИНОВОЙ КИСЛОТЫ in vivo ОБРАЗУЕТСЯ:
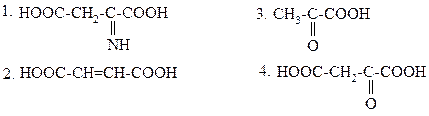 |
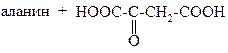 39.
39.
В РЕЗУЛЬТАТЕ ПЕРЕАМИНИРОВАНИЯ
ОБРАЗУЮТСЯ:
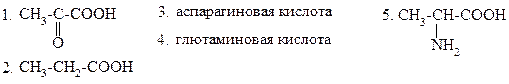 |
40.
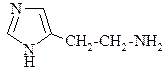 ДАННОЕ СОЕДИНЕНИЕ ЯВЛЯЕТСЯ ПРОДУКТОМ:
ДАННОЕ СОЕДИНЕНИЕ ЯВЛЯЕТСЯ ПРОДУКТОМ:
1. декарбоксилирования триптофана
2. декарбоксилирования гистидина
3. неокислительного дезаминирования гистидина
4. дезаминирования триптофана in vitro
ВПИШИТЕ НЕДОСТАЮЩЕЕ СЛОВО (СЛОВА)!
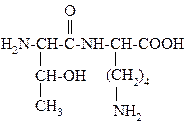 41.
41.
НАЗВАНИЕ ДИПЕПТИДА
______.
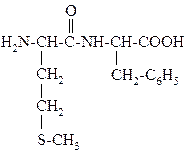 42.
42.
НАЗВАНИЕ ДИПЕПТИДА
______.
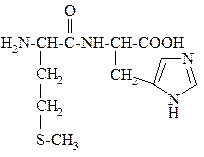 |
43.
НАЗВАНИЕ ДИПЕПТИДА
______.
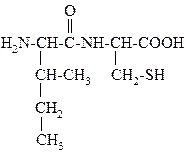 44.
44.
НАЗВАНИЕ ДИПЕПТИДА
______.
45.
РЕАКЦИЯ С КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТОЙ ЯВЛЯЕТСЯ
КАЧЕСТВЕННОЙ НА _________________ АМИНОКИСЛОТЫ. ОНА НАЗЫВАЕТСЯ ______________________________ РЕАКЦИЕЙ.
46.
ПРИ НАГРЕВАНИИ ФЕНИЛАЛАНИНА С КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТОЙ ПОЯВЛЯЕТСЯ ___________________ ОКРАШИВАНИЕ, КОТОРОЕ В ЩЕЛОЧНОЙ СРЕДЕ ИЗМЕНЯЕТСЯ НА _____________________.
УКАЖИТЕ ПРАВИЛЬНЫЙ ОТВЕТ (ОТВЕТЫ)!
47.
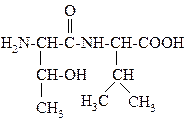
НАЗВАНИЕ ДИПЕПТИДА:
1. серилвалин
2. валилсерин
3. треонилсерин
4. серинвалин
5. треонинсерин
6. треонилвалин
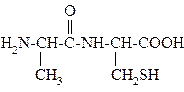 48.
48.
НАЗВАНИЕ ДИПЕПТИДА:
1. серилцистеин
2. серилметионин
3. аланинцистеин
4. аланилцистеин
5. цистеилсерин
6. цистеинсерин
49.
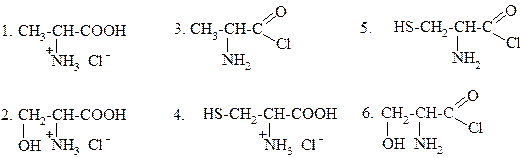 |
ПРИ КИСЛОТНОМ (В ПРИСУТСТВИИ HCl) ГИДРОЛИЗЕ АЛА-ЦИС
ОБРАЗУЮТСЯ:
50.
ПРИ ЩЕЛОЧНОМ ГИДРОЛИЗЕ (NaOH) ДИПЕПТИДА ГЛИ-АЛА ОБРАЗУЮТСЯ:
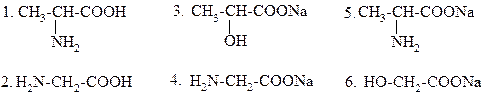 |
51.
ПРИ ФЕРМЕНТАТИВНОМ ГИДРОЛИЗЕ ВАЛ-ТРЕ ОБРАЗУЮТСЯ:
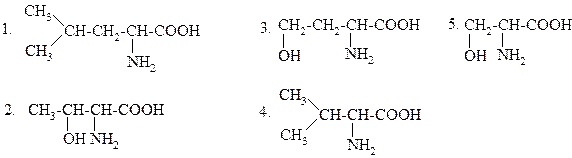 |
52.
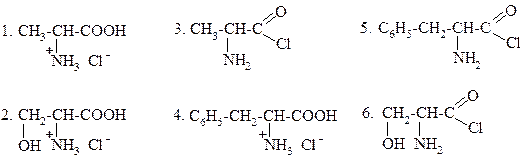 |
ПРИ КИСЛОТНОМ (В ПРИСУТСТВИИ HCl) ГИДРОЛИЗЕ АЛА-ФЕН
ОБРАЗУЮТСЯ:
53.
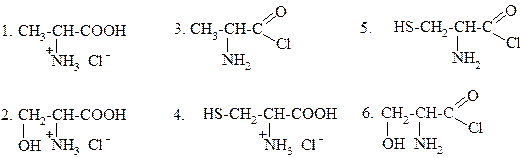 |
ПРИ КИСЛОТНОМ (В ПРИСУТСТВИИ HCl) ГИДРОЛИЗЕ АЛА-ЦИС
ОБРАЗУЮТСЯ:
54.
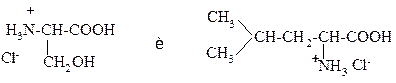 ДАННЫЕ СОЕДИНЕНИЯ МОГУТ БЫТЬ ПРОДУКТАМИ:
ДАННЫЕ СОЕДИНЕНИЯ МОГУТ БЫТЬ ПРОДУКТАМИ:
1. кислотного гидролиза Тре-Вал
2. ферментативного гидролиза Вал-Тре
3. кислотного гидролиза Сер-Лей
4. кислотного гидролиза Сер-Иле
5. кислотного гидролиза Лей-Сер
55.
ЭЛЕКТРОННОЕ И ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПЕПТИДНОЙ СВЯЗИ
ВЫРАЖЕНО ФОРМУЛОЙ:
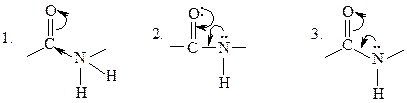 |
56.
РЕАГЕНТАМИ ДЛЯ БИУРЕТОВОЙ РЕАКЦИИ ЯВЛЯЮТСЯ:
1. конц. HNO3
2. CuSO4 + NaOH
3. (CH3COO)2Pb
4. CuSO4 + HCl
5. (CH3CO)2O
57.
РЕАКЦИЯ БЕЛКОВ С ГИДРОКСИДОМ МЕДИ (II) ЯВЛЯЕТСЯ КАЧЕСТВЕННОЙ.
1. на серусодержащие аминокислоты белков
2. на ароматические аминокислоты белков
3. на пептидные связи
4. на многоатомные спирты
58. ВПИШИТЕ НЕДОСТАЮЩИЕ СЛОВА (БУКВЫ, ЦИФРЫ)!
ПЕПТИДНАЯ СВЯЗЬ ПРЕДСТАВЛЯЕТ СОБОЙ ____ , _____-СОПРЯЖЁННУЮ СИСТЕМУ, В КОТОРОЙ ДЕЛОКАЛИЗОВАНО ___________ ЭЛЕКТРОНА.
Занятие № 16
