Получение этилхлорида из этилового спирта
В пробирку насыпьте 2 лопаточки хлорида натрия, прилейте 5-6 капель этилового спирта. Затем добавьте 3-4 капли концентрированной серной кислоты и нагревайте на слабом пламени спиртовки, не допуская обильного выделения хлороводорода. Время от времени подносите отверстие пробирки к пламени горелки (этилхлорид образуется не сразу). Выделяющийся этилхлорид загорается, образуя колечко зеленого цвета.
Запишите схемы протекающих реакций. Укажите механизм реакции образования этилхлорида. Укажите роль серной кислоты в данной реакции.
Дегидратация этилового спирта
В пробирку № 1 поместите 8 капель концентрированной серной кислоты, 4 капли этилового спирта и несколько крупинок оксида алюминия. Закройте пробирку газоотводной трубкой. В пробирку № 2 поместите 10 капель бромной воды, в пробирку № 3 – 2 капли 2% раствора перманганата калия и 10 капель воды. Нагревайте пробирку № 1 в пламени спиртовки, опустив конец газоотводной трубки в пробирку № 2. Что вы наблюдаете? Затем, не прекращая нагревания, опустите конец газоотводной трубки в пробирку № 3. Какие изменения происходят в пробирке? Удалите пробирку № 3 и поднесите конец газоотводной трубки к пламени горелки. Выделяющийся газ горит светящимся пламенем.
Запишите схемы реакций, протекающих в пробирках № 1, 2 и 3. Укажите их механизмы.
Окисление этилового спирта бихроматом калия в кислой среде
В пробирку поместите 2 капли этилового спирта, добавьте 1 каплю 10% раствора серной кислоты и 2 капли 10% раствора бихромата калия. Полученный раствор нагрейте в пламени спиртовки. Зафиксируйте изменение окраски и появление характерного запаха.
Запишите схему протекающей реакции. Будет ли характерна подобная реакция для пропанола-2?
Реакция фенола с хлоридом железа (III)
Крупинку фенола растворите в 1 мл воды и добавьте 2 капли раствора хлорида железа (III). Опишите наблюдаемый эффект реакции. Какой фрагмент молекулы фенола является ответственным за эту реакцию?
Блок информации
Граф 9
Реакционные центры в молекулах спиртов
 |
Граф 10
Свойства спиртов 

|
|
|




 RCOOH,H+
RCOOH,H+
|

 HCl R-OH,H+
HCl R-OH,H+
 | ||||||||
 | ||||||||
 |  | |||||||
 | ||||||||

конц. H2SO4, to K2Cr2O7, H+
|
|

Na

Граф 11
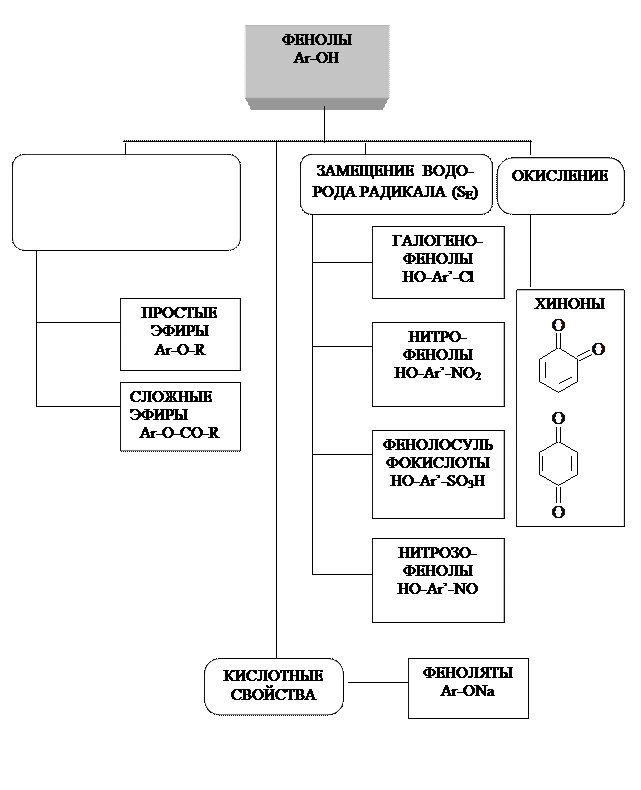
Свойства фенолов
РЕАКЦИИ НУКЛЕОФИЛЬ-
НОГО ЗАМЕЩЕНИЯ
Cl2 K2Cr2O7
R-Cl
HNO3
R-CO-Cl
(R-CO)2O
H2SO4
HNO2
NaOH
