Исследование эффективности и ингаляционной токсичности средства для обеззараживания воздуха в зоне дыхания человека для неспецифической профилактики воздушно-капельных инфекций
Исследование эффективности и ингаляционной токсичности средства для обеззараживания воздуха в зоне дыхания человека для неспецифической профилактики воздушно-капельных инфекций
А.Ю. Скопин1,2, Л.С. Федорова1,2, Д.Л. Виноградов2, Е.В. Карадулева3, Р.Г. Гончаров3, А.В. Кочкина3, А.Е. Гордеева3, В.А. ЕВДОКИМОВ3, Р.В. Разживин3, В.И. Новоселов3
1 ФБУН «НИИ дезинфектологии» Роспотребнадзора, Москва, Россия;
2 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия
3 ФГБУН «Институт биофизики клетки» РАН, г. Пущино, Россия;
Цель исследования – определение эффективности и ингаляционной токсичности генератора диоксида хлора (ДХ) используемого в качестве персонального обеззараживателя воздуха для инактивации возбудителей воздушно-капельных инфекций.
Исследования, проведенные в ФГБУ «НИИ гриппа» Минздрава России (Санкт-Петербург), показали высокую вирулицидную активность генератора ДХ в отношении вируса гриппа: в низких, малотоксичных концентрациях ДХ титр вируса в пробах воздуха через 1–3 мин снижался на 90%, через 3–5 мин – на 97%, через 10–12 мин – на 99%. Средство эффективно в течение не менее 30 суток. Ингаляционную токсичность ДХ изучали в экспериментах с использоваем крыс, которых определенное время выдерживали в атмосфере ДХ. Затем состояние структуры трахеи и легких определяли гистологическими методами, степень окислительного стресса – по содержанию малонового альдегида в тканях и динамике экспрессии генов всех классов ферментовантиоксидантов (всего 15 разных ферментов). Установлена полная сохранность структуры эпителия трахеи и легких, при этом не произошло увеличения гибели клеток по апопотическому пути в обеих тканях и увеличения перекисного окисления липидов в ткани легкого. Повышенная защита клеток эпителиев трахеи и легкого от действия высокотоксичных активных форм кислорода, образующихся в ткани, связана с активацией экспрессии генов ферментов-антиоксидантов в эпителии, которая наблюдается в первые часы после действия ДХ. Результаты проведенных исследований позволяют рекомендовать обеззраживатель воздуха для профилактики воздушно-капельных инфекций.
Ключевые слова: диоксид хлора, воздушно-капельные инфекции, верхние дыхательные пути, профилактика.
Для цитирования: Скопин А.Ю., Федорова Л.С., Виноградов Д.Л., Карадулева Е.В., Гончаров Р.Г., Кочкина А.В, Гордеева А.Е., Евдокимов В.А., Разживин Р.В., Новоселов В.И. Исследование эффективности и ингаляционной токсичности средства для обеззараживания воздуха в зоне дыхания человека для неспецифической профилактики воздушно-капельных инфекций. Эпидемиол. инфекц. болезни. Актуал. вопр. 2017(4):71–77
Токсикологическое воздействие ДХ на организм
Газообразный ДХ обладает мощным антимикробным действием в очень низкой концентрации. Так, было продемонстрировано, что антимикробное действие газообразного ДХ проявляется при концентрации от 0,01 до 0,03 мг/м³ [4–5]. При этом остается неизвестным, является ли безопасным хроническое воздействие газообразного ДХ на организм в концентрациях, эффективных для борьбы с микроорганизмами. В этой связи было выполнено исследование ингаляционной токсичности ДХ в низкой концентрации при долговременном воздействии на экспериментальных животных. При ингаляции ДХ в первую очередь воздействию подвергаются верхние дыхательные пути, соответственно было изучено воздействие ДХ на эпителий трахеи и легких. Наконец, воздействие ряда химически активных веществ на органы дыхания практически всегда сопровождается окислительным стрессом в этих органах [6, 7]. Для нейтрализации негативных последствий в органе активируются различные звенья антиоксидантной системы [8], поэтому исследуя динамику экспрессии генов ферментов-антиоксидантов органа, мы можем характеризовать как сам окислительный стресс, так и основные звенья, ответственные за его нейтрализацию.
Материалы и методы
В экспериментах были использованы крысы линии «Вистар» мужского пола весом 200-220 г. В качестве источника ДХ был применен серийный обеззараживатель воздуха (генератор ДХ)
Животных помещали в клетки, расположенные в камере размером 75 х 75 х 80 см при температуре 24°C и относительной влажности воздуха 7 %, с 12-часовым циклом чередования светлого и темного времени суток. Генератор ДХ был расположен на расстоянии 25 см от верха клеток. Животных выдерживали в атмосфере ДХ в течение определенного времени. В случае суточных экспериментов через 5 ч после каждого воздействия генератор ДХ из камеры удаляли. При исследовании хронического воздействия ДХ генератор находился в камере в течение всех 30 дней.
Все эксперименты над животными проводили в строгом соответствии с требованиями Руководства по обращению с лабораторными животными РФ и Руководством по работе с животными сотрудниками ИБК РАН (утверждено приказом директора ИБК РАН № 57 от 30.12. 2011).
Перед забоем животных наркотизировали путем внутрибрюшинного введения раствора диэтилбарбитуровой кислоты из расчета 10 мг на 100 г массы животного. Выделенную ткань для экспериментов немедленно помещали в жидкий азот. Для одновременного гистологического анализа и анализа экспрессии генов на одном животном в случае трахеи для гистологии брали верхнюю половину трахеи, для анализа уровня экспрессии генов – нижнюю половину трахеи.
Гистологические исследования проводили на парафиновых срезах по стандартной методике. Выделенные образцы ткани закрепляли в фиксаторе Mirsky’sFixative («NationalDiagnostics», США) с последующей проводкой в соответствующих растворах и заключении в парафин. Срезы толщиной 2–5 мкм получали на криотоме HM 325 Microm («ThermoScientific», Германия).и окрашивали гематоксилином-эозином (Hematoxylin-EozinaccordingtoEhrlich, «Fluka», США). Для выявления муцина и клеток, его секретирующих, срезы окрашивали альциановым синим. Дальнейший анализ проводили на световом микроскопе Leica DM 6000 B («LeicaMicrosystems», Германия) с помощью камеры Leica DFC 420 C.
Для определения малоновогодиальдегида (МДА) Предварительно замороженную в кельвинаторе до -80°С ткань (легкие) размалывали до пылеобразного состояния (с использованием жидкого азота). К 100 мг образца добавляли 3 мл 1% H3PO4, 1 мл 0,8% водного раствора тиобарбитуровой кислоты (ТБК), нагревали смесь на кипящей водяной бане в течение 45 мин. После охлаждения добавляли 4 мл н-бутанола и отделяли слой бутанола путем центрифугирования. Оптическую плотность определяли при длине волны 535 нм по сравнению с контрольными образцами без добавления ткани.
В трахее и легких анализировали экспрессию генов для 15 основных ферментов-антиоксидантов: глутатионпероксидаз 1–8, пероксиредоксинов 1–6, супероксиддисмутаз 1–3 и каталазы. Также исследовали уровень экспрессии генов для маркера апоптоза клеток (сaspase-3) и клеточного маркера пролиферации клеток (Ki-67). Использовали ген-специфическиепраймеры, синтезированные согласно их последовательностям в GenBank. Уровень экспрессии определяли методом ОТ ПЦР (обратная транскрипция + ПЦР) в реальном времени. Нормирование проводили относительно гена фактора элонгации EFIα или гена β-актина – Аctb.
Статистический анализ выполняли с использованием программы SigmaPlot 11.0 Sortware. Результаты выражали как среднее значение (М) ± стандартная ошибка (m). Показатели считали статистически достоверными при p Результаты
Таблица 1. Изменение уровня экспрессии генов ферментов-антиоксидантов в трахее после воздействия ДХ
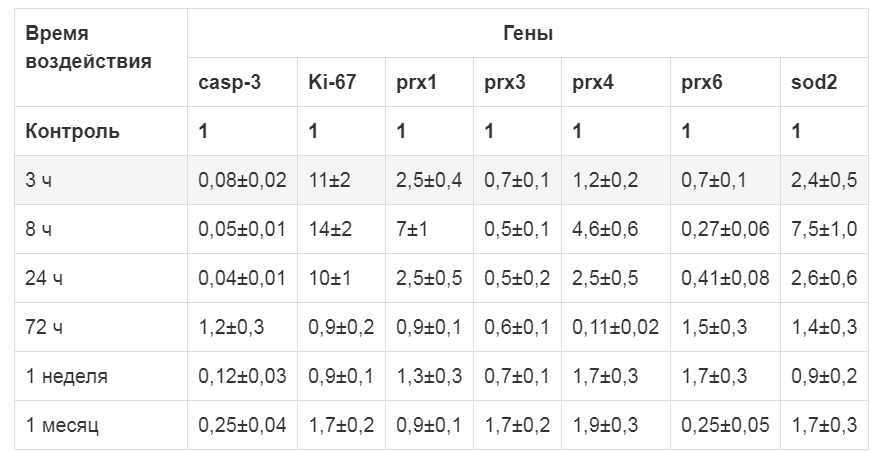
Уровень экспрессии caspase-3 не увеличивался за время действия ДХ, следовательно в эпителии трахеи не происходило гибели клеток путем апоптоза, что согласуется с гистологическими данными. Значительное (более чем в 10 раз) увеличение экспрессии Ki-67 свидетельствует об активации внутриклеточных процессов.
В первые часы после действия ДХ резко увеличивается экспрессия некоторых ферментов-антиоксидантов, что свидетельствует о реакции клеток трахеи на развитие окислительного стресса. Максимальный уровнь экспрессии зафиксирован через 8 ч после действия ДХ. При хроническом воздействии ДХ наблюдается полная адаптация всех систем.
Таблица 2. Содержание МДА в ткани легкого после действия ДХ (в нмоль/г ткани)
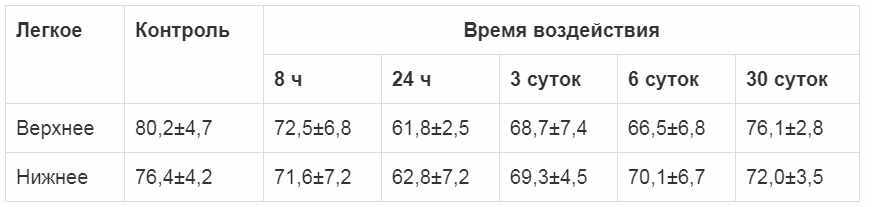
Таблица 3. Изменение уровня экспрессии генов ферментов-антиоксидантов в ткани легких после воздействия ДХ
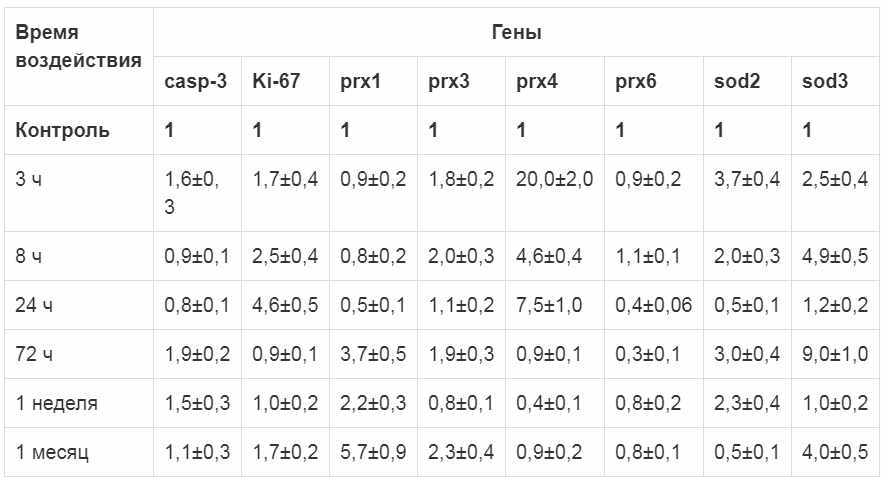
Динамика экспрессии генов значимых ферментовантиоксидантов в ткани легкого несколько отличается от таковой для трахеи как по времени, так и по набору ферментов. Это, по-видимому, связано с различным клеточным составом эпителия трахеи и легкого. Активация экспрессии генов-антиоксидантов по времени в ткани легкого и трахее имеет 2 максимума как по времени, так и по типу ферментаантиоксиданта: первый – через 3 ч, второй – через 3 суток.
Обсуждение
Полученные результаты свидетельствует о том, что в эпителии трахеи и легких существенно повышается уровень АФК. Основную роль в нейтрализации избыточного количества АФК играют пероксиредоксины и супероксиддисмутазы, что согласуется с литературными данными о вкладе этих ферментов в нейтрализацию окислительного стресса в верхних дыхательных путях при острых патологиях [6–8]. Для трахеи максимум активации генов пероксиредоксинов и супероксиддисмутаз происходит через 8 ч после действия ДХ. В это же время достигает максимума активация секреции бокаловидными клетками, то есть в трахее существенно повышается защитный потенциал. Тот факт, что одновременно не разрушаются ткани эпителия, свидетельствует об эффективности антиоксидантной защиты, поскольку именно эти ферменты обеспечивают дополнительную защиту клеток эпителия трахеи от избыточного количества АФК.
То же происходит в ткани легкого при воздействии ДХ. Отсутствие роста перекисного окисления липидов и разрушения структуры ткани свидетельствует об эффективности активации антиоксидантной системы. Поскольку активация экспрессии генов ферментов-антиоксидантов в легких имеет 2 максимума (через 3 ч и через 3 суток), можно сделать вывод, что антиоксидантная защита ткани легкого состоит из 2 этапов: первого, когда антиоксидантная система активируется сразу после воздействия ДХ, и второго, когда необходимо нейтрализовать возможные негативные процессы, связанные с окислительным стрессом.
Суммируя вышесказанное, можно сделать заключение, что во время действия паров ДХ в малых концентрациях антиоксидантные системы верхних дыхательных путей заметно активируются и полностью предотвращают возможные нарушения в функционировании клеток трахеи и бронхов. Это согласуется с данными других исследователей, которые не обнаружили значимых нарушений в организме животных при использовании генераторов ДХ, схожих посвоим характеристикам с генератором [9, 10]. Принимая во внимание значительное сходство антиоксидантных систем верхних дыхательных путей крысы и человека [11], полученные результаты могут служить доказательством того, что генератор ДХ безопасен и для человека.
Литература
- Карпова Л.С., Пелих М.Ю., Еропкин М.Ю., Поповцева Н.М., Столярова Т.П., Столяров К.А., Соминина А.А., Киселев О.И. Эпидемиологическая ситуация по гриппу в мире и России в сезон 2014–2015 годов. Эпидемиология и вакцинопрофилактика 2015; (4): 8–17.
- Бурцева Е.И., Федякина И.Т., Кириллова Е.С., Трушакова С.В., Феодоритова Е.Л., Беляев А. Л., Краснослободцев К. Г., Мукашева Е.А., Гарин Е.О., Оскерко Т.А., Аристова В.А., Львов Д.К. Заболеваемость гриппом в январе–марте 2016 г. в РФ. Эпидемический и пандемический потенциал вируса гриппа А(Н1N1)PDM09. Пульмонология 2016; (4): 436–43.
- Зарубаев В.В., Штро А.А., Светницкий Е.Н. Изучение эффективности обеззараживателя воздуха нового типа – генератора диоксида хлора на примере вируса гриппа A (H1N1)pdm09 в составе аэрозоля. Лечащий врач 2016; (11): 1–3. medi.ru/info/12755
- Kuroyama I., Osato S., Nakajima S., Kumota R., Ogawa T. Environmental monitoring and bactericidal efficacy of chlorine dioxide gas in a dental office. Biocontrol. Sci. 2010; 15: 103–9.
- Rastogi V.K., Ryan S.P., Wallace L., Smith L.S., Shah S.S., Martin G.B. Systematic valuation of the efficacy of chlorine dioxide in decontamination of building interior surfaces contaminated with anthrax spores. Appl. EnvironMicrobiol. 2010; (76): 3345–51.
- Cиpота Т.В., Cафpонова В.Г., Амелина А.Г., Мальцева В.Н., Авxачева Н.В., Cофин А.Д., Янин В.А., Мубаpакшина Э.К., Pоманова Л.К., Новоcелов В.И. Дейcтвиеотpицательныx ионов воздуxа на оpганыдыxания и кpовь. Биофизика 2008; (53): 886–93.
- Новоселов В.И. Роль пероксиредоксинов при окислительном стрессе в органах дыхания. Пульмонология 2012; (10): 80–8.
- Новоселов В.И., Мубаракшина Э.К., Янин В.А., Амелина С.Е., Фесенко Е.Е. Роль ангиоксидантпых систем в регенерации эпителия трахеи после термического ожога верхних дыхательных путей. Пульмонология 2008; (6): 80–3.
- Paulet G., Desbrousses S. On the toxicology of chlorine dioxide. Arch. Mal. Prof. 1972; (33): 59–61.
- Paulet G., Desbrousses S. Actions of discontinuous exposure to chlorine dioxide (ClO2) on the rat. Arch. Mal. Prof. 1974; (35): 797–804.
- Chuchalin A.G., Novoselov V.I., Shifrina O.N., Soodaeva S.K., Yanin V.A., Barishnikova L.M. Peroxiredoxin VI in human respiratory system. Respir. Med. 2003; (97): 147–51. Поступила 26.06.2017
References
- Karpova L.S., PelikhM.Yu., EropkinM.Yu., Popovtseva N.M., Stolyarova T.P., Stolyarov K.A., Sominina A.A., Kiselev O.I. [The Epidemiological Situation of Influenza in the World and Russia in the Season 2014–2015]. Epidemiologiya i Vaktsinoprofilaktika 2015; (4): 8–17. (InRuss.).
- Burtseva E.I., Fedyakina I.T., Kirillova E.S., Trushakova S.V., Feodoritova E.L., Belyaev A.L., Krasnoslobodtsev K.G., Mukasheva E. A., Garina E O., Oskerko T.A., Aristova V.A., L’vov D. K. [FlumorbidityinJanuary–March, 2016, inRussianFederation.Epidemic and pandemic potential of A (H1N1) pdm09 influenza virus]. Pul’monologiya 2016; (4): 436–43. (InRuss.).
- Zarubaev V.V., Shtro A.A., Svetnitcky E.N. [A study of the effectiveness of a new type of air disinfector – a chlorine dioxide generator on the example of the influenza virus A (H1N1) pdm09 as an aerosol]. Lechashchiyvrach 2016; (11): 1–3. (InRuss.). medi.ru/info/12755
- Kuroyama I., Osato S., Nakajima S., Kumota R., Ogawa T. Environmental monitoring and bactericidal efficacy of chlorine dioxide gas in a dental office. Biocontrol. Sci. 2010; 15: 103–9.
- Rastogi V.K., Ryan S.P., Wallace L., Smith L.S., Shah S.S., Martin G.B. Systematic valuation of the efficacy of chlorine dioxide in decontamination of building interior surfaces contaminated with anthrax spores. Appl. EnvironMicrobiol. 2010; (76): 3345–51.
- Sirota T.V., Safronova V.G., Amelina A.G., Mal’tseva V.N., Avkhacheeva N.V., Sofin A.D., Ianin V.A., Mubarakshina E.K., Romanova L.K., Novoselov V.I. [Effect of negative air ions on respiratory organs and blood]. Biofizika 2008; 53(5): 886–93. (InRuss.).
- Novoselov V.I. [The role of peroxiredoxins during oxidative stress in the respiratory organs]. Pulmonologiya 2012; (10): 80–8. (InRuss.).
- Novoselov V.I., Mubarakshina E.K., Yanin V.A., Amelina S.E., Fesenko E.E. [Contribution of antioxidant systems to regeneration of trachea epithelium after the burn of upper airways]. Pulmonologiya 2012; (10): 80–8. (InRuss.).
- Paulet G., Desbrousses S. On the toxicology of chlorine dioxide. Arch. Mal. Prof. 1972; (33): 59–61.
- Paulet G., Desbrousses S. Actions of discontinuous exposure to chlorine dioxide (ClO2) on the rat. Arch. Mal. Prof. 1974; (35): 797–804.
- Chuchalin A.G., Novoselov V.I., Shifrina O.N., Soodaeva S.K., Yanin V.A., Barishnikova L.M. Peroxiredoxin VI in human respiratory system. Respir. Med. 2003; (97): 147–51.
Сведения об авторах:
Скопин Антон Юрьевич – к.м.н., ведущий научный сотрудник ФБУН «НИИ дезинфектологии» Роспотребнадзора; доцент кафедры гигиены ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Федорова Людмила Самуиловна – д.м.н., профессор, заведующий лабораторией проблем дезинфекции ФБУН «НИИ дезинфектологии» Роспотребнадзора; профессор кафедры дезинфектологии ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Виноградов Дмитрий Леонидович – к.м.н., доцент кафедры госпитальной терапии № 2 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
Карадулева Елена Валерьевна – к.б.н., научный сотрудник ФГБУН «Институт биофизики клетки» РАН
Гончаров Руслан Георгиевич – аспирант ФГБУН «Институт биофизики клетки» РАН
Кочкина Ангелина Владимировна – аспирант ФГБУН «Институт биофизики клетки» РАН
Гордеева Алина Евгеньевна – к.б.н., научный сотрудник ФГБУН «Институт биофизики клетки» РАН
Евдокимов Вячеслав Александрович – к.б.н.,, научный сотрудник ФГБУН «Институт биофизики клетки» РАН
Разживин Роман Вячеславович – к.фарм.н., научный консультант ФГБУН «Институт биофизики клетки» РАН
Informationabouttheauthors:
Anton Yu. Scopin, Cand. Med. Sci.; Leading Researcher, Research Institute of Disinfectology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Welfare; Teacher, Department of Hygiene, I.M. Sechenov First Moscow State Medical University, Ministry of Health of Russia (Sechenov University), Moscow, Russia
Prof. Lyudmila S. Fedorova, MD; Head, Laboratory of Disinfection Problems, Research Institute of Disinfectology, Russian Federal Service for Supervision of Consumer Rights Protection and Human Welfare; Professor, Department of Disinfectology, I.M. Sechenov First Moscow State Medical University, Ministry of Health of Russia (Sechenov University), Moscow, Russia
Dmitry L. Vinogradov, Cand. Med. Sci.; Associate Professor, I.M. Sechenov First Moscow State Medical University, Ministry of Health of Russia (Sechenov University), Moscow, Russia
Elena V. Karaduleva, Cand. Biol. Sci.; Researcher, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
Ruslan G. Goncharov, Postgraduate Student, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
Angelina V. Kochkina, Postgraduate Student, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
Alina E. Gordeeva, Cand. Biol. Sci.; Researcher, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
Vyacheslav A. Evdokimov, Cand. Biol. Sci.; Researcher, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
Roman V. Razzhavin, Cand. Pharm. Sci.; Scientific Consultant, Institute of Cell Biophysics, Russian Academy of Sciences, Pushchino, Russia
30 апреля 2017 г.
Исследование эффективности и ингаляционной токсичности средства для обеззараживания воздуха в зоне дыхания человека для неспецифической профилактики воздушно-капельных инфекций
А.Ю. Скопин1,2, Л.С. Федорова1,2, Д.Л. Виноградов2, Е.В. Карадулева3, Р.Г. Гончаров3, А.В. Кочкина3, А.Е. Гордеева3, В.А. ЕВДОКИМОВ3, Р.В. Разживин3, В.И. Новоселов3
1 ФБУН «НИИ дезинфектологии» Роспотребнадзора, Москва, Россия;
2 ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия
3 ФГБУН «Институт биофизики клетки» РАН, г. Пущино, Россия;
Цель исследования – определение эффективности и ингаляционной токсичности генератора диоксида хлора (ДХ) используемого в качестве персонального обеззараживателя воздуха для инактивации возбудителей воздушно-капельных инфекций.
Исследования, проведенные в ФГБУ «НИИ гриппа» Минздрава России (Санкт-Петербург), показали высокую вирулицидную активность генератора ДХ в отношении вируса гриппа: в низких, малотоксичных концентрациях ДХ титр вируса в пробах воздуха через 1–3 мин снижался на 90%, через 3–5 мин – на 97%, через 10–12 мин – на 99%. Средство эффективно в течение не менее 30 суток. Ингаляционную токсичность ДХ изучали в экспериментах с использоваем крыс, которых определенное время выдерживали в атмосфере ДХ. Затем состояние структуры трахеи и легких определяли гистологическими методами, степень окислительного стресса – по содержанию малонового альдегида в тканях и динамике экспрессии генов всех классов ферментовантиоксидантов (всего 15 разных ферментов). Установлена полная сохранность структуры эпителия трахеи и легких, при этом не произошло увеличения гибели клеток по апопотическому пути в обеих тканях и увеличения перекисного окисления липидов в ткани легкого. Повышенная защита клеток эпителиев трахеи и легкого от действия высокотоксичных активных форм кислорода, образующихся в ткани, связана с активацией экспрессии генов ферментов-антиоксидантов в эпителии, которая наблюдается в первые часы после действия ДХ. Результаты проведенных исследований позволяют рекомендовать обеззраживатель воздуха для профилактики воздушно-капельных инфекций.
Ключевые слова: диоксид хлора, воздушно-капельные инфекции, верхние дыхательные пути, профилактика.
Для цитирования: Скопин А.Ю., Федорова Л.С., Виноградов Д.Л., Карадулева Е.В., Гончаров Р.Г., Кочкина А.В, Гордеева А.Е., Евдокимов В.А., Разживин Р.В., Новоселов В.И. Исследование эффективности и ингаляционной токсичности средства для обеззараживания воздуха в зоне дыхания человека для неспецифической профилактики воздушно-капельных инфекций. Эпидемиол. инфекц. болезни. Актуал. вопр. 2017(4):71–77
