Иммунитет. Определение, виды и их сравнительная характеристика.
Иммунная система организма. Структура и основные функции.
Структура иммунной системы. Иммунная система представлена лимфоидной тканью. Это специализированная, анатомически обособленная ткань, разбросанная по всему организму в виде различных лимфоидных образований. К лимфоидной ткани относятся вилочковая, или зобная, железа, костный мозг, селезенка, лимфатические узлы (групповые лимфатические фолликулы, или пейеровы бляшки, миндалины, подмышечные, паховые и другие лимфатические образования, разбросанные по всему организму), а также циркулирующие в крови лимфоциты.
Функции иммунной системы.Иммунная система выполняет функцию специфической зашиты от антигенов, представляющую собой лимфоидную ткань, способную комплексом клеточных и гуморальных реакций, осуществляемых с помощью набора иммунореагентов, нейтрализовать, обезвредить, удалить, разрушить генетически чужеродный антиген, попавший в организм извне или образовавшийся в самом организме.
Специфическая функция иммунной системы в обезвреживании антигенов дополняется комплексом механизмов и реакций неспецифического характера, направленных на обеспечение резистентности организма к воздействию любых чужеродных веществ, в том числе и антигенов.
Центральные и периферические органы иммунной системы. Строение и функции.
Центральные: костный мозг и тимус.
Периферические: селезенка, лимфатические узлы, лимфоидная ткань ассоциированная со слизистыми.
Лимфоидная ткань состоит из ретикулярных клеток, составляющих остов ткани, и лимфоцитов, находящихся между этими клетками. Основными функциональными клетками иммунной системы являются лимфоциты, подразделяющиеся на Т- и В-лимфоциты и их субпопуляции. Общее число лимфоцитов в человеческом организме достигает 1012, а общая масса лимфоидной ткани составляет примерно 1—2 % от массы тела.
В центральных органах иммунной системы постоянно идут процессы пролиферации клеток-предшественниц Т- и В-лимфоцитов, их созревания (дифференцировки), их отбора (селекции), сопровождающиеся их частичной гибелью или транспортировкой созревающих клеток через кровь в периферические органы.
Периферические органы иммунной системы являются местом встречи Т-и В-лимфоцитов с поступающими туда антигенами, местом распознавания антигенов и развития последовательных стадий специфического иммунного ответа на данный антиген. Распознавание антигена лимфоцитом служит сигналом его усиленной пролиферации, ускоренной дифференцировки и активации. В-лимфоциты после активации в периферических органах иммунной системы дифференцируются в плазматические клетки, продуцирующие и секретирующие антитела — иммуноглобулины. Активированные Т- и В-лимфоциты в периферических органах иммунной системы продуцируют и секретируют межклеточные медиаторы — цитокины, влияющие на иммунный ответ. Там же, в периферических органах иммунной системы, накапливаются и сохраняются долгоживущие Т- и В-лимфоциты, ответственные за поддержание «иммунологической памяти» о встрече с данным антигеном.
Цитокины
Под термином “цитокины” объединяются так называемые ростовые факторы, которые регулируют пролиферацию, дифференцировку и функцию клеток крови, в том числе и клеток иммунной системы. Это обширный класс биохимических веществ, продуцируемый большинством свободных клеток крови, для общения друг с другом, через поверхностные рецепторы на их мембранах. Цитокины оказывают аутокринное и паракринное воздействие. Цитокины можно разделить на несколько “семейств”: интерлейкины, интерфероны, опухольнекротизирующие факторы, трансформирующие факторы роста, хемокины, собственно ростовые факторы и др
Семейство интерферонов. Интерференция - это явление, когда ткани, инфицированные одним вирусом, становятся устойчивыми к заражению другим вирусом. Было установлено, что такая резистентность связана с продукцией зараженными клетками особого белка, который и был назван интерфероном.
В настоящее время интерфероны хорошо изучены. Они представляют собой семейство гликопротеидов с молекулярной массой от 15 000 до 70 000. В зависимости от источника получения эти белки делят на интерфероны I и II типов.
I тип включает ИФН α и β, которые продуцируются инфицированным вирусом клетками: ИФН-α - лейкоцитами, ИФН-β - фибробластами. В последние годы описаны три новых интерферона: ИФН-τ/ε (трофобластный ИФН), ИФН-λ и ИФН-К. В противовирусной защите участвуют ИФН-α и β.
Механизм действия ИФН-α и β не связан с прямым влиянием на вирусы. Он обусловлен активацией в клетке ряда генов, блокирующих репродукцию вируса. Ключевое звено - индукция синтеза протеинкиназы R, которая нарушает трансляцию вирусной мРНК и запускает апоптоз зараженных клеток через Вс1-2 и каспазазависимые реакции. Другой механизм - это активация латентной РНК-эндонуклеазы, которая вызывает деструкцию вирусной нуклеиновой кислоты.
II тип включает интерферон γ. Он продуцируется Т-лимфоцитами и естественными киллерами после антигенной стимуляции.
Эйкозаноиды
Эйкозаноиды - метаболиты арахидоновой кислоты, которая, в свою очередь освобождается из мембранных фосфолипидов в ходе липолиза под действием фосфолипаз. Одни эйкозаноиды являются продуктами циклооксигеназного пути: простагландины, простациклин и тромбоксан, другие - продуктами липоксигеназного пути: лейкотриены.
Эйкозаноиды принадлежат к классу аутокринных или паракринных факторов. Они усиливают или ослабляют действие других агонистов, т.е. их относят к третьим посредникам, к короткоживущим интермедиатам.
Простагландины
Поскольку фосфолипиды всех клеточных мембран содержат арахидоновую кислоту, то и все клетки организма потенциально могут быть источником простагландинов, и они могут проявлять активность в самых разных системах. Действие ПГ проявляется чаще в тех гормоночувствительных клетках, где вторым посредником служит цАМФ: влияют на уровень цАМФ путем изменения активности аденилатциклазы. Следует подчеркнуть многофункциональность биологических эффектов ПГ - ов, причём простагландины групп Е и Г оказывают противоположное действие. Основные эффекты простагландинов
| Процесс | Ткань | Эффект | |
| Сокращение или расслабление гл. мускулатуры | Легкие; матка; ЖКТ; Кровеносные сосуды | Расширение бронхов Сокращение Вазодилятация | |
| Стероидогенез | Кора надпочечников | Стимуляция | |
| Секреция и биосинтез тириоидных гормонов | Щитовидная железа | Имитация эффекта ТТГ | |
| Транспорт солей и воды | Почка | Повышение клиренса своб. Воды | |
| Свертывание крови | Тромбоциты | Торможение или усиление агрегации | |
| Секреция кислоты | Слизистая желудка | Торможение | |
| Липолиз | Адипоциты | Торможение | |
Простациклин и тромбоксан обладают прямо противоположным действием на два принципиально важных процесса: простациклин расслабляет гладкую мускулатуру сосудистой стенки и тормозит агрегацию тромбоцитов; тромбоксан, наоборот, сокращает гладкую мускулатуру сосудов и способствует агрегации тромбоцитов. Одним из основных достижений в изучении простагландинов является установление факта, что они - важнейший компонент развития воспалительного процесса.
Лейкотриены
Эйкозаноиды, биосинтез которых идет по липоксигеназному пути из арахидоновой кислоты. Три лейкотриена: ЛТС4, ЛТД4 и ЛТЕ4 в совокупности являются МРВ-А ( медленно реагирующим веществом, А-анафилаксии). Они секретируются тучными клетками, принимающими участие в реакциях гиперчувствительности. Эффект компонентов МРВ-А в 4000 раз сильнее, чем гистамина в отношении стимуляции гладкой мускулатуры трахеи и бронхов. Эти компоненты действуют и на гладкую мускулатуру ЖКТ, но не столь сильно. Они также действуют и на гладкую мускулатуру артерий. Как и гистамин, компоненты МРВ-А увеличивают проницаемость сосудов.[13]
С -реактивный белок (СРБ)
Очень чувствительный элемент крови, быстрее других реагирующий на повреждение тканей. Наличие реактивного белка в сыворотке крови - признак воспалительного процесса, травмы, проникновения в организм чужеродных микроорганизмов - бактерий, паразитов, грибов. С - реактивный белок стимулирует защитные реакции, активирует иммунитет.
Содержание СРБ в сыворотке крови - до 0,5 мг/л считается нормой. Уже через 4-6 часов после того, как в организм проникает инфекция, развивается воспалительный процесс, который может сопровождаться опухолями, уровень СРБ начинает быстро расти. Чем острее воспалительный процесс, активнее заболевание, тем выше СРБ в сыворотке крови. Когда заболевание в хронической форме переходит в фазу, то содержание СРБ в крови практически не обнаруживается. Как наступает обострение, СРБ снова начинает расти.
Пептиды малой плотности
Пептиды малой плотности (ПМП) - относятся к новому классу регуляторных молекул, являющиеся катионными белками, открытыми в середине 80-х годов R.Lehrer и В.Н. Кокряковым.
ПМП обладают широким спектром прямой противомикробной активацией, в частности подавляют рост грамположительных и грамотрицательных бактерий, грибов, некоторых вирусов. В настоящее время известны два больших класса ПМП человека: дефензины и кателецидины. Они действуют как эндогенные антибиотики и участвуют в передаче сигналов клеткам, вовлечения в процесс иммунной защиты. В основном эти белки синтезируются эпителиальными клетками покровных тканей и активированы. Недавно получены данные о том, что кателицидин LL-37 обладает прямым действием на вирус осповакцины.[7,13]
Пропердин
Пропердин или фактор Р-белок, содержащийся в сыворотке крови. Система пропердина состоит из самого фактора Р и 3-х дополнительных белков (А,В,0).
Все они принимают участие в активации комплемента - в расщеплении С3 компонента, который в свою очередь обладает выраженными антимикробными свойствами, стимулятором фагоцитоза. Все эти субстанции имеются в организме и не нужно времени на их образование.[4]
Цитокины
Под термином “цитокины” объединяются так называемые ростовые факторы, которые регулируют пролиферацию, дифференцировку и функцию клеток крови, в том числе и клеток иммунной системы. Это обширный класс биохимических веществ, продуцируемый большинством свободных клеток крови, для общения друг с другом, через поверхностные рецепторы на их мембранах. Цитокины оказывают аутокринное и паракринное воздействие.
Рецепторы-киназы
Впервые рецепторы опознавания паттерна были открыты у растений[1]. Позже множество гомологичных рецепторов было обнаружено при анализе геномов растений (у риса 370, у Arabidopsis — 47). В отличие от рецепторов опознавания паттерна у животных, которые связывают внутриклеточные протеинкиназы с помощью адапторных белков, растительные рецепторы представляют собой один белок, состоящий из нескольких доменов, внеклеточного, опознающего патоген, внутриклеточного, обладающего киназной активностью, и трансмембранного, связывающего первые два.
Толл-подобные рецепторы
Этот класс рецепторов опознает патогены вне клеток или в эндосомах[2]. Они были впервые обнаружены у дрозофилы и индуцируют синтез и секрецию цитокинов, необходимых для активации иммунного ответа. В настоящее время толл-подобные рецепторы обнаружены у многих видов. У животных их насчитывают 11 (TLR1-TLR11). Взаимодействие толл-подобных рецепторов с лигандами приводит к индукции сигнальных путей NF-kB и МАР-киназы, которые, в свою очередь, индуцируют синтез и секрецию цитокинов и молекул, стимулирующих презентацию антигена[3].
Nod-подобные рецепторы
Nod-подобные рецепторы — это цитоплазматические белки с различными функциями. У млекопитающих их найдено около 20, и большинство из них подразделяют на два главных подсемейства: NOD и NALP. Кроме того, к этому семейству рецепторов относят трансактиватор главного комплекса гистосовместимости класса II и некоторые другие молекулы. Опознавая патоген внутри клетки, рецепторы олигомеризуются и образуют инфламмасому, активирующую ферменты протеолитической активации цитокинов, например, интерлейкина 1 бета. Рецепторы активируют также сигнальный путь NF-kB и синтез цитокинов[4][5].
NODS
Известны два главных представителя: NOD1 и NOD2. Связывают два разных бактериальных пептидогликана[6].
NALPS
Известно 14 белков (NALP1 — NALP14), которые активируются бактериальными пептидогликанами, ДНК, двухцепочечной РНК, парамиксовирусом и мочевой кислотой. Мутации некоторых из NALPS являются причиной наследственных аутоиммунных заболеваний.
РНК хеликазы
Индуцируют антивирусный иммунный ответ после активации вирусной РНК. У млекопитающих это три молекулы: RIG-I, MDA5 и LGP2.
Система комплемента
Комплемент - система сывороточных белков и нескольких белков клеточных мембран, выполняющих 3 важные функции: опсонизацию микроорганизмов для дальнейшего их фагоцитоза, инициацию сосудистых реакций воспаления и перфорацию мембран бактериальных и других клеток. Компоненты комплементаобозначают буквами латинского алфавита C, B и D с добавлением арабской цифры (номер компонента) и дополнительных строчных букв. Компоненты классического пути обозначают латинской буквой «С» и арабскими цифрами (C1, C2 ... C9), для субкомпонентов комплемента и продуктов расщепления к соответствующему обозначению добавляют строчные латинские буквы (C1q, C3b и т.д.). Активированные компоненты выделяют чертой над литерой, инактивированные компоненты - буквой «i» (например, iC3b).
• Активация комплементаВ норме, когда внутренняя среда организма «стерильна» и патологического распада собственных тканей не происходит, уровень активности системы комплемента невысок. При появлении во внутренней среде микробных продуктов происходит активация системы комплемента. Она может происходить по трём путям: альтернативному, классическому и лектиновому.
- Альтернативный путь активации.Его инициируют непосредственно поверхностные молекулы клеток микроорганизмов [факторы альтернативного пути имеют буквенное обозначение: P (пропердин), B и D].
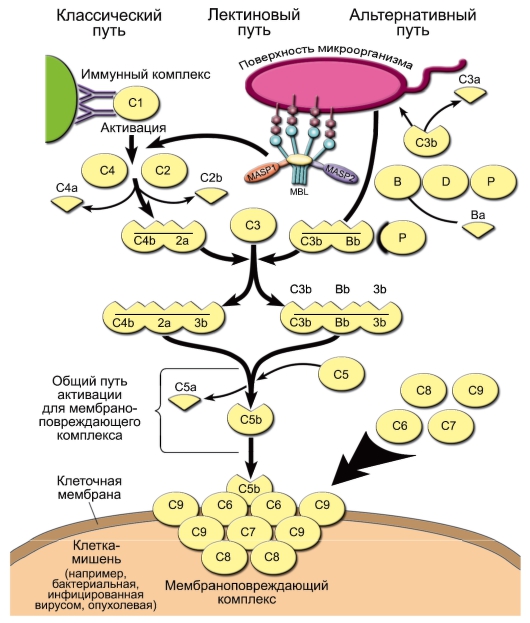
Из всех белков системы комплемента в сыворотке крови больше всего C3 - его концентрация в норме составляет 1,2 мг/мл. При этом всегда имеется небольшой, но значимый уровень спонтанного расщепления C3 с образованием C3a и C3b. Компонент C3b - опсонин, т.е. он способен ковалентно связываться как с поверхностными молекулами микроорганизмов, так и с рецепторами на фагоцитах. Кроме того, «осев» на поверхности клеток, C3b связывает фактор В. Тот, в свою очередь, становится субстратом для сывороточной сериновой протеазы - фактора D, который расщепляет его на фрагменты Ва и Bb. C3b и Bb образуют на поверхности микроорганизма активный комплекс, стабилизируемый пропердином (фактор Р).
◊ Комплекс C3b/Bb служит С3-конвертазой и значительно повышает уровень расщепления С3 по сравнению со спонтанным. Кроме того, после связывания с C3 он расщепляет C5 до фрагментов C5a и C5b. Малые фрагменты C5a (наиболее сильный) и C3a - анафилатоксины комплемента, т.е. медиаторы воспалительной реакции. Они создают условия для миграции фагоцитов в очаг воспаления, вызывают дегрануляцию тучных клеток, сокращение гладких мышц. C5a также вызывает повышение экспрессии на фагоцитах CR1 и CR3.
◊ С C5b начинается формирование «мембраноатакующего комплекса», вызывающего перфорацию мембраны клеток микроорганизмов и их лизис. Сначала образуется комплекс C5b/C6/ C7, встраивающийся в мембрану клетки. Одна из субъединиц компонента C8 - C8b - присоединяется к комплексу и катализирует полимеризацию 10-16 молекул C9. Этот полимер и формирует неспадающуюся пору в мембране, имеющую диаметр около 10 нм. В результате клетки становятся неспособными поддерживать осмотический баланс и лизируются.
- Классический и лектиновый путисходны друг с другом и отличаются от альтернативного способом активации C3. Главной C3конвертазой классического и лектинового пути служит комплекс C4b/C2a, в котором протеазной активностью обладает C2a, а C4b ковалентно связывается с поверхностью клеток микроорганизмов. Примечательно, что белок C2 гомологичен фактору В, даже их гены расположены рядом в локусе MHC-III.
◊ При активации по лектиновому пути один из белков острой фазы - MBL - взаимодействует с маннозой на поверхности клеток микроорганизмов, а MBL-ассоциированная сериновая протеаза (MASP - Mannose-bindingprotein-Associated Serine Protease) катализирует активационное расщепление C4 и C2.
◊ Сериновой протеазой классического пути служит C1s, одна из субъединиц комплекса C1qr2s2. Она активируется, когда по крайней мере 2 субъединицы C1q связываются с комплексом антиген-антитело. Таким образом, классический путь активации комплемента связывает врождённый и адаптивный иммунитет.
• Рецепторы компонентов комплемента.Известно 5 типов рецепторов для компонентов комплемента (CR - Complement Receptor) на различных клетках организма.
- CR1 экспрессирован на макрофагах, нейтрофилах и эритроцитах. Он связывает C3b и C4b и при наличии других стимулов к фагоцитозу (связывания комплексов антиген-антитело через FcyR или при воздействии ИФНу - продукта активированных T-лимфоцитов) оказывает пермиссивное действие на фагоциты. CR1 эритроцитов через C4b и C3b связывает растворимые иммунные комплексы и доставляет их к макрофагам селезёнки и печени, обеспечивая тем самым клиренс крови от иммунных комплексов. При нарушении этого механизма иммунные комплексы выпадают в осадок - прежде всего в базальных мембранах сосудов клубочков почек (CR1 есть и на подоцитах клубочков почек), приводя к развитию гломерулонефрита.
- CR2 B-лимфоцитов связывает продукты деградации C3 - C3d и iC3b. Это в 10 000-100 000 раз увеличивает восприимчивость B-лимфоцита к своему антигену. Эту же мембранную молекулу - CR2 - использует в качестве своего рецептора вирус Эпштейна-Барр - возбудитель инфекционного мононуклеоза.
- CR3 и CR4 также связывают iC3b, который, как и активная форма C3b, служит опсонином. В случае если CR3 уже связался с растворимыми полисахаридами типа бета-глюканов, связывания iC3b с CR3 самого по себе достаточно для стимуляции фагоцитоза.
- C5aR состоит из семи доменов, пенетрирующих мембрану клетки. Такая структура характерна для рецепторов, связанных с G-белками (белки, способные связывать гуаниновые нуклеотиды, в том числе ГТФ).
• Защита собственных клеток.Собственные клетки организма защищены от деструктивных воздействий активного комплемента благодаря так называемым регуляторным белкам системы комплемента.
- C1-ингибитор(C1inh) разрушает связь C1q с C1r2s2, тем самым ограничивая время, в течение которого C1s катализирует активационное расщепление C4 и C2. Кроме того, C1inh ограничивает спонтанную активацию C1 в плазме крови. При генетическом дефекте dinh развивается наследственный ангионевротический отёк. Его патогенез состоит в хронически повышенной спонтанной активации системы комплемента и избыточном накоплении анафилактинов (C3a и С5а), вызывающих отёки. Заболевание лечат заместительной терапией препаратом dinh.
- C4-связывающий белок- C4BP (C4-Binding Protein) связывает C4b, предотвращая взаимодействие C4b и С2а.
- DAF(Decay-Accelerating Factor - фактор, ускоряющий деградацию, CD55) ингибирует конвертазы классического и альтернативного путей активации комплемента, блокируя формирование мембраноатакующего комплекса.
- Фактор H(растворимый) вытесняет фактор В из комплекса с C3b.
- Фактор I(сывороточная протеаза) расщепляет C3b на C3dg и iC3b, а C4b - на C4c и C4d.
- Мембранный кофакторный белок MCP(Membrane Cofactor Protein, CD46) связывает C3b и C4b, делая их доступными для фактора I.
- Протектин(CD59). Связывается с C5b678 и предотвращает последующее связывание и полимеризацию С9, блокируя тем самым образование мембраноатакующего комплекса. При наследственном дефекте протектина или DAF развивается пароксизмальная ночная гемоглобинурия. У таких больных эпизодически возникают приступы внутрисосудистого лизиса собственных эритроцитов активированным комплементом и происходит экскреция гемоглобина почками.
Нейтрофилы и макрофаги.
Способностью к эндоцитозу (поглощению частиц с образованием внутриклеточной вакуоли) обладают все эукариотические клетки. Именно таким образом внутрь клеток проникают многие патогенные микроорганизмы. Однако в большинстве инфицированных клеток отсутствуют механизмы (либо они слабы), обеспечивающие деструкцию патогена.
Нейтрофилы и мононуклеарные фагоциты имеют общее миелоидное происхождение из стволовой кроветворной клетки. Однако эти клетки различаются рядом свойств.
Нейтрофилы - наиболее многочисленная и подвижная популяция фагоцитов, созревание которых начинается и заканчивается в костном мозгу. Около 70% всех нейтрофилов сохраняется в виде резерва в костно-мозговых депо, откуда они под влиянием соответствующих стимулов (провоспалительных цитокинов, продуктов микробного происхождения, С5а-компонента комплемента, колониестимулирующих факторов, кортикостероидов, катехоламинов) могут экстренно перемещаться через кровь в очаг тканевой деструкции и участвовать в развитии острого воспалительного ответа. Нейтрофилы - это «отряд быстрого реагирования» в системе антимикробной защиты.
Нейтрофилы - короткоживущие клетки, продолжительность их жизни около 15 сут. Из костного мозга они выходят в кровоток уже зрелыми клетками, утратившими способность к дифференцированию и пролиферации. Из крови нейтрофилы перемещаются в ткани, в которых они либо гибнут, либо выходят на поверхность слизистых оболочек, где и заканчивают свой жизненный цикл.
Моноциты, в отличие от нейтрофилов, - незрелые клетки, которые, попадая в кровяное русло и далее в ткани, созревают в тканевые макрофаги (плевральные и перитонеальные, купферовские клетки печени, альвеолярные, интердигитальные клетки лимфатических узлов, костного мозга, остеокласты, микроглиоциты, мезангиальные клетки почек, сертолиевы клетки яичек, клетки Лангерганса и Гринстейна кожи). Продолжительность жизни мононуклеарных фагоцитов от 40 до 60 сут.
Макрофаги - не очень быстрые клетки, но они рассеяны во всех тканях, и, в отличие от нейтрофилов, им нет необходимости в столь срочной мобилизации. Если продолжить аналогию с нейтрофилами, то макрофаги в системе врожденного иммунитета - это «войска специального назначения».
Важной особенностью нейтрофилов и макрофагов является наличие в их цитоплазме большого количества лизосом. Нейтрофилы и макрофаги чутко реагируют на любые изменения гомеостаза. Для этой цели они оснащены богатым арсеналом рецепторов, располагающихся на их цитоплазматической мембране.
Основной функцией нейтрофилов и макрофагов является фагоцитоз.
Не все микроорганизмы чувствительны к бактерицидным системам фагоцитов. Гонококки, стрептококки, микобактерии и другие выживают после контакта с фагоцитами, такой фагоцитоз называется незавершенным.
Фагоциты, помимо фагоцитоза (эндоцитоза), могут осуществлять свои цитотоксические реакции путем экзоцитоза - выделения своих гранул наружу (дегрануляция) - таким образом фагоциты осуществляют внеклеточный киллинг. Нейтрофилы, в отличие от макрофагов, способны образовывать внеклеточные бактерицидные ловушки - в процессе активации клетка выбрасывает наружу нити ДНК, в которых располагаются гранулы с бактерицидными ферментами. Благодаря липкости ДНК бактерии приклеиваются к ловушкам и под действием фермента погибают.
Нейтрофилы эффективны при инфекциях, вызванных внеклеточными патогенами (гноеродные кокки, энтеробактерии и др.), индуцирующими развитие острого воспалительного ответа. При таких инфекциях эффективна кооперация нейтрофил-комплемент-антитело. Макрофаги защищают от внутриклеточных патогенов (микобактерии, риккетсии, хламидии и др.), вызывающих развитие хронического гранулематозного воспаления, где главную роль играет кооперация макрофаг-Т- лимфоцит.
Помимо участия в антимикробной защите, фагоциты участвуют в удалении из организма отмирающих, старых клеток и продуктов их распада, неорганических частиц (уголь, минеральная пыль и др.). Фагоциты (особенно макрофаги) являются антигенпредставляющими, они обладают секреторной функцией, синтезируют и выделяют наружу широкий спектр биологически активных соединений: цитокины (интерлейкины-1, 6, 8, 12, фактор некроза опухоли), простагландины, лейкотриены, интерфероны α и γ. Благодаря этим медиаторам фагоциты активно участвуют в поддержании гомеостаза, в процессах воспаления, в адаптивном иммунном ответе, регенерации.
Эозинофилыотносятся к полиморфно-ядерным лейкоцитам. Они отличаются от нейтрофилов тем, что обладают слабой фагоцитарной активностью. Эозинофилы поглощают некоторые бактерии, но внутриклеточный киллинг у них менее эффективен, чем у нейтрофилов.
Основная функция эозинофилов заключается в защите от крупных паразитов. После активации эти клетки выделяют токсичные продукты своих гранул, оказывающих губительное действие на гельмины. К таким продуктам относят: катионный белок - РНКазу, пероксидазу эозинофилов; главный основной белок эозинофилов - основной компонент гранул, который способен полимеризоваться в оболочке паразита с образованием трансмембранных пор, через которые внутрь мишени проникают другие медиаторы.
Естественные киллеры. Естественные киллеры - большие лимфоцитоподобные клетки, которые происходят из лимфоидных предшественников. Они содержатся в крови, тканях, особенно их много в печени, слизистой оболочке репродуктивной системы женщин, селезенке. Естественные киллеры, как и фагоциты, содержат лизосомы, но фагоцитарной активностью не обладают.
Классификация антигенов
Основываясь на отдельных характерных свойствах, все многообразие антигенов можно классифицировать по происхождению, природе, молекулярной структуре, степени иммуногенности, степени чужеродности, направленности активации и обеспеченности иммунного реагирования.
По происхождению различают экзогенные (возникшие вне организма) и эндогенные (возникшие внутри организма) антигены. Среди эндогенных особого внимания заслуживают ауто- и неоантигены. Аутогенные антигены (аутоантигены) - это структурно неизмененные антигены собственного организма, синтезируемые в организме в физиологических условиях. В норме аутоантигены неиммуногенны вследствие сформировавшейся иммунологической толерантности(невосприимчивости) либо их недоступности для контакта с факторами иммунитета - это так называемые забарьерные антигены. При срыве толерантности или нарушении целостности биологических барьеров (воспаление, травма) компоненты иммунной системы начинают специфически реагировать на аутоантигены выработкой специфических факторов иммунитета (аутоантитела, клон аутореактивных лимфоцитов). Неоантигены, в отличие от аутоантигенов, возникают в организме в результате генетических мутаций или модификаций и всегда чужеродны.
По природе: биополимеры белковой (протеиды) и небелковой (полисахариды, липиды, липополисахариды, нуклеиновые кислоты и др.) природы.
По молекулярной структуре: глобулярные (молекула имеет шаровидную форму) и фибриллярные (форма нити).
По степени иммуногенности: полноценные и неполноценные. Полноценные антигены обладают выраженной антигенностью и иммуногенностью - иммунная система чувствительного организма реагирует на их введение выработкой факторов иммунитета. Такие вещества, как правило, имеют достаточно большую молекулярную массу (более 10 кД), большой размер молекулы (частицы) в виде глобулы и хорошо взаимодействуют с факторами иммунитета.
Неполноценные антигены, или гаптены (термин предложен К. Ландштейнером), обладают антигенностью - способны специфически взаимодействовать с уже готовыми факторами иммунитета (антителами, лимфоцитами), но не способны при введении в нормальных условиях индуцировать в организме иммунный ответ. Чаще всего гаптенами являются низкомолекулярные соединения (молекулярная масса менее 10 кД).
По степени чужеродности: ксено-, алло- и изоантигены. Ксеногенные антигены (или гетерологичные) - общие для организмов, стоящих на разных ступенях эволюционного развития.
Аллогенные антигены (или групповые) - общие для генетически неродственных организмов, но относящихся к одному виду.
Изогенные антигены (или индивидуальные) - общие только для генетически идентичных организмов.
В пределах отдельного организма в определенных органах или тканях обнаруживаются специфичные для них антигены, которые нигде больше не встречаются. Такие антигены получили название органо- и тканеспецифических.
В зависимости от физико-химических свойств антигена, условий его внедрения, характера реакции и реактивности макроорганизма различают иммуногены, толерогены и аллергены.
По направленности активации и обеспеченности иммунного реагирования, т.е. необходимости вовлечения Т-лимфоцитов в индукцию иммунного ответа, выделяют Т-зависимые и Т-независимыеантигены.
От Т-независимых антигенов следует отличать суперантигены. Это группа веществ, в основном микробного происхождения, которые могут неспецифически вызывать поликлональную реакцию.
Антигены микробов и клеток человека (CD, MHC). Гаптены
Антигены организма человека
В организме человека выделяют множество разнообразных антигенов. Они не только нужны для полноценного развития и функционирования всего организма в целом, но также несут важную информацию при клинико-лабораторной диагностике, определении иммунной совместимости органов и тканей в трансплантологии, а также в научных исследованиях. Наибольший медицинский интерес из числа аллогенных антигенов представляют антигены групп крови, среди изогенных - антигены гистосовместимости, а в группе органо- и тканеспецифических - раково-эмбриональные антигены.
Антигены групп крови человека
Антигены групп крови человека располагаются на цитоплазматической мембране клеток, но наиболее легко определяются на поверхности эритроцитов. Поэтому они получили название«эритроцитарные антигены». На сегодняшний день известно более 250 различных эритроцитарных антигенов. Однако наиболее важное клиническое значение имеют антигены системы АВ0 и Rh (резус-фактор).
Антигены системы АВ0 обнаруживаются в плазме крови, лимфе, секретах слизистых оболочек и других биологических жидкостях, но наиболее выражены на эритроцитах. Они синтезируются многими клетками организма, включая ядросодержащие предшественники эритроцитов, и свободно секретируются в межклеточное пространство. На мембране клеток эти антигены могут появиться либо как продукт клеточного биосинтеза, либо в результате сорбции из межклеточных жидкостей.
Антигены системы АВ0 представляют собой высокогликозилированные пептиды: 85% приходится на углеводную часть и 15% - на полипептидную. Пептидный компонент состоит из 15 аминокислотных остатков. Он постоянен для всех групп крови АВ0 и иммунологически инертен. Иммуногенность молукулы антигена системы АВ0 определяется его углеводной частью.
В системе антигенов АВ0 выделяют три варианта антигенов, различающихся по строению углеводной части: Н, А и В.
Антигены системы АВ0 определяют в реакции агглютинации. Однако, учитывая высокий популяционный полиморфизм данной антигенной системы, перед гемотрансфузией обязательно проводят биологическую пробу на совместимость крови реципиента и донора.
Другой важнейшей системой эритроцитарных антигенов является система резус-антигенов (Rh) или резус-факторов. Эти антигены синтезируются предшественниками эритроцитов и обнаруживаются главным образом на эритроцитах, так как они водонерастворимы. Резус-антиген представляет собой термолабильный липопротеид. Выделяют 6 разновидностей этого антигена. Генетическая информация о его строении закодирована в многочисленных аллелях трех сцепленных между собой локусов (D/d, C/c, E/e). В зависимости от наличия или отсутствия резус-антигена в популяции людей различают две группы: резус-положительных и резус-отрицательных индивидуумов.
Совпадение по резус-антигену важно не только при переливании крови, но также для течения и исхода беременности. При беременности резус-отрицательной матери резус-положительным плодом может развиться резус-конфликт. Это патологическое состояние связано с выработкой антирезусных антител, способных вызвать иммунологический конфликт: невынашивание беременности или желтуху новорожденного (внутрисосудистый иммунный лизис эритроцитов).
Антигены гистосовместимости
На цитоплазматических мембранах практически всех клеток макроорганизма обнаруживаютсяантигены гистосовместимости. Большая часть из них относится к системе главного комплекса гистосовместимости, или MHC (от англ. Main Hystocompatibility Complex). Установлено, что антигены гистосовместимости играют ключевую роль в осуществлении специфического распознавания «свой-чужой» и индукции приобретенного иммунного ответа, определяют совместимость органов и тканей при трансплантации в пределах одного вида и другие эффекты.
MHC имеет сложную структуру и высокую полиморфность. Антигены гистосовместимости представляют собой гликопротеины, прочно связанные с цитоплазматической мембраной клеток. Их отдельные фрагменты имеют структурное сходство с молекулами иммуноглобулинов и поэтому относятся к единому суперсемейству. Различают два основных класса молекул MHC (I и II), которые объединяют множество сходных по структуре антигенов, кодируемых множеством аллельных генов. На клетках индивидуума могут одновременно экспрессироваться не более двух разновидностей продуктов каждого гена MHC. MHC I класса индуцирует преимущественно клеточный иммунный ответ, а MHC II класса - гуморальный.
В структуре и функции MHC II класса есть ряд принципиальных отличий. Комплекс образован двумя нековалентно связанными полипептидными цепями (α и β), имеющими сходное доменное строение. Обе цепи являются трансмембранными пептидами и «заякорены» в цитоплазматической мембране. Щель Бъеркмана в MHC II класса образована одновременно обеими цепями. Она вмещает олигопептид размером 12-25 аминокислотных остатков, недосягаемый специфическими антителами. MHC II класса включает в себя пептид, захваченный из внеклеточной среды путем эндоцитоза, а не синтезированный самой клеткой. Молекулы МНС II класса экспрессируются на поверхности ограниченного числа клеток: дендритных, В-лимфоцитах, Т-хелперах, активированных макрофагах, тучных, эпителиальных и эндотелиальных клетках.
MHC II класса участвуют в индукции приобретенного иммунного ответа. Фрагменты молекулы антигена экспрессируются на цитоплазматической мембране особой группы клеток, которая получила название антигенпрезентирующих. Осно
