Факторы, способствующие развитию ОДН
• Возрастание давления в системе легочной артерии
• Избыток жидкости
• Снижение коллоидно-осмотического давления
• Панкреатит, перитонит, кишечная непроходимость
• Ожирение
• Старческий возраст
• Курение
• Дистрофия
• Кифосколиоз
ОДН возникает в результате нарушений в цепи регуляторных механизмов, включая центральную регуляцию дыхания, нейромышечную передачу и газообмен на уровне альвеол.
Поражение легких, одного из первых «органов-мишеней», обусловлено как характерными для критических состояний патофизиологическими сдвигами, так и функциональными особенностями легких — их участием во многих метаболических процессах. Эти состояния часто осложняются развитием неспецифической реакции, которая реализуется иммунной системой. Реакцию на первичное воздействие объясняют действием медиаторов — арахидоновой кислоты и ее метаболитов (простагландины, лейкотриены, тромбоксан А2, серотонин, гистамин, B-эпинефрин, фибрин и продукты его распада, комплемент, супероксид-радикал, полиморфнонуклеарные лейкоциты, тромбоциты, свободные жирные кислоты, брадикинины, протеолитические и лизосомальные ферменты). Эти факторы в сочетании с первичным стресс-воздействием вызывают повышенную сосудистую проницаемость, приводящую к синдрому капиллярного просачивания, т.е. отеку легких.
Таким образом, этиологические факторы ОДН можно объединить в две группы — внелегочные и легочные.
Внелегочные факторы:
• поражения ЦНС (центрогенная ОДН);
• поражения нейромышечного аппарата (нейромышечная ОДН);
• поражения грудной клетки и диафрагмы (торакоабдоминальная ОДН);
• другие экстралегочные причины (левожелудочковая недостаточность, сепсис, дисбаланс электролитов, дефицит энергии, избыток жидкости, уремия и др.).
Легочные факторы:
• обструкция дыхательных путей (обструктивная ОДН);
• поражение бронхов и легких (бронхолегочная ОДН);
• нарушения вентиляции из-за плохой растяжимости легких (рестриктивная ОДН);
• нарушения процессов диффузии (альвеолокапиллярная, блок-диффузионная ОДН);
• нарушения легочного кровообращения.
Клиническая картина. При острых расстройствах дыхания нарушаются оксигенация артериальной крови и выведение углекислоты. В одних случаях преобладают явления артериальной гипоксемии — эту форму нарушений принято называть гипоксемической дыхательной недостаточностью. Поскольку гипоксемия наиболее характерна для паренхиматозных легочных процессов, ее также называют паренхиматозной дыхательной недостаточностью. В других случаях преобладают явления гиперкапнии — гиперкапническая, или вентиляционная, форма дыхательной недостаточности.
Гипоксемическая форма ОДН. Причинами этой формы дыхательной недостаточности могут быть: легочный шунт (сброс крови справа налево), несоответствие вентиляции и кровотока, альвеолярная гиповентиляция, нарушения диффузии и изменения химических свойств гемоглобина. Важно выявить причину гипоксемии. Альвеолярную гиповентиляцию легко определить при исследовании РаСО2. Артериальная гипоксемия, возникающая при изменениях отношения вентиляция/кровоток или при ограничении диффузии, обычно устраняется дополнительным назначением кислорода. При этом вдыхаемая фракция кислорода (ВФК) не превышает 5 %, т.е. равна 0,5. При наличии шунта увеличение ВФК очень незначительно влияет на уровень кислорода в артериальной крови. Отравление окисью углерода не приводит к снижению РаО2, но сопровождается значительным снижением содержания кислорода в крови, поскольку происходит замена части гемоглобина карбоксигемоглобином, неспособным переносить кислород.
Гипоксемическая форма ОДН может возникать на фоне сниженного, нормального или высокого уровня углекислоты в крови. Артериальная гипоксемия ведет к ограничению транспорта кислорода к тканям. Эта форма ОДН характеризуется быстро прогрессирующим течением, невыраженностью клинических симптомов и возможностью летального исхода в течение короткого промежутка времени. Наиболее частые причины гипоксемической формы ОДН: РДСВ, травмы грудной клетки и легких, нарушения проходимости дыхательных путей.
В диагностике гипоксемической формы ОДН следует обращать внимание на характер дыхания: инспираторный стридор — при нарушениях проходимости верхних дыхательных путей, экспираторная одышка — при бронхообструктивном синдроме, парадоксальное дыхание — при травме грудной клетки, прогрессирующее олигопноэ (поверхностное дыхание, снижение МОД) с возможностью апноэ. Другие клинические признаки не выражены. Вначале тахикардия с умеренной артериальной гипертензией. С самого начала возможны неспецифические неврологические проявления: неадекватность мышления, спутанность сознания и речи, заторможенность и т.д. Цианоз не выражен, лишь при прогрессировании гипоксии он становится интенсивным, внезапно нарушается сознание, затем наступает кома (гипоксическая) с отсутствием рефлексов, падает АД, и наступает остановка сердца. Продолжительность гипоксемической ОДН может колебаться от нескольких минут (при аспирации, асфиксии, синдроме Мендельсона) до нескольких часов и дней (РДСВ).
Таким образом, главным в тактике врача является быстрое установление диагноза, причины, вызвавшей ОДН, и проведение неотложных экстренных мер по лечению данного состояния.
Гиперкапническая форма ОДН. К гиперкапнической ОДН относят все случаи острой гиповентиляции легких, независимо от причины возникновения: 1) центрального происхождения; 2) вызванную нейромышечными нарушениями; 3) гиповентиляцию при травме грудной клетки, астматическом состоянии, хронических обструктивных заболеваниях легких (ХОЗЛ).
В отличие от гипоксемической гиперкапническая ОДН сопровождается многими клиническими проявлениями, зависящими от стимуляции адренергической системы в ответ на повышение РаСО2. Нарастание РСО2 приводит к стимуляции дыхательного центра, следствием которой должно быть значительное повышение всех параметров внешнего дыхания. Однако этого не происходит из-за патологического процесса. Если при этом осуществляется активная оксигенация, то может наступить апноэ в результате депрессии дыхательного центра. Повышение АД при гиперкапнии обычно более значительно и стойко, чем при гипоксии. Оно может возрасти до 200 мм рт.ст. и более, а мозговые симптомы тем более выражены, чем медленнее развивается гиперкапния. При легочном сердце артериальная гипертензия менее выражена и переходит в гипотензию в связи с декомпенсацией правого сердца. Очень характерные симптомы гиперкапнии — значительная потливость и заторможенность. Если помочь больному откашляться и ликвидировать бронхиальную обструкцию, то заторможенность исчезает. Гиперкапнии также свойственна олигурия, которая всегда присутствует при выраженном дыхательном ацидозе.
Декомпенсация состояния наступает в тот момент, когда высокий уровень РСО2 крови перестает стимулировать дыхательный центр. Признаками декомпенсации служат резкое снижение МОД, расстройство кровообращения и развитие комы, которая при прогрессирующей гиперкапнии представляет собой СО2-наркоз. РаСО2 при этом достигает 100 мм рт.ст., но кома может наступить раньше из-за имеющейся гипоксемии. В этой стадии необходимо не только проводить оксигенацию, но и ИВЛ для элиминации углекислоты. Развитие шока на фоне коматозного состояния означает начало быстрого повреждения клеточных структур мозга, внутренних органов и тканей.
Клинические признаки прогрессирующей гиперкапнии:
• нарушения дыхания (одышка, постепенное уменьшение дыхательного и минутного объемов дыхания, олигопноэ, бронхиальная гиперсекреция, невыраженный цианоз);
• нарастающая неврологическая симптоматика (безразличие, агрессивность, возбуждение, заторможенность, кома);
• сердечно-сосудистые нарушения (тахикардия, стойкое повышение АД, затем декомпенсация сердечной деятельности, гипоксическая остановка сердца на фоне гиперкапнии).
ДиагностикаОДН основана на клинических признаках и изменениях газов артериальной крови и рН.
Признаки ОДН:
• острое нарушение дыхания (олигопноэ, тахипноэ, брадипноэ, апноэ, патологические ритмы);
• прогрессирующая артериальная гипоксемия(РаO2 < 50 мм рт.ст. при дыхании воздухом);
• прогрессирующая гиперкапния (РаСO2 > 50 мм рт.ст.);
• рН < 7,3
Все эти признаки выявляются не всегда. Диагноз ставят при наличии хотя бы двух из них.
Глава 3
РЕСПИРАТОРНАЯ ТЕРАПИЯ
Респираторная терапия включает в себя комплекс мероприятий, направленных на восстановление вентиляционной и газообменной функций легких. Ее важнейшие составные элементы — обеспечение свободной проходимости дыхательных путей, кислородная и лекарственная терапия, ингаляции, применение респираторной поддержки при несостоятельном спонтанном дыхании больного.
В настоящей главе рассматриваются вопросы оксигенотерапии, применение бронходилататоров, кортикостероидов и других лекарственных средств, а также общие положения и правила, которыми руководствуются при лечении ОДН.
ОКСИГЕНОТЕРАПИЯ
Оксигенотерапия показана во всех случаях остро возникающей артериальной гипоксемии.
Относительно безопасный уровень РаО2 — 60 мм рт.ст., поскольку он не сопровождается значительными изменениями SaO2. При этом SaO2 снижается до 90 % (норма 95—98 %), а содержание кислорода в артериальной крови до 18 мл/100 мл (норма 20 мл/100 мл). Даже небольшое повышение FiO2 с 0,21 до 0,24 ведет к восстановлению нормального уровня кислорода в крови.
В тех же случаях, когда гипоксемия более значительна иРаО2 становится ниже 50 мм рт.ст., кривая диссоциацииHbО2 резко падает, что обусловливает значительное снижениеSaO2.
Так, если РаО2 снижается с 60 до 40 мм рт.ст., SaO2 падает до 75 % и становится равным по этому показателю насыщению венозной крови. Содержание кислорода в крови при этом снижается до 15 мл/100 мл. Поэтому уровень РаО2 50 мм рт.ст. и ниже следует рассматривать как критический, при котором показания к кислородотерапии можно определить как экстренные. Даже небольшое повышение РаО2, достигаемое с помощью окси гемотерапии, будет способствовать значительному ростуSаO2 и содержания кислорода в артериальной крови (рис. 3.1).
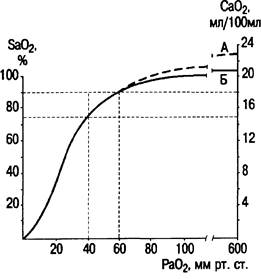
Рис. 3.1. Кривая диссоциации оксигемоглобина.
Верхняя пунктирная линия (А) соответствует общему содержанию кислорода в артериальной крови при рН 7,4, РС02 = 40 мм рт.ст. и 37 °С. Непрерывная кривая (Б) соответствует количеству кислорода, связанного с гемоглобином.
Токсичность кислорода. Во всех случаях кислородотерапии требуется осторожность. Токсичность кислорода подтверждается данными экспериментальных исследований и клинических наблюдений. Дыхание чистым кислородом в течение 3—5 дней может привести к гибели экспериментальных животных. Имеются указания на то, что высокие концентрации кислорода могут быть причиной РДСВ. Какие концентрации кислорода могут приводить к токсическому эффекту, не установлено.
Безопасная FiО2 равна 0,21, т.е. соответствует концентрации кислорода в атмосферном воздухе. Следует полагать, что FiО2 0,4, используемая длительное время, также безопасна, а FiО2 0,5 возможно нетоксична, но ее назначение должно быть строго аргументировано. При этом, однако, нужно учитывать и возрастные факторы, поскольку с возрастом нормальные уровни РаО2 и SаO2 снижаются. Любого больного, получающего кислород в концентрации более 60 %, относят к группе высокого риска.
Опасность гипероксигенации документируется тем, что небольшая часть кислорода (1—2 %) претерпевает одноэлектронное восстановление до воды, в процессе которого в качестве промежуточных продуктов образуются высокореактивные свободно-радикальные формы кислорода. Они могут вызывать окисление биомакромолекул и инициировать цепные процессы, способные приводить к повреждению мембраны клетки [супероксидный анионрадикал кислорода, пероксид кислорода (Н2О2), гидроксильный радикал (ОН)]. Липиды — основной компонент биологических мембран — представляют собой легко окисляющиеся соединения. Многие продукты ПОЛ (гидропероксиды, альдегиды, кетоны и др.) высокотоксичны и способны повреждать биологические мембраны. Защитные механизмы обеспечивают ферменты, ускоряющие превращение токсичных метаболитов в воду. Вторая линия защиты — фенольные антиоксиданты, серосодержащие соединения, каротиноиды и витамины А, С и Е.
Витамин С может проявлять прооксидантную активность. Витамин Е (альфа-токоферола ацетат) относится к основным липофильным антиоксидантам [Марино П., 1998].
Методы оксигенотерапии. Кислородотерапию проводят с помощью носовых катетеров и масок, создающих определенные концентрации кислорода.
Носовые катетеры. При использовании носовых канюль или катетеров поток кислорода от 1 до 6 л/мин создает во вдыхаемом воздухе его концентрацию, равную 24—44 %. Более высокие значения FiO2 достигаются при нормальной минутной вентиляции легких (5—6 л/мин). Если минутная вентиляция превышает поток кислорода, то избыток последнего будет сбрасываться в атмосферу, а FiO2 окажется сниженной. Носовые катетеры обычно хорошо переносятся больными. Их не следует применять при высокой ЧД и гиповентиляции.
Носовые и лицевые маски. Маски снабжены клапанами, с помощью которых выдыхаемый воздух выводится в окружающую среду. Более удобны для пациента носовые маски. Последние имеют меньшее мертвое пространство и позволяют пациенту принимать пищу. Достоинством лицевых масок является их способность лучше справляться с непреднамеренной утечкой потока кислорода через рот, что является проблемой для многих больных. Они могут быть использованы даже в тех случаях, когда словесный контакт с пациентом ограничен. Оба типа масок эффективны у больных с ОДН, однако в острых ситуациях лицевые маски предпочтительнее. Лицевые маски могут быть использованы у больных с более выраженными нарушениями сознания. Стандартные лицевые маски позволяют подавать кислород до 15 л/мин и, соответственно, обеспечивать более высокую FiO2 (50—60 %). У больных с высокой минутной вентиляцией легких применение масок, как и катетеров, ограничено.
Так называемая вентимаска при потоке кислорода 4—8 л/мин обеспечивает точные концентрации кислорода во вдыхаемом воздухе: 0,24; 0,28; 0,35; 0,40. Воздух подсасывается через боковые трубки по принципу инжекции. В этих масках поддерживаются все указанные вдыхаемые фракции кислорода, и больной не испытывает неприятных ощущений.
При необходимости использования более высоких FiO2 применяют маски для дыхания по полуоткрытому контуру. Такие маски позволяют повысить FiO2 более 0,5 и даже до 1, но это не всегда удается, поскольку воздух при потоке кислорода со скоростью 12—15 л/мин подсасывается под маску во время вдоха. Если требуется длительная кислородотерапия с высокой FiO2, следует проводить интубацию трахеи. С помощью специального Т-образного переходника можно осуществить более точную дозировку FiO2 — от 0,21 до 1.
Более высокие концентрации кислорода во вдыхаемом воздухе (60 %) создаются при использовании специальных масокс частично возвратной и невозвратной масочной системой. Эти маски снабжены мешком-резервуаром. Поток кислорода 100 % концентрации обеспечивает постоянное раздувание этих мешков. В маске с частично возвратной системой имеются клапаны, позволяющие выдыхаемому воздуху свободно сбрасываться в атмосферу, однако часть выдыхаемого воздуха попадает в резервуар, и при вдохе возможно повторное вдыхание углекислого газа. В маске с невозвратной системой имеется клапан, предохраняющий мешок-резервуар от попадания в него выдыхаемого воздуха.
Экстракорпоральная мембранная оксигенация (ЭМО) показана при наиболее тяжелых формах гипоксемии, когда неэффективна обычная терапия. Доказана возможность поддержания адекватного газового состава крови при тяжелых формах ОДН. Улучшение общих результатов при ЭМО не наблюдалось.
Для оценки правильности кислородотерапии необходимо исследовать все интегральные параметры кислородно-транспортной системы: МОС и СИ, КЕК, содержание кислорода в артериальной и смешанной венозной крови, потребление кислорода.
Основные правила кислородотерапии:
• кислородотерапия показана во всех случаях артериальной гипоксемии, должна быть безопасной (т.е. проводиться с соблюдением существующих инструкций — скорость потока кислорода, увлажнение, асептика), контролируемой (пульсоксиметрия, анализы содержания газов в крови, капнография), легко управляемой;
• 100 % концентрацию кислорода применяют лишь при терминальных состояниях, апноэ, гипоксической коме, остановке сердца, отравлениях окисью углерода. По возможности не следует прибегать к использованию токсичных концентраций кислорода для достижения нормальных значенийРаО2;
• если РаО2 = 60 мм рт.ст. при ПО2, равной 0,5, не следует увеличивать FiO2;
• если выбранный метод кислородотерапии неэффективен, применяют ИВЛ, в том числе в режиме ПДКВ или постоянного положительного давления в дыхательных путях.
БРОНХОДИЛАТАТОРЫ
Бронходилататоры снижают сопротивление дыхательных путей и повышают скорость воздушного потока. Бронходилататоры при ОДН у взрослых используют при лечении астматического статуса, обострении ХОЗЛ или при повышенном сопротивлении в дыхательных путях, обусловленном бронхоспастическим состоянием.
Чтобы убедиться в правильности назначения бронхолитика, следует воспользоваться измерением пиковой скорости экспираторного потока с помощью пикфлоуметра или пикового инспираторного давления во время ИВЛ.
К бронходилататорам относятся адреномиметики, метилксантины (теофиллин) и холиноблокирующие вещества.
Адреномиметики. Эти препараты оказывают бета1- и бета2-стимулирующее действие. Чаще используют селективные агонисты бета2-адренорецепторов, не дающие кардиостимулирующего эффекта, присущего агонистам бета1-адренорецепторов.
Бета1-адренорецепторы повышают частоту и силу сердечных сокращений, в то время как бета2-адренорецепторы действуют на гладкую мускулатуру бронхов, приводя к бронходилатации. Эти препараты (тербуталин, сальбутамол, изоэтарин, орципреналин) при использовании через распылитель не вызывают тахикардии и аритмий. Селективные бета2-адреномиметики применяются для ингаляций в следующих дозах: изоэтарин - 0,5 мл 1 % раствора; орципреналина сульфат - 0,3 мл 5 % раствора; тербуталин - 0,3 мл 1 % раствора; сальбутамол — 0,1 мл 5 % раствора.
Указанные растворы смешивают с 2,5 мл изотонического раствора хлорида натрия и распыляют через небулайзер. Продолжительность действия изоэтарина 2 ч, орципреналина сульфата 3—6 ч, остальных препаратов 4—6 ч.
Во всех случаях препарат подбирают индивидуально. При возникновении после ингаляции аэрозоля тахикардии следует снизить дозу. Возможными побочными эффектами стимуляции бета2-адренорецепторов являются мышечный тремор и снижение концентрации калия в сыворотке крови. Высокие дозы могут стимулировать бета2-адренорецепторы. Препараты можно назначать и внутрь, и подкожно, но ингаляционный путь более безопасный и эффективный.
Теофиллин. Несмотря на некоторые трудности в предсказании терапевтического эффекта, этот препарат до сих пор является одним из основных средств лечения астматического статуса и ОДН, вызванной обострением ХОЗЛ. Указание на его относительно небольшой бронходилатирующии эффект очевидно правильно, но в сочетании с другими препаратами это положительное действие возрастает. Его с успехом можно комбинировать с бета-адреномиметиками, кортикостероидами. У больных с компрометированной сердечно-сосудистой системой применение бета-адреномиметиков как одного из главных компонентов бронходилатирующей терапии часто бывает невозможно. Важно соблюдать периодичность внутривенного введения препарата и контролировать концентрацию последнего в сыворотке крови.
Холиноблокирующие вещества. Бронходилатирующим эффектом обладают атропина сульфат и ипратропия бромид. Эти вещества являются м-холиноблокаторами, предупреждающими вагусные реакции. Они снимают стимуляцию парасимпатических нервов, приводящую к бронхоспазму.
Для лечения ОДН эти препараты применяют редко. Они могут быть использованы при наличии общей вагусной реакции: брадикардии, бронхореи, повышенной саливации. Атропин в форме аэрозоля может усиливать бронхолитический эффект других препаратов и применяется при тяжелом течении бронхиальной астмы, резистентном к общепринятой терапии.
Для ингаляций используют атропина сульфат из расчета 0,025— 0,075 мг/кг массы тела. Начало его действия 15-30 мин, продолжительность — 3—5 ч.
Кортикостероиды. Несмотря на то, что эффективность кортикостероидов при многих состояниях не доказана, их все же широко применяют в клинической практике (при многих острых состояниях, в том числе при ОДН различного генеза). Показаниями к назначению кортикостероидов могут быть аллергические реакции, отек гортани, аспирационный синдром, РДСВ и др. Наибольшим показанием к применению этих средств является астматический статус. Бронхиальная астма - это первичный воспалительный процесс, а не заболевание гладкой мускулатуры бронхов. Глюкокортикоиды в этих случаях блокируют продукцию провоспалительных медиаторов и уменьшают чувствительность к медиаторам, усиливающим сосудистую проницаемость (брадикинин, гистамин). Терапия кортикостероидами больных с обострением бронхиальной астмы сопровождается тенденцией к восстановлению бета-адренорецепторной чувствительности бронхов.
Наиболее эффективен бетаметазон (целестон) — 3,75 мг препарата эквивалентно по действию 30 мг преднизолона и 120 мг гидрокортизона.
