Гемостаз коагуляционный (вторичный) (свертывание крови)
Коагуляционный гемостаз: общие сведения. В процессе вторичного гемостаза (Secondary (definitive) hemostasis) на основе тромбоцитного агрегата формируется сгусток крови , который на завершающей стадии гемостаза подвергается самопроизвольному сжатию ( ретракция сгустка крови ) (см. Гемостаз: общая схема ). Таким образом, первичная или временная гемостатическая пробка , представляющая собой рыхлый тромбоцитный агрегат, превращается во вторичную или окончательную гемостатическую пробку, в которой тромбоцитный агрегат консолидируется фибрином и подвергается дополнительному уплотнению в процессе спонтанного сокращения сгустка крови. Вторичный или окончательный гемостаз обеспечивает полную остановку кровотечения из вен, артериол и артерий. Коагуляционный (вторичный) гемостаз, или свертывание крови, протекает в течение нескольких минут и представляет собой каскад реакций между плазменными белками , заканчивающийся образованием нитей фибрина . Благодаря этому останавливается кровотечение из крупных сосудов и предотвращается их возобновление через несколько часов или суток. Одновременно с образованием тромбоцитарного тромба активируются факторы свертывания и запускается коагуляционный гемостаз . Гемостатические реакции, совокупность которых принято называть плазменным(коагуляционным) гемостазом и итогом которых является образование фибрина, обеспечиваются протеинами, носящими название плазменных факторов. Процесс протекания плазменного гемостаза можно условно разделить на три фазы.
Первая фаза - протромбиназообразование, или контактно-калликреин-кинин-каскадная активация. Первая фаза представляет собой многоступенчатый процесс, в результате которого в крови накапливается комплекс факторов, способных превратить протромбин в тромбин, поэтому комплекс называется протромбиназой. В зависимости от пути формирования протромбиназы различают внутренний и внешний пути ее формирования. По внутреннему пути свертывание крови инициируется без участия тканевого тромбопластина; в образовании протромбиназы принимают участие факторы плазмы (XII, XI, IX, VIII, X), калликреин-кининовая система и тромбоциты. В результате инициации реакций внутреннего пути образуется комплекс факторов Ха с V на фосфолипидной поверхности (3-й фактор тромбоцитов) в присутствии ионизированного кальция. Весь этот комплекс действует как протромбиназа, превращая протромбин в тромбин. Пусковым фактором этого механизма является фактор XII, который активируется либо вследствие контакта крови с чужеродной поверхностью, либо при контакте крови с субэндотелием (коллагеном) и другими компонентами соединительной ткани при повреждении стенок сосудов, либо фактор XII активируется путем его ферментативного расщепления (калликреином, плазмином, другими протеазами). Во внешнем пути формирования протромбиназы основную роль играет тканевый фактор (фактор III), который экспрессируется на клеточных поверхностях при повреждении тканей и образует с фактором VIIa и ионами кальция комплекс, способный перевести фактор X в фактор Ха, который и активирует протромбин. Кроме того, фактор Ха ретроградно активирует комплекс тканевого фактора + фактора VIIa. Таким образом, внутренний и внешний пути соединяются на факторах свертывания. Однако так называемые «мосты» между этими путями реализуются через взаимную активацию факторов XII, VII и IX. Эта фаза длится от 4 мин 50 с до 6 мин 50 с.
Вторая фаза - тромбинообразование. В эту фазу протромбиназа вместе с факторами коагуляции V, VII, X и IV переводит неактивный фактор II (протромбин) в активный фактор IIа - тромбин. Эта фаза длится 2 - 5 с.
Третья фаза свертывания крови - фибринообразование. Возникший тромбин отщепляет от молекулы фибриногена два пептида А и два В, переводит его в фибрин-мономер. Молекулы последнего полимеризуются сначала в димеры, затем в еще растворимые, особенно в кислой среде, олигомеры, и фибрин-папилляры становятся фибрин-полимером. Кроме того, тромбин способствует превращению фактора XIII в фактор ХIIIа. Последний в присутствии Са2+ изменяет фибрин-полимер из лабильной, легко растворимой фибринолизином (плазмином) формы в медленно и ограниченно растворимую форму, составляющую основу кровяного сгустка. Эта фаза длится 2 - 5 с.
Факторы плазмы крови
Фактор I(фибриноген) – важнейший компонент свертывающей системы
крови, так как биологической сущностью процесса свертывания крови
является образование фибрина из фибриногена. Фибриноген состоит из
3 пар неидентичных полипептидных цепей, которые связаны между собой
дисульфидными связями. Каждая цепь имеет олигосахаридную группу.Фактор II(протромбин) является одним из основных белков плазмы крови, определяющих свертывание крови. При гидролитическом расщепле- нии протромбина образуется активный фермент свертывания крови – тромбин. Фактор III(тканевый фактор, или тканевый тромбопластин) образуется
при повреждении тканей. Это комплексное соединение липопротеиновой природы.Фактор IV(ионы Са2+). Известно, что удаление из крови ионов Са2+
(осаждение оксалатом или фторидом натрия), а также перевод ионов Са2+
в неионизированное состояние (с помощью цитрата натрия) предупреждаетсвертывание крови. Следует также помнить, что нормальная скорость свертывания крови обеспечивается лишь оптимальными концентрациями ионов Са2+.Фактор V(проакцелерин) относится к глобулиновой фракции плазмы крови. Он является предшественником акцелерина (активного фактора). Фактор V синтезируется в печени, поэтому при поражении этого органа
может возникнуть недостаточность проакцелерина. Кроме того, существует
врожденная недостаточность в крови фактора V, которая носит название
парагемофилии и представляет собой одну из разновидностей геморрагических диатезов. Фактор VII(антифибринолизин, проконвертин) – предшественник кон-
вертина. Механизм образования активного конвертина из проконвертина изучен мало. Биологическая роль фактора VII сводится прежде всего к участию во внешнем пути свертывания крови.
Мигофибрилы.
В каждом мышечном волокне в полужидкой саркоплазме по длине волокна расположено, нередко в форме пучков, множество нитевидных образований – миофибрилл (толщина их обычно менее 1 мкм), обладаю-
щих, как и все волокно в целом, поперечной исчерченностью. Поперечная исчерченность волокна, зависящая от оптической неоднородности белковых веществ, локализованных во всех миофибриллах на одном уровне, легко выявляется при исследовании волокон скелетных мышц в поляризационном или фазово-контрастном микроскопе. Повторяющимся элементом поперечно-полосатой миофибриллы явля-
ется саркомер – участок миофибриллы, границами которого служат узкие Z-линии. Каждая миофибрилла состоит из нескольких сот саркомеров. Средняя длина саркомера 2,5–3,0 мкм. В середине саркомера находится зона протяженностью 1,5–1,6 мкм, темная в фазово-контрастном микроскопе. В поляризованном свете она дает сильное двойное лучепреломление. Эту зону принято называть диском А (анизотропный диск). В центре диска А расположена линия М, которую можно наблюдать только в электронном микроскопе. Среднюю часть диска А занимает зона Н более слабого
двойного лучепреломления. Наконец, существуют изотропные диски, или диски I, с очень слабым двойным лучепреломлением. В фазово-контрастном микроскопе они кажутся более светлыми, чем диски А. Длина дисковI около 1 мкм. Каждый из них разделен на две равные половины Z-мембраной, или Z-линией.К группе миофибриллярных белков
Миозин составляет 50–55% от сухой массы миофибрилл. две тяжелые полипептидные цепи с мол. массой 205000–210000 и несколько коротких легких цепей, мол. масса которых около 20000. Тяжелые цепи образуют длинную закрученную α-спираль (≪хвост≫ молекулы), конец каждой тяжелой цепи совместно с легкими цепями создает глобулу (≪головка≫ молекулы), способную соединяться с актином. Эти ≪головки≫ выдаются из основного стержня молекулы. Легкие цепи, находящиеся в ≪головке≫ миозиновой молекулы и принимающие участие в проявлении АТФазной активности
миозина, гетерогенны по своему составу. Количество легких цепей в молекуле миозина у различных видов животных и в разных типах мышц неодинаково. Актомиозин образуется при соединении миозина с F-актином. Актомиозин, как естественный, так и искусственный, т.е. полученный путем соединения in vitro высокоочищенных препаратов миозина и F-актина, обладает АТФазной активностью, которая отличается от таковой миозина,
АТФазная активность миозина значительно возрастает в присутствии стехиометрических количеств F-актина. Фермент актомиозин активируется ионами Mg2+ и ингибируется этилендиаминтетраацетатом (ЭДТА) и вы-
сокой концентрацией АТФ, тогда как миозиновая АТФаза ингибируется
ионами Mg2+, активируется ЭДТА и не ингибируется высокой концентрацией АТФ. Оптимальные значения рН для обоих ферментов также различны. Как отмечалось, кроме рассмотренных основных белков, в миофибриллах содержатся также тропомиозин, тропонин и некоторые другие регуляторные белки. Тропомиозин был открыт К. Бейли в 1946 г. Молекула тропомиозина состоит из двух α-спиралей и имеет вид стержня длиной 40 нм; его мол.
масса 65000. На долю тропомиозина риходится около 4–7% всех белков
миофибрилл. Тропонин – глобулярный белок, открытый С. Эбаси в 1963 г.; его мол.
масса 80000. В скелетных мышцах взрослых животных и человека тропонин (Тн) составляет лишь около 2% от всех миофибриллярных белков. В его состав входят три субъединицы (Тн-I, Тн-С, Тн-Т). Тн-I (ингибирующий) может ингибировать АТФазную активность, ТН-С (кальцийсвязывающий) обладает значительным сродством к ионам кальция, Тн-Т (тропомиозин-связывающий) обеспечивает связь с тропомиозином. Тропонин, соединяясь с тропомиозином, образует комплекс, названный нативным тропомиозином. Этот комплекс прикрепляется к актиновым филаментам и придает актомиозину скелетных мышц позвоночных чувствительность к ионам
Са2+.
Сокращение- Однако основной функцией мышц является осуществление
двигательного акта, т.е. сокращение и расслабление. При сокращениимышц осуществляется работа, связанная с превращением химической энергии в механическую. В данном разделе в основном рассматривается структурная основа процесса сокращения поперечно-полосатых мышц позвоночных, поскольку этот процесс изучен наиболее полно. Как отмечалось, сократительная система поперечно полосатой мышцы состоит из
перекрывающихся белковых нитей, которые скользят относительно друг друга. Сокращение происходит за счет энергии, освобождающейся при гидролизе АТФ. В поперечно-полосатой мышце сокращение зависит от концентрации ионов Са2+, которая в свою очередь регулируется саркоплазматическим ретикулумом – специализированной системой мембран,
накапливающей Са2+ в состоянии покоя и высвобожающей его при воздействии на мышечное волокно нервного импульса.Источники энергии мышечной деятельности
Принято считать, что процессом, непосредственно связанным с работающим механизмом поперечно-полосатого мышечного волокна, является распад АТФ с образованием АДФ и неорганического фосфата. Возникает вопрос: каким образом мышечная клетка может обеспечить свой сократительный аппарат достаточным количеством энергии в форме АТФ. Креатинкиназный путь ресинтеза АТФ является чрезвычайно быстрым и максимально эффективным (за счет каждой молекулы креатинфосфата образуется молекула АТФ). Именно поэтому долгое время не удавалось установить уменьшение концентрации АТФ и соответственно повышение концентрации АДФ даже при достаточно продолжительном тетанусе.
Соединительная ткань составляет примерно 50% от массы тела. Рыхлая
соединительная ткань подкожной клетчатки, компактная кость и зубы,
сухожилия и межмышечные фасциальные прослойки, кожа и внутриорган-
ная строма паренхиматозных органов, нейроглия и брюшина – все это
соединительная ткань.Коллаген
Характерным компонентом структуры соединительной ткани являются
коллагеновые волокна. Они построены в основном из своеобразногобелкаи – коллагена. Коллаген составляет 25–33% от общего количества
белка организма взрослого человека, или 6% от массы тела.
Видимые в оптическом микроскопе коллагеновые волокна состоят из
различимых в электронном микроскопе фибрилл – вытянутых в длину
белковых молекул, названных тропоколлагеном. Тропоколлаген – ос-
новная структурная единица коллагена. Молекула тропоколлагена – это белок коллаген. Одной из отличительных черт данного белка является то, что 1/3 всех его аминокислотных остатков составляет глицин,
1/3 – пролин и 4-гидроксипролин, около 1% – гидроксилизин; некоторые молекулярные формы коллагена содержат также 3-гидроксипролин, хотя и в весьма ограниченном количестве:
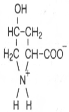
4-Гидроксипролин
Эластин
Эластин – основной белковый компонент, из которого состоят эластические волокна. Он отличается от коллагена по химическому составу и молекулярной структуре. Общими для эластина и коллагена являются большое содержание глицина и пролина, наличие оксипролина, хотя последнего в эластине примерно в 10 раз меньше, чем в коллагене.
При ферментативном гидролизе эластина в гидролизате обнаруживаются десмозин и изодесмозин. Эти соединения содержатся только в эластине. Структура их довольно необычна: 4 остатка лизина, соединяясь своими радикалами, образуют замещенное пиридиновое кольцо. Считают, что при образовании десмозина сначала 3 остатка лизина окисляются до соответствующих ε-альдегидов, а затем происходит их соединение с четвертым остатком лизина. Очевидно, именно благодаря своей структуре десмозин и изодесмозин
могут одновременно входить в состав четырех пептидных цепей. По-ви-
димому, этим можно объяснить, что эластин в отличие от других фибриллярных белков способен растягиваться в двух направлениях
Химический состав не
Характерной структурной основой нервной клетки является базофильное вещество (субстанция Ниссля), состоящее из рибонуклеиновых кислот и белков. В цитоплазме также выявляется сеть тонких нитей – нейрофибрилл, которые в совокупности образуют густую сеть. Нейрофибриллы – это структурное выражение правильной линейной
ориентации белковых молекул. Важный компонент цитоплазмы нейрона –пластинчатый комплекс (аппарат Гольджи), где сосредоточены главным образом липидные компоненты клетки. Одной из особенностей митохондрий, изолированных из нервных клеток, является то, что они содержат меньше ферментов, участвующих в процессах окисления жирных кислот и аминокислот, чем митохондрии из других тканей. Миелиновое вещество – понятие морфологическое. По сути миелин – это система, образованная многократно наслаивающимися мембранами клеток нейроглии * вокруг нервных отростков (в периферических нервных стволах нейроглия представлена леммоцитами, или шванновскими клетками, а в белом веществе ЦНС – астроцитами). По химическому составу миелиновое вещество является сложным белково-липидным комплексом.
На долю липидов приходится до 80% плотного осадка; 90% всех липидов миелина представлено холестерином, фосфолипидами и цереброзидами. Считают, что в липоидных слоях миелиновых оболочек молекулы различных липидов имеют строго определенное расположение.ХИМИЧЕСКИЙ СОСТАВ МОЗГА. Белки
На долю белков приходится примерно 40% от сухой массы головного мозга.нейроальбуминамии нейроглобулинами. Количество нейроглобулинов в головном мозге относительно велико – в среднем 5% по отношению ко всем растворимым белкам. Нейроальбумины являются основным белковым компонентом фосфопротеинов нервной ткани, на их долю приходится основная масса растворимых белков (89–90%).Нейросклеропротеиныможно охарактеризовать как структурно-опорные
белки. Основные представители этих белков – нейроколлагены, нейроэластины, нейростромины и др. Они составляют примерно 8–10% от общего количества простых белков нервной ткани и локализованы в основном в белом веществе головного мозга и в периферической нервной системе.ЛипидыСреди химических компонентов головного мозга особое место занимаютлипиды, высокое содержание и специфическая природа которых придают
мозговой ткани характерные особенности. В группу липидов головного мозга входят фосфоглицериды, холестерин, сфингомиелины, цереброзиды,ганглиозиды и очень небольшое количество нейтрального жира
УглеводыВ мозговой ткани имеются гликоген и глюкоза, но по сравнению с другимитканями ткань мозга бедна углеводами.Интенсивность обновления богатых энергией фосфорных соединений в головном мозге очень велика. Именно этим можно объяснить, что содержание АТФ и креатинфосфата в мозговой ткани характеризуется значительным постоянством. В случае прекращения доступа кислорода мозг может
≪просуществовать≫ немногим более минуты за счет резерва лабильных
фосфатов. Прекращение доступа кислорода даже на 10–15 с нарушает энергетику нервных клеток, что в целостном организме выражается наступлением обморочного состояния. По-видимому, при кислородном голодании мозг может очень недолго получать энергию за счет процессов
гликолиза.
Глюкоза. Основным субстратом дыхания мозговой ткани является глюкоза. В 1 мин
100 г ткани мозга потребляют в среднем 5 мг глюкозы. Подсчитано, что более 90% утилизируемой глюкозы в ткани мозга окисляется до СО2 и Н2О при участии цикла трикарбоновых кислот. В физиологических условиях роль пентозофосфатного пути окисления глюкозы в мозговой ткани не-
велика, однако этот путь окисления глюкозы присущ всем клеткам головного мозга. Образующаяся в процессе пентозофосфатного цикла восстановленная форма НАДФ (НАДФН) используется для синтеза жирных кислот и стероидов. Интересно отметить, что в расчете на всю массу головного мозга содержание глюкозы в нем составляет около 750 мг. За 1 мин тканью мозга окисляется 75 мг глюкозы. Следовательно, количество глюкозы, имеющееся в ткани головного мозга, могло бы быть достаточным лишь на 10 мин жизни человека. Между глюкозой и гликогеном мозговой ткани имеется тесная связь,
выражающаяся в том, что при недостаточном поступлении глюкозы из
крови гликоген головного мозга является источником глюкозы, а глюкоза при ее избытке – исходным материалом для синтеза гликогена. Распад гликогена в мозговой ткани происходит путем фосфоролиза с участием системы цАМФ. Однако в целом использование гликогена в мозге по сравнению с глюкозой не играет существенной роли в энергетическом
отношении, так как содержание гликогена в головном мозге невелико.
Детоксикация функция печени
Чужеродные вещества (ксенобиотики) в печени нередко превращаются
в менее токсичные и даже индифферентные вещества. По-видимому, только
в этом смысле можно говорить об ≪обезвреживании≫ их в печени. Происхо-
дит это путем окисления, восстановления, метилирования, ацетилирования
и конъюгации с теми или иными веществами. Необходимо отметить, что
в печени окисление, восстановление и гидролиз чужеродных соединений
осуществляют в основном микросомальные ферменты. Наряду с микро-
сомальным в печени существует также пероксисомальное окисление.
Пероксисомы – микротельца, обнаруженные в гепатоцитах; их можно рас-
сматривать как специализированные окислительные органеллы. Эти
микротельца содержат оксидазу мочевой кислоты, лактатоксидазу, окси-
дазу D-аминокислот, а также каталазу. Последняя катализирует расщеп-
ление перекиси водорода, которая образуется при действии указанных оксидаз. В печени широко представлены также ≪защитные≫ синтезы, например синтез мочевины, в результате которого обезвреживается весьма токсичный аммиак. В результате гнилостных процессов, протекающих в кишечнике, из тирозина образуются фенол и крезол, а из триптофона – скатол и индол. Эти вещества всасываются и с током крови поступают в печень, где
обезвреживаются путем образования парных соединений с серной или глюкуроновой кислотой. Обезвреживание фенола, крезола, скатола и индола в печени происходит
в результате взаимодействия этих соединений не со свободными серной
и глюкуроновой кислотами. Глюкуроновая кислота участвует не только в обезвреживании продуктов гниения белковых веществ, образовавшихся в кишечнике, но и в связывании ряда других токсичных соединений, образующихся в процессе обмена в тканях. В частности, свободный, или непрямой, билирубин, обладающий значительной токсичностью, в печени взаимодействует с глюкуроновой
кислотой, образуя моно- и диглюкурониды билирубина. Нормальным метаболитом является и гиппуровая кислота, образующаяся в печени из бензойной кислоты и глицина. Примером обезвреживания токсичных продуктов в печени путем восстановления является превращение нитробензола в парааминофенол. Многие ароматические углеводы обезвреживаются путем окисления с образованием соответствующих карбоновых кислот. Печень принимает активное участие в инактивации различных гормонов. С током крови гормоны попадают в печень, при этом активность их в большинстве случаев резко снижается или полностью утрачивается. Так, стероидные гормоны, подвергаясь микросомальному окислению, инактивируются, превращаясь затем в соответствующие глюкурониды и сульфаты. Под влиянием аминооксидаз в печени происходит окисление катехоламинов и т.д.
Роль почек. Почки оказывают значительное влияние на кислотно-основное равновесие,
но оно сказывается по истечении значительно большего времени, чем влияние буферных систем крови и легких. .почкам необходимо около 10–20 ч для восстановления нарушенного
кислотно-основного равновесия. Основным механизмом поддержания концентрации водородных ионов в организме, реализуемым в клетках почечных канальцев, являются процессы реабсорбции натрия и секреции ионов водорода. Этот механизм осуществляется с помощью нескольких химических процессов. Первый из них –
реабсорбция натрия при превращении двузамещенных фосфатов в однозамещенные. Почечный фильтрат, формирующийся в клубочках, содержит
достаточное количество солей, в том числе и фосфатов. Однако концентрация двузамещенных фосфатов постепенно убывает по мере продвижения первичной мочи по почечным канальцам. Так, в крови отношение однозамещенного фосфата к двузамещенному составляет 1:4, в клубочковом фильтрате – 9:1, в моче, которая проходит через дистальный сегмент нефрона,50:1. Это объясняется избирательным всасыванием канальцевыми клетками ионов натрия. Вместо них из канальцевых клеток в просвет почечного
канальца выделяются ионы водорода. Таким образом, двузамещенный фосфат Na2HPO4 превращается в однозамещенный NaH2PO4 и в таком виде выделяется с мочой. В клетках канальцев из угольной кислоты
образуется бикарбонат, увеличивая тем самым щелочной резерв крови. Второй химический процесс, который обеспечивает задержку натрия в организме и выведение излишка водородных ионов,– это превращение в просвете канальцев бикарбонатов в угольную кислоту. В клетках канальцев при взаимодействии воды с углекислым газом под влиянием карбоан-
гидразы образуется угольная кислота. Водородные ионы угольной кислоты
выделяются в просвет канальца и соединяются там с анионами бикарбоната; эквивалентный этим анионам натрий поступает в клетки почечных канальцев. Образовавшаяся в просвете канальца Н2СО3 легко распадается на СО2 и Н2О и в таком виде покидает организм.
Третьим процессом, который также способствует сохранению натрия в организме, является образование в почках аммиака, который используется вместо других катионов для нейтрализации и выведения кислых эквивалентов с мочой. Основным источником этого служат процессы дезаминирования глутамина, а также окислительного дезаминирования аминокислот,главным образом глутаминовой кислоты.
