Е.г. доркина, н.в. постникова
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ПЯТИГОРСКАЯ ГОСУДАРСТВЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАФЕДРА БИОЛОГИЧЕСКОЙ ХИМИИ И МИКРОБИОЛОГИИ
Е.Г. ДОРКИНА, Н.В. ПОСТНИКОВА
ИНФЕКЦИЯ И ИММУНИТЕТ
Методические указания для самостоятельной внеаудиторной работы студентов очной формы обучения по дисциплине
С2.Б.12 – МИКРОБИОЛОГИЯ
Пятигорск 2012
УДК 576. 8. 097 (076.5)
ББК 52.6 я 73
Д 68
Рецензент: зав.каф. биологии и физиологии Л.Е. Назарова
Е.Г. Доркина, Н.В. Постникова
Д 68 Инфекция и иммунитет: методические указания для самостоятельной внеаудиторной работы студентов заочной формы обучения по дисциплине С2.Б.12 – МИКРОБИОЛОГИЯ/ Е.Г. Доркина, Н.В. Постникова. – Пятигорск: Пятигорская ГФА. 2012. – 38 с.
Методические указания для самостоятельной внеаудиторной работы студентов по микробиологии «Инфекция и иммунитет» составлены в соответствии с Примерной программой по микробиологии, утвержденной в соответствии с ФГОСТ-3 ВПО для студентов заочной формы обучения. В указаниях содержатся основные сведения об инфекции, современные понятия об иммунитете, видах иммунитета, видах иммунного ответа, иммунологическом статусе организма. Доступная форма изложения материала поможет студентам в усвоении материала, написании вопросов контрольной работы и решению задач и упражнений по данному разделу.
УДК 576. 8. 097 (076.5)
ББК 52.6 я 73
Допущено к внутривузовскому изданию
Председатель ЭМС
проф. _____________________ В.В. Гацан
Протокол № 513 от « 13 » марта 2012 г.
Ó Пятигорская государственная фармацевтическая академия, 2012
Содержание
1. Понятия «инфекция», «инфекционный процесс», «инфекционная болезнь»………………………...……………………………………….4
2. Возбудители инфекции и их свойства...………...............................4
3. Характеристика стадий развития инфекционного процесса и факторов вирулентности…...…………………………………………..6
4. Свойства бактериальных токсинов и их получение………...……….7
5. Понятия инфицирующей дозы и входных ворот инфекции.….…..11
6. Динамика развития инфекционной болезни………………………..11
7. Формы инфекционного процесса…………………………………….12
8. Характеристика основных элементов эпидемического процесса………………………………………………………...……...14
9. Понятия об иммунитете, виды иммунитета………………………...16
10. Функции иммунной системы и общая характеристика её центральных и периферических органов……………………………18
11. Т- и В-лимфоциты и их субпопуляции……………………..………20
12. Факторы и механизмы неспецифической противоинфекционной защиты организма………………………………………………..……21
13. Антигены и их свойства……………………………………………...26
14. Антигены микроорганизмов…………………………………………28
15. Антитела и их свойства……………………………………………....30
16. Классы иммуноглобулинов…………………………………………..31
17. Динамика накопления антител при первичном и вторичном иммунном ответе………………………………………………………33
18. Характеристика гуморального и клеточного иммунного ответа….33
19. Понятие иммунологической памяти и иммунологической толерантности………………………………………………………….36
20. Понятие иммунного статуса организма…………………………….37
1. ПОНЯТИЯ "ИНФЕКЦИЯ", "ИНФЕКЦИОННЫЙ ПРОЦЕСС", "ИНФЕКЦИОННАЯ БОЛЕЗНЬ".
Инфекция (лат. infectio - заражение) - проникновение микроорганизма в макроорганизм и его размножение в нем, в результате чего возникает инфекционный процесс.
Инфекционный процесс - это совокупность физиологических и патологических реакций, происходящих в макроорганизме при внедрении в него патогенных микроорганизмов, и вызывающих нарушение его внутренней среды и физиологических функций.
Инфекционный процесс в зависимости от свойств возбудителя и формы его воздействия может иметь различные проявления: от бессимптомного носительства до тяжелейших форм с летальным исходом.
Инфекционная болезнь - ярко выраженная форма проявления инфекционного процесса, характеризующаяся наличием определенного возбудителя, инкубационного периода, специфичных для данной болезни симптомов и иммунного ответа.
В отличие от других заболеваний инфекционные болезни могут передаваться от зараженных человека или животного здоровому (контагиозность) и способны к массовому (эпидемическому) распространению.
С биологической точки зрения инфекционный процесс представляется разновидностью паразитизма - формы отношения между двумя организмами разных видов, из которых один, называемый паразитом, использует другого, именуемого хозяином, как источник питания и место постоянного или временного обитания. К паразитам относятся все возбудители инфекционных болезней человека.
Название болезни формируется от названия возбудителя (вида, рода или семейства) добавлением суффиксов -оз или -аз. Например, сальмонелла - сальмонеллез, риккетсия- риккетсиоз, амеба- амебиаз.
Экзотоксины
Белковые токсины образуются различными видами микроорганизмов: дифтерийной и столбнячной палочками, возбудителями газовой гангрены, ботулизма, стафилококками, стрептококками, некоторыми видами дизентерийных микробов, кишечной палочкой, холерным вибрионом и другими микроорганизмами. Это белки с разной молекулярной массой простой или сложной структуры.
Независимо от сложности строения токсины имеют два центра. Один из них фиксирует молекулу токсина на соответствующем клеточном рецепторе, второй - токсический фрагмент - проникает внутрь клетки, где блокирует жизненно важные метаболические реакции.
Будучи белками, экзотоксины, как правило, термолабильны (разрушаются при t 60°С). Дифтерийный токсин разрушается при t 60°С в течение часа, столбнячный - в течение 20 минут. Но имеются и термостабильные токсины, которые могут переносить кратковременное кипячение. Это токсины возбудителя ботулизма, стафилококка, холерного вибриона, кишечной палочки.
Белковые токсины малоустойчивы и к действию света, кислорода, кислот и щелочей.
Экзотоксины обладают избирательным действием на отдельные органы и ткани организма. Специфичность токсического действия определяется избирательной фиксацией токсина на рецепторах клеток-мишеней определенных тканей (эпителиальной, нервной и др.) организма человека и животных. Дифтерийный токсин вызывает некроз в месте введения, повреждает надпочечники и мышцу сердца; столбнячный токсин воздействует на двигательные нервные клетки.
При парентеральном введении белковых токсинов они вызывают образование специфических веществ (антител), способных нейтрализовать эти токсины, т.е. они обладают хорошо выраженной антигенностью.
Одни токсины (дифтерийный, столбнячный, анаэробной инфекции) разрушаются под действием пищеварительных ферментов, вследствие чего они являются безвредными при введении их через рот; другие (ботулинический, патогенных стафилококков) не разрушаются в желудке и кишечнике и вызывают отравление при пероральном введении.
Экзотоксины характеризуются высокой токсичностью, действуют на восприимчивый организм в малых дозах. Высокую токсичность белковых токсинов можно объяснить особенностью строения участков их молекул, имитирующих структуры субъединиц гормонов, ферментов, нейромедиаторов макроорганизма. Это делает их антиметаболитами вышеупомянутых жизненно важных соединений, блокирующих функциональную активность последних.
Силу действия токсинов оценивают в тех же единицах, в которых оценивают вирулентность - DLM и LD50.
Белковые токсины под действием формалина утрачивают свою ядовитость, сохраняя при этом иммуногенные свойства. Такие токсины получили название анатоксинов. Анатоксины получают воздействием на белковые токсины 0,4% раствором формалина в течение 3-4 недель при температуре 39-40°С. Они применяются в качестве вакцин для специфической профилактики токсинемических инфекций.
По механизму действия белковые токсины делятся на 4 группы:
1. Цитотоксины - блокируют синтез белка на субклеточном уровне. Например, дифтерийный гистотоксин полностью выводит из строя фермент трансферазу II, ответственную за элонгацию (удлинение) полипептидной цепи на рибосоме.
2. Мембранотоксины - повышают проницаемость поверхностной мембраны эритроцитов (гемолизины) и лейкоцитов (лейкоцидины), вызывая гемолиз первых и разрушение вторых.
3. Функциональные блокаторы – токсины, блокирующие функции определенных тканевых систем. Энтеротоксины (холероген и др.) активируют фермент аденилатциклазу, что приводит к повышению проницаемости стенки тонкой кишки и повышению выхода жидкости в ее просвет, т.е. диарее. Нейротоксины (тетаноспазмин столбнячной палочки и др.) блокируют передачу нервных импульсов в клетках спинного мозга.
4. Эксфолиатины и эритрогенины, образуемые некоторыми штаммами золотистого стафилококка и скарлатинозным стрептококком, влияют на процесс взаимодействия клеток между собой и с межклеточными веществами. Многие бактерии образуют не один, а несколько белковых токсинов, которые обладают разным действием: летальным, дермонекротическим, цитотоксическим, нейро-токсическим, гемолитическим.
Получение экзотоксинов включает два основных этапа. Первый этап - выращивание микроорганизма, продуцирующего экзотоксин, в жидкой питательной среде. На втором этапе культуральную жидкость очищают от микробных клеток различными способами:
- фильтрованием через бактериальные фильтры;
- коагуляцией в изоэлектрической точке;
- многократным переосаждением трихлоруксусной кислоты при низкой температуре и рН 4,0;
- высаливанием сульфатом аммония;
- адсорбцией различными веществами.
Эндотоксины
Патогенные грамотрицательные бактерии (возбудители брюшного тифа, паратифов, гонореи, туляремии, бруцеллеза и др.) не продуцируют экзотоксины, они содержат эндотоксины.
Эндотоксины - это липополисахариды (ЛПС) клеточной стенки.
Эндотоксины в отличие от токсинов белковой природы (экзотоксинов) более устойчивы к повышенной температуре (термостабильны): выдерживают кипячение и автоклавирование при 120˚С в течение 30 минут. Под влиянием формалина они не переходят в анатоксины.
Действие эндотоксинов на организм не отличается специфичностью. Независимо от того, из какого микроба получен эндотоксин, клиническая картина, вызываемая им, однотипна и характеризуется угнетением фагоцитоза, одышкой, диареей, падением сердечной деятельности, понижением температуры тела, слабостью. Малые дозы эндотоксина могут вызвать обратный эффект: стимуляция фагоцитоза, повышение температуры тела, менее выраженный токсикоз.
ЛПС - сравнительно слабые антигены. Сыворотка крови животных, иммунизированных чистым эндотоксином, не обладает высокой антитоксической активностью и не способна полностью нейтрализовать его ядовитые свойства.
Для получения эндотоксинов пользуются различными методами, в основу которых положено разрушение микробной клетки. Т.к. эндотоксин является липополисахаридным комплексом клеточной стенки грамотрицательных бактерий, он может быть извлечен из микробной клетки путем разрушения ее трихлоруксусной кислотой с последующим диализом, при котором используются полупроницаемые мембраны, задерживающие высокомолекулярные вещества (белки) и пропускающие низкомолекуляр-ные (в т.ч. и липополисахариды). Данный комплекс определяет антигенные свойства эндотоксина и получил название «полный антиген».
Некоторые бактерии одновременно образуют как белковые токсины, так и эндотоксины, например, кишечная палочка, холерный вибрион и другие.
Популяции Т-лимфоцитов.
Т-лимфоциты имеют антигенраспознающий рецептор – TCR (Т-клеточный рецептор). Формирование TCR происходит аналогично формированию антител (рекомбинация генов).
Т-лимфоциты делятся на две группы:
1) Т-лимфоциты, распознающие антигены, представляемые при участии MHC;
2) Т-лимфоциты, распознающие антигены, представляемые другими «неклассическими» молекулами (т.е. не MHC): например, СD1, или распознающие свободные антигены (без представления АПК). Они располагаются в слизистых оболочках и коже, заселяя эпидермис в виде межэпителиальных клеток.
Т-лимфоциты 1-ой группы по своим корецепторам (дополнительным рецепторам) делятся на:
- Т-хелперы (ТH): корецептор - СД4- распознают комплекс: антиген - MHC II класса антигенпрезентирующих клеток (АПК).
- Цитотоксические Т-лимфоциты (ЦТЛ): корецептор СД8 - распознают комплекс: антиген - MHC I класса АПК или клеток-мишеней.
Т-хелперы бывают 3 видов.
После распознавания антигена нулевые (наивные) Т-хелперы ТH0 под влиянием различных сигналов дифференцируются на:
- ТH1-хелперы – отвечают за стимуляцию клеточного иммунитета; участвуют в иммунном воспалении по типу ГЗТ, активируя макрофаги; продуцируют ТH1-цитокины (ИЛ-2, γ-интерферон, TNF-b). ТH1-ответ стимулируют внутриклеточные возбудители (вирусы, микобактерии, некоторые грибы и патогенные простейшие.
- ТH2-хелперы- отвечают за развитие гуморального иммунитета, стимулируя антителообразование; продуцируют ТH2-цитокины (ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10, ИЛ-13). ТH2-ответ стимулируют внеклеточные бактерии и паразиты.
- ТH3-хелперы -регуляторные Т-лимфоциты, могут угнетать ТH1 и ТH2.
ТH1 и ТH2 оказывают друг на друга супрессирующее действие. ТH1 угнетает ТH2 , продуцируя γ-интерферон, а ТH2 угнетает ТH1, продуцируя ИЛ-10.
ЦТЛ при помощи TCR и корецептора СД8 распознают комплекс антиген - MHC I класса. Распознавание усиливается дополнительным сигналом в виде ИЛ-2 от ТH1, что вызывает пролиферацию ЦТЛ с образование антигенспецифического клона, обладающего прямой цитотоксичностью: уничтожают клетки-мишени без участия антител и комплемента при помощи выделяемых ими цитотоксических белков. ЦТЛ выбрасывают из гранул эти белки (перфорины, гранулизины, гранзимы), которые, встраиваясь в мембрану клетки-мишени, образуют поры, способствующие проникновению гранзимов, которые запускают апоптоз клетки-мишени. После уничтожения одной клетки-мишени ЦТЛ способны разрушать и другие клетки-мишени (серийные убийцы). Ранее ЦТЛ называли Т-киллерами. Но оказалось, что и другие клетки способны уничтожать клетки-мишени (ТH1, возможно около 10% ЦТЛ).
Регуляторные Т-лимфоциты –играют важную роль в негативной регуляции иммунного ответа; выделяют цитокины, блокирующие иммунокомпетентные клетки. Они сильнее действуют на субпопуляции Т-хелперов с повышенной функцией, регулируя баланс ТH1/ТH2.
Т-лимфоциты памяти –долгоживущие потомки Т-лимфоцитов, сохраняющие рецепторы к антигенам ("память" об антигене) и организующие более быстрый и сильный клеточный иммунный ответ при повторном попадании антигена в организм.
Популяции В-лимфоцитов.
Существуют В1 (СД5+) и В2 (СД5-)-популяции В-лимфоцитов.
В-лимфоциты(В1 (СD5+) и В2 (СD5-)-популяции)- участвуют в образовании антител (гуморальном иммунитете). Антитела, связанные с мембраной В-лимфоцита, являются маркерами В-лимфоцитов.
В1 (СД5+) - популяция В-лимфоцитов находится только в брюшной и плевральной полостях, секретируя IgM- антитела и участвуя в антибактериальной иммунитете. Они взаимодействуют с Т-лимфоцитами через свои СД1 молекулы.
В2 (СD5-) - популяция– главная популяция В-лимфоцитов. Встречая антиген, они исполняют роль антигенпрезентирующей клетки (АПК), представляя антиген хелперу ТH2 с помощью MHC II класса. После преобразований В-лимфоциты дифференцируются в плазматические клетки (плазмоциты), синтезирующие и секретирующие антитела одной специфичности (IgM, IgG, IgA, IgE, IgD). Пролиферация В-лимфоцитов усиливается ИЛ-2. ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10, продуцируемые ТH2, участвуют в переключении синтеза различных классов Ig.
В-лимфоциты памяти – долгоживущие клетки, несущие на своей мембране IgG и IgA, в отличие от обычных, несущих IgM или IgM/IgD. Стимулированные антигеном, они быстро достигают красного костного мозга, где превращаются в антителообразующие плазмоциты.
Фагоцитоз
Неиммунный: Иммунный
(неспецифический, (фактор специфического иммунитета)
фактор видового иммунитета)
Завершенный, незавершенный
Завершенный фагоцитоз заканчивается полным перевариванием микроба. При незавершенном фагоцитозе микробы поглощаются фагоцитами, но не перевариваются (микробы могут даже размножаться внутри фагоцита).
Фагоцитоз авирулентных и низковирулентных является завершенным. Высоковирулентные бактерии, наделенные факторами агрессивности, фагоцитам трудно переварить. Причины выживаемости: подавление слияние лизосомы с фагосомой (при туберкулезе), устойчивость к лизосомальным ферментам (гонококки), выход микробов из фагосом в цитоплазму (риккетсии). «Непереваренные остатки» микробов макрофаги помещают (презентируют) на своей мембране для узнавания лимфоцитами, и подключения специфического иммунитета («ударной артилерии»). После чего одни лимфоциты вырабатывают антитела (гуморальный иммунный ответ), другие – вещества, убивающие микроб (антиген) (клеточный иммунный ответ). Антитела опсонизируют микроорганизм (специфическая опсонизация, антитела – опсонины), Т-лимфоциты выделяют цитокины (γ-интерферон), которые активируют макрофаги. Активированные макрофаги вместе с антителами осуществляют более эффективный фагоцитоз, разрушая фагоцитированные микробы. Такой фагоцитоз называется иммунным! Это фагоцитоз активированными макрофагами антигенов, опсонизированных антителами!
ФАГОЦИТОЗОМ НАЧИНАЕТСЯ ИММУНИТЕТ И ЗАКАНЧИВАЕТСЯ ИМ!
АНТИГЕНЫ И ИХ СВОЙСТВА.
Свойства антигенов.
1. Чужеродность- структурное отличие от собственных молекул, в первую очередь белков, из которых состоит организм, которые определяют индивидуальность организма, и информация о структуре которых хранится в генах. Поэтому чужие белки (антигены) распознаются иммунной системой, как чужеродные - не свои. Чужеродность – это есть отличие данного антигена от антигенов организма.
2. Антигенность (иммуногенность)- способность антигена при введении ворганизм индуцировать иммунный ответ, т.е. вызывать образование антител или сенсибилизированных (иммунных) лимфоцитов.
3. Специфичность- способность взаимодействовать только с теми антителами, которые образовались в ответ на этот антиген. Специфичность определяется наличием на поверхности молекулы антигена характерного участка, который связывается с антителом. Этот участок называется – антигенная детерминанта или эпитоп.Он представляет собой определенную химическую группировку (на белке это мозаика поверхностно расположенных аминокислот), которая как "ключ к замку" соответствует определенному участку (активному центру) на молекуле антитела или рецепторам на поверхности Т-и В- лимфоцитов (TCR и BCR). Именно этот участок определяет специфичность взаимодействия антител и лимфоцитов с антигенами. Т.о. можно сказать, что антитела связывают и нейтрализуют только те антигены, которые вызвали их образование. Антигены могут иметь несколько эпитопов (поливалентны).
Виды антигенов.
Полные антигеныспособны вызывать синтез антител и реагировать с ними. Это наиболее сильные антигены. К ним относятся белки и их комплексы с углеводами, липидами и нуклеиновыми кислотами. Они имеют 2 и более эпитопа, т.е. являются 2-х и более валентными.
Неполные антигены или гаптены- самостоятельно не вызывают выработку антител, но приобретают эту способность при присоединении с высокомолекулярными белковыми носителями. К гаптенам относятся вещества с небольшим молекулярным весом; они имеют одну детерминанту: полисахариды, нуклеиновые кислоты, липиды, пептиды.
Полугаптены– имеют более низкий молекулярный вес, это неорганические радикалы (йод, бром, нитрогруппа и др. радикалы), которые так же, как и гаптены, неспособны вызывать образование антител, но приобретают эту способность после соединения с белками. Такие йодированные или бромированные белки вызывают образование антител, специфичных йоду и брому, т.е. тем детерминантам, которые расположены на поверхности полного антигена, а не белку-носителю.
CD-антигены –молекулы на поверхности клеток, по которым их отличают от других клеток (маркируют).Насчитывается около 350 этих антигенов. На поверхности лимфоцитов имеются CD3, CD4, CD8-антигены.
Гетероантигены– одинаковы антигены у представителей разных видов Например, антигены эритроцитов человека с первой группой крови и антигены возбудителя чумы; стрептококки группы А и антигены клубочков почек человека. Антигенная мимикрия.
Аллоантигены (изоантигены)- разные антигены внутри одного вида (антигены эритроцитов человека с разными группами крови). К ним относятся антигены главного комплекса гистосовместимости (MHC I и II классов).Эти антигены участвуют в презентации антигена(антигенного пептида)Т-лимфоцитам.MHC I класса представляют внутриклеточныеантигены CD8-цитотоксическим Т-лимфоцитам (ЦТЛ). Имеют все клетки организма (кроме эритроцитов, нейронов). Они являются маркерами «своего» для антигенраспознающих клеток, которые уничтожают клетки с измененными молекуламиMHC I класса. MHC II класса представляют внеклеточные антигены CD4 ТH-лимфоцитам (хелперам). Имеют определенные антигенпрезентирующие клетки (АПК), активированные Т-лимфоциты.
Аутоантигены– собственные антигены организма человека: поврежденные или измененные в генетическом отношении компоненты собственных клеток (приобретенные), а также собственные структуры, отделенные от контакта с иммунной системой организма гематоэнцефалическим, гематотестикулярным и др. барьерами – врожденные (например, мозг, хрусталик глаза, щитовидная железа, сперматозоиды).
Суперантигены– антигены микробов, способные без предварительной переработки (презентации) активировать большие группы лимфоцитов (поликлональная активация). Это сопровождается гиперпродукцией различных медиаторов иммунного ответа, что вызывает синдром общей интоксикации организма. [После поликлональной активации наступает дефицит лимфоцитов – иммунодефицит]. Свойства суперантигенов проявляют энтеротоксины стафилококков, токсин синдрома токсического шока, вирус бешенства, микоплазмы, стрептококки, кампилобактер и др.
Существуют также тимусзависимые антигены, которые индуцируют синтез антител с участием Т-клеток, и тимуснезависимые, индуцирующие синтез антител без помощи Т-клеток.
Большинство антигенов относится к тимусзависимым, к тимуснезависимым относятся липополисахариды клеточных стенок грамотрицательных бактерий, синтетические полимеры и др.
АНТИГЕНЫ МИКРООРГАНИЗМОВ.
Микроорганизмы представляют собой сложный комплекс антигенов.
Группоспецифические антигены встречаются у разных видов одного и того же рода или семейства. Видоспецифические антигены - у разных представителей одного вида. Типоспецифи-ческие антигены (или вариантные) - у разных вариантов в пределах одного и того же вида. Последние подразделяют на серологические варианты (серовары).
Среди бактериальных антигенов различают Н-, О-, К- и др.
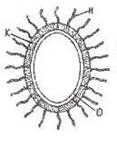
Н – жгутиковые антигены;
К – капсульные антигены;
О – соматический антиген клеточной стенки.
Жгутиковый Н-антиген представлен белком флагеллином жгутиков бактерий. Он разрушается при нагревании, при 5б-80°С, а после обработки фенолом сохраняет свои свойства. Н-антиген получают путем инактивации микробной взвеси формалином.
Соматический О-антиген. Ранее полагали, что О-антиген заключен в содержимое клетки, ее соме, поэтому назвали его соматическим антигеном. Впоследствии оказалось, что этот антиген связан с клеточной стенкой бактерий. О-антиген грамотрицательных бактерий связан с липополисахаридами клеточной стенки. Детерминантными группами этого сложного комплексного антигена являются концевые повторяющиеся звенья полисахаридных цепей (О-специфическая цепь ЛПС), присоединенных к ее основной части. Число и состав сахаров у разных бактерий неодинаковы. Чаще всего в них содержатся гексозы (глюкоза, галактоза, рамноза и др.), аминосахар N-ацетилглюкозамин. У грамотрицательных бактерий О-антиген является их эндотоксином.
О-антиген термостабилен: он сохраняется при кипячении в течение 1-2 часов.
При иммунизации живыми культурами, имеющими жгутики, образуются антитела к О- и Н-антигенами, а при иммунизации кипяченой культурой образуются антитела только к О-антигену.
К-антигены (капсульные) так же, как О-антигены, тесно связаны с липополисахаридами клеточной стенки и с капсулой, но в отличие от О-антигена содержат главным образом кислые полисахариды: глюкуроновую, галактуроновую и другие уроновые кислоты.
По чувствительности к температуре К-антигены подразделяются на А-, В- и L-антигены. А-антигены выдерживают кипячение в течение более 2-х часов. В-антигены не разрушаются при t 60°C в течение часа, L-антигены разрушаются при нагревании до 60°С.
К-антигены располагаются более поверхностно, чем О-антигены, и часто маскируют их. Поэтому для выявления О-антигена нужно кипячением разрушить К-антиген.
Капсульные антигены полисахаридной природы выявлены у пневмококков, клебсиелл и других бактерий, образующих выраженную капсулу. У сибиреязвенных бактерий капсульный антиген состоит из полипептидов.
К капсульным антигенам относится так называемый Vi-антиген брюшнотифозных и некоторых других энтеробактерий, обладающих высокой вирулентностью, в связи с чем данный антиген получил название антигена вирулентности.
Протективный антиген был получен из отечной жидкости сибиреязвенного карбункула. Это термолабильный белок (разрушается при 56°С в течение 30 мин). Он обладает сильно выраженными иммуногенными свойствами, обеспечивающими иммунитет к соответствующему агенту. Протективный антиген образуют возбудители чумы, бруцеллеза, туляремии, коклюша при попадании в организм хозяина, однако он не является их постоянной составной частью.
АНТИТЕЛА И ИХ СВОЙСТВА.
АНТИТЕЛА - это белки глобулиновой фракции крови, которые специфически соединяются с антигенами, вызвавшими их образование.
Они называются иммуноглобулинами и обозначаются Ig.По химическому составу они являются гликопротеидами (белок + углевод) и образуются В-лимфоцитами (плазматическими клетками).
Функции антител:1) участвуют в реакциях образования комплексов антиген-антитело в результате чего происходит связывание, нейтрализация и выведение антигена из организма;
2) усиливают фагоцитоз вместе с другими опсонинами;
3) активация комплемента;
4) входят в состав рецепторов В-лимфоцитов.
Основные свойства антител:
1) гетерогенность – способность вырабатывать на одну молекулу антигена столько антител, сколько у антигена эпитопов;
2) специфичность - способность антител вступать в реакцию только с тем антигеном, на который выработалось данное антитело.
Структура антител
По химическому составу иммуноглобулины относятся к гликопротеидам, т.к. их молекула состоит из протеина и углеводов.
Ig характеризуют по молекулярной массе, константе седиментации и т.п. Различия этих свойств позволили разделить их на 5 классов: IgG, IgM, IgA, IgE и IgD. IgM, G, А имеют подклассы. Все классы и подклассы различаются по аминокислотным последовательностям.
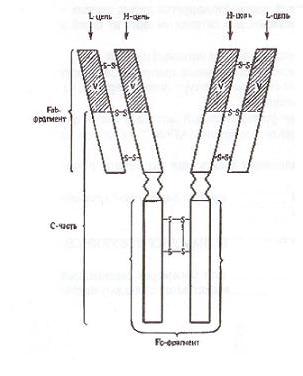 Структурной единицей антител является мономер, состоящий из четырех полипептидных цепей - двух тяжелых Н-цепей (от англ. heavy - тяжелый) и двух легких L-цепей (от англ. light - легкий), соединенных между собой дисульфидными мостиками -S-S-. Легкие и тяжелые цепи отличаются по молекулярной массе: мол. масса L-цепей 23000, мол. масса Н-цепей 50000-70000. Соответственно каждому классу иммуноглобулинов М, G, A,E, D различают пять типов тяжелых цепей: μ (мю), γ (гамма), α (альфа), ε (эпсилон), δ (дельта). Легкие цепи всех пяти классов являются общими и бывают двух типов: κ (каппа) и λ (лямбда). В одной и той же молекуле могут быть только идентичные L-цепи.
Структурной единицей антител является мономер, состоящий из четырех полипептидных цепей - двух тяжелых Н-цепей (от англ. heavy - тяжелый) и двух легких L-цепей (от англ. light - легкий), соединенных между собой дисульфидными мостиками -S-S-. Легкие и тяжелые цепи отличаются по молекулярной массе: мол. масса L-цепей 23000, мол. масса Н-цепей 50000-70000. Соответственно каждому классу иммуноглобулинов М, G, A,E, D различают пять типов тяжелых цепей: μ (мю), γ (гамма), α (альфа), ε (эпсилон), δ (дельта). Легкие цепи всех пяти классов являются общими и бывают двух типов: κ (каппа) и λ (лямбда). В одной и той же молекуле могут быть только идентичные L-цепи.
Как в Н- так и в L-цепях имеется вариабельная V-часть (от англ. various -разный), в которой последовательность аминокислот непостоянна. Остальная часть Н- и L-цепей называется константной С-частью (от англ. constant - постоянный).
При обработке меркаптоэтанолом разрушаются дисульфидные связи, и молекула иммуноглобулина распадается на отдельные цепи полипептидов.
При воздействии протеолитическим ферментом - папаином Ig распадается на три фрагмента: два некристаллизующихся, содержащих антигенсвязывающие центры (активные центры) и названных Fab-фрагментами I и II (от англ. fragment antigen binding – фрагменты, связывающие антиген) и один Fc-фрагмент кристаллизующийся (от англ. fragment crystalizable). Fab-I и Fab-II фрагменты сходны по свойствам и аминокислотному составу и отличаются от Fc-фрагмента. Fab- и Fc-фрагменты соединены между собой гибкими участками Н-цепи (шарнир), благодаря чему молекулы Ig имеют гибкую структуру.
Активный центр (антигенсвязывающий) образован вариабельными концевыми участками легких и тяжелых цепей (V-частъ) и представляет собой полость, пространственная конфигурация которой в точности повторяет пространственную конфигурацию антигенной детерминанты (как перчатка повторяет форму руки). Активный центр занимает около 2% поверхности молекулы Ig.
Соединение антигена с антителом обеспечивают ван-дер-ваальсовы силы, гидрофобные и электростатические взаимодействия, водородные связи.
Таким образом, каждый активный центр формируется двумя цепями - легкой и тяжелой, т.е. полноценной активностью антител ни одна из цепей в отдельности не обладает.
Валентность антитела определяется числом его активных центров.
Полные антитела имеют не менее двух активных центров. Они могут связать две молекулы антигена, образуя сетевую структуру (конгломераты), которая выпадает в осадок (видимые изменения).
Неполные антитела имеют один функциональный активный центр, они не образуют сетевой структуры иммунных комплексов (АГ+АТ), т.е. осадка не образуют.
Моноклональные антитела распознают только одну антигенную детерминанту.
Поликлональные антитела (например, сыворотки) распознают несколько антигенных детерминант в составе антигена.
КЛАССЫ ИММУНОГЛОБУЛИНОВ.
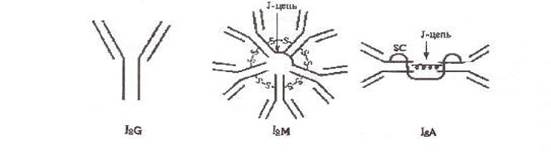
Иммуноглобулины класса М состоят из пяти мономеров соединенных полипептидной цепью (J-цепь) и являются десятивалентными, обладают наиболее высокой авидностью. Это наиболее ранний класс антител, обнаруживаемый при первичном попадании антигена (антитела других классов синтезируются позднее). Обладают свойствами агглютининов, преципитинов, лизинов, опсонинов. Активируют комплемент. Наличие IgM антигенов конкретного возбудителя указывает на наличие острого инфекционного процесса.
Иммуноглобулины класса G являются основным классом антител (до 75% всего Ig), двухвалентны. При первичном контакте с антигеном синтезируются после IgM, а при вторичном - образуются первыми. Единственные из иммуноглобулинов, проникающие через плаценту, обеспечивая пассивный иммунитет плода. Обладают свойствами агглютининов, преципитинов, лизинов, опсонинов. Активируют комплемент.
Обнаружение высоких титров IgG к антигенам конкретного возбудителя указывает на то, что организм находится на стадии реконвалесценции или конкретное заболевание перенесено недавно.
Иммуноглобулины класса А существуют в нескольких формах: моно-, ди- и тримерной. Мономерная форма встречается в сыворотке крови (10-15% всех иммуноглобулинов). Иммуноглобулин А синтезируется плазматическими клетками слизистых оболочек и подслизистых тканей дыхательных путей и кишечного тракта. Часть попадает в кровь, но большая часть остается в слизистых оболочках и играет существенную роль в местном иммунитете, поскольку препятствует адгезии патогенных микроорганизмов на эпителиальных клетках слизистых оболочек.
Секреторный IgA отличается от сывороточного наличием секреторного компонента (SC), выделяемого эпителиальными клетками, что защищает IgA от разрушения ферментами. В отличие от сывороточного секреторный IgA активирует комплемент, что ведет к стимуляции местной фагоцитарной защиты.
Иммуноглобулины класса Е или реагины участвуют в аллергических реакциях. IgE обладают выраженной цитофильностъю, т.е. способностью присоединяться к базофилам и тучным клеткам, в результате чего эти клетки выделяют гистамин и гистаминоподобные вещества, являющиеся медиаторами аллергической реакции. Комплемент не активируют.
Иммуноглобулины класса D обнаруживаются на поверхности развивающихся В-лимфоцитов. Их биологическая роль не установлена. Некоторое увеличение титров IgD находят при беременности, у больных бронхиальной астмой, системной красной волчанкой и лиц с иммунодефицитами. Комплемент не активируют.
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ПЯТИГОРСКАЯ ГОСУДАРСТВЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАФЕДРА БИОЛОГИЧЕСКОЙ ХИМИИ И МИКРОБИОЛОГИИ
Е.Г. ДОРКИНА, Н.В. ПОСТНИКОВА
ИНФЕКЦИЯ И ИММУНИТЕТ
Методические указания для самостоятельной внеаудиторной работы студентов очной формы обучения по дисциплине
С2.Б.12 – МИКРОБИОЛОГИЯ
Пятигорск 2012
УДК 576. 8. 097 (076.5)
ББК 52.6 я 73
Д 68
Рецензент: зав.каф. биологии и физиологии Л.Е. Назарова
Е.Г. Доркина, Н.В. Постникова
Д 68 Инфекция и иммунитет: методические указания для самостоятельной внеаудиторной работы студентов заочной формы обучен
