Часть ii. типовые патологические процессы
Глава 8. ПАТОЛОГИЧЕСКАЯ ФИЗИОЛОГИЯ ПЕРИФЕРИЧЕСКОГО КРОВООБРАЩЕНИЯ И МИКРОЦИРКУЛЯЦИИ
Снабжение организма позвоночных животных кровью обеспечивает система кровообращения. Циркуляция крови по замкнутой системе зависит от деятельности сердца и состояния кровеносных сосудов. По функциональным признакам кровообращение условно делят на центральное (системное), периферическое (органное) и кровообращение в сосудах микроциркуляторного русла. Центральное кровообращение представлено сердцем, обеспечивающим ток крови, и крупными магистральными сосудами. Оно поддерживает уровень системного давления крови, ее поступление в периферические, органные сосуды за счет сердечного выброса, возврата к полостям сердца.
Периферическое, или органное, кровообращение определяет ток крови по артериям и венам отдельных органов и тканей в зависимости от их функционального состояния.
К сосудам микроциркуляторного русла относят: артериолы, прекапилляры, капилляры, посткапилляры, венулы, артериовенулярные анастомозы (шунты), лимфатические капилляры и сосуды. Они доставляют клеткам с кровью необходимое количество кислорода, питательных и минеральных веществ, воду, биологически активные соединения и выводят метаболиты.
К периферическим (органным) типовым нарушениям кровообращения относят артериальную гиперемию, ишемию, венозную гиперемию, стаз, тромбоз, эмболию.
АРТЕРИАЛЬНАЯ ГИПЕРЕМИЯ
Артериальная гиперемия (от греч. hyper —сверх, haima — кровь) — увеличение кровенаполнения органа или ткани в результате поступления крови по расширенным артериям.
Проявляется артериальная гиперемия характерными признаками:
Ø ярко-красной окраской непигментированных органов, тканей, их участков за счет повышенного притока оксигенированной крови, увеличения числа функционирующих терминальных сосудов;
Ø повышением температуры ткани, органа вследствие притока большого количества теплой крови от «ядра» к «периферии» и интенсификации обменных процессов;
Ø пульсацией артериол и мелких артерий из-за перемещения пульсовой волны с крупных магистральных сосудов;
Ø увеличением объема гиперемированного органа за счет повышенного поступления крови и избыточного накопления межтканевой жидкости;
Ø повышенным лимфообразованием и лимфотоком;
Ø усилением функциональной активности органа, обеспеченным дополнительными энергетическими ресурсами и адекватным выведением метаболитов.
Этиология функциональных гиперемий разнообразна. К причинам, их вызывающим, относят физические (механические воздействия, тепло, холод, разные виды излучений); химические (кислоты, щелочи, соли); биологические (яд насекомых, алкалоиды растений, бактериальные эндо- и экзотоксины); токсемия паразитарного происхождения; химические соединения, образующиеся в самом организме (ацетилхолин, гистамин, простагландины).
Различают несколько видов артериальной гиперемии.
Физиологическая артериальная гиперемия возникает прежде всего как ответ на повышение функциональной нагрузки. В качестве примера может служить повышенное кровоснабжение интенсивно работающей скелетной мышцы, миокарда, органов пищеварения после приема корма животным, молочной железы в послеродовом периоде и др.
Патологическая артериальная гиперемия развивается как результат неадекватного действия на ткани раздражителей разного происхождения, вне связи с функцией органа. Может возникнуть на месте контакта патогена с тканью (повышенная температура) или рефлекторно, быть результатом повышенной чувствительности стенки сосудов к аллергенам и у сенсибилизированных животных к фотосенсибилизаторам. Патологическая артериальная гиперемия присуща воспалительным процессам и развивается за счет биологически активных веществ (медиаторов воспаления), выделяемых поврежденными тканевыми структурами.
Патологическую артериальную гиперемию по патогенезу подразделяют на нейрогенную и развивающуюся под непосредственным действием метаболитов на стенки сосудов.
Нейрогенная артериальная гиперемия имеет две разновидности.
Нейротоническая артериальная гиперемия возникает рефлекторно в результате раздражения экстеро- и интерорецепторов и непосредственного действия патогена на сосудодвигательные центры. Эффекторные нервные проводники представлены парасимпатическими нервами, обеспечивающими вазодилатацию. Впервые в экспериментах на собаках и кроликах нейротоническая артериальная гиперемия была продемонстрирована Клодом Бернаром путем раздражения chorda tympani — ветви лицевого нерва (п. facialis), состоящей из парасимпатических волокон, реализующих сосудорасширяющий эффект. В ответ на раздражение повышался приток артериальной крови к нижнечелюстной слюнной железе, сопровождаемый гиперсекрецией слюны. Холинергический механизм артериальной гиперемии может быть реализован и при раздражении симпатических холинергических нервов. Их медиатор — ацетилхолин расширяет артерии слизистых оболочек кишечника, скелетных мышц. Вазодилатоторная гиперемия возникает рефлекторно при раздражении чувствительных периферических нервов.
Нейропаралитическая артериальная гиперемия может развиваться при поражении сосудосуживающего вазомоторного центра под влиянием химических или физических воздействий. К химическим факторам относят, в частности, токсины бактериального происхождения (пневмококки, В. pyocyaneus). Классическим примером развития нейрогенной артериальной гиперемии нейропаралитического типа может служить опыт перерезки шейного узла симпатического нерва, впервые выполненной К. Бернаром (1851 г.). На стороне перерезанного нерва четко выделяются контуры переполненных артериальных сосудов уха.
Симпатические вазомоторы обеспечивают постоянный тонус стенок артерий за счет регулирующего действия медиатора — норадреналина. Блокада его выделения, в том числе путем применения симпатолитических средств, ведет к развитию нейропаралитической артериальной гиперемии.
Вазомоторный механизм артериальной гиперемии, свойственный воспалительному процессу, в определенной мере связан с параличом вазоконстрикторного аппарата.
Миопаралитическая артериальная гиперемия развивается при преимущественном поражении самой сосудистой стенки. Снижение тонуса гладкомышечных элементов, которое возможно при воздействии на ткани холода, тепла (компрессы), механического раздражения, химических соединений (скипидар, кротоновое и горчичное масло, ксилол) и др. Непосредственное влияние химических, физических раздражителей на мышечные элементы стенки сосудов доказывается экспериментами на денервированных или полностью изолированных органах.
К этому типу артериальной гиперемии может быть отнесена вакатная, обусловленная снижением атмосферного давления, например при постановке банок больному животному. Резкое расширение сосудов органов брюшной полости наблюдают у коров после прокола рубца троакаром при остром метеоризме и быстром выведении газов. Увеличение объема рубца, вызванное скоплением газов, приводит к ишемизации сосудов, понижению тонуса их стенок. Снижение внешнего давления на сосуды после прокола сопровождается развитием реактивной артериальной гиперемии.
Постанемическую артериальную гиперемию можно наблюдать и когда быстро выводят жидкость из плевральной (гидроторакс) или брюшной (асцит) полости. Ввиду большой емкости сосудов, снабжающих органы брюшной полости, особенно брыжеечных сосудов, при быстром выведении газов из рубца у крупного рогатого скота возможно осложнение в виде коллапса, развивающегося вследствие ишемии головного мозга. Поэтому выведение газов и жидкости из полостей больных животных следует делать очень осторожно, медленно, чтобы не допустить депонирования крови и ишемии головного мозга.
Нарушения микроциркуляции при артериальной гиперемии определяются:
ξ повышением разницы в гидродинамическом давлении в пре- и посткапиллярах;
ξ увеличением числа функционирующих капилляров с заполнением их эритроцитами;
ξ возрастанием площади сосудов для транскапиллярного обмена кислорода, субстратов и продуктов их метаболизма, ионов, гормонов, медиаторов, других биологически активных веществ;
ξ усилением циркуляции жидкости между кровеносными и лимфатическими сосудами, накоплением ее в тканях;
ξ чрезмерным растяжением стенок сосудов, приводящим к повышению проницаемости гистогематического барьера.
Последствия артериальной гиперемии зависят от ее происхождения. Физиологическая артериальная гиперемия способствует активации обменных процессов, усилению функциональной активности органа, неспецифических факторов защиты (фагоцитоз), гипертрофии и гиперплазии. Положительное значение артериальной гиперемии лежит в основе таких лечебных процедур, как применение горчичников, согревающих компрессов, всевозможных мазей, постановки банок.
Артериальная гиперемия, развивающаяся в результате патологических процессов, сопровождается нежелательными последствиями для организма:
ض перерастяжением и выходом в ткань эритроцитов путем диапедеза или в результате микроразрывов;
ض увеличением объема органа за счет накопления межтканевой жидкости, которое негативно сказывается на функции окружающих тканей, особенно в головном мозге;
ض возможностью перехода артериальной гиперемии в венозную.
ВЕНОЗНАЯ ГИПЕРЕМИЯ
Венозная гиперемия характеризуется увеличением кровенаполнения органа и тканей вследствие затрудненного оттока крови или его полного прекращения. Препятствуют оттоку крови механические причины. К ним могут быть отнесены:
· сдавливание вен снаружи отечной тканью, опухолью, соединительнотканным рубцом, туго наложенной повязкой, жгутом;
· сужение просвета вен или их закупорка тромбом, эмболом;
· гипотензии в результате сердечной или сосудистой недостаточности.
Венозная гиперемия не развивается в тех случаях, когда имеется достаточно выраженное коллатеральное кровообращение, обеспечивающее адекватный отток крови по анастомозам.
Признаки венозной гиперемии обусловлены снижением кровотока, переполнением органа венозной кровью. Это приводит к гипоксии циркуляторного происхождения, накоплению продуктов метаболизма, повышению содержания в крови восстановленного гемоглобина. Появляется один из кардинальных признаков венозного застоя — цианоз, т. е. синюшный оттенок органов и тканей, особенно характерный для видимых слизистых оболочек. Замедление обменных процессов, скопление в ткани венозной крови, менее нагретой, чем артериальная, проявляются снижением температуры поверхностно расположенных органов. Увеличение давления в капиллярной сети, посткапиллярах и венулах приводит к выходу за их пределы транссудирующей жидкости. Она растягивает тканевые щели и накапливается там в значительных количествах. Переполнение сосудов кровью и скопление транссудирующей жидкости в ткани приводят к увеличению объема органа — отеку.
Микроциркуляторные расстройства в области венозной гиперемии определяются механическим препятствием кровотоку в венах. Замедляется кровоток, снижается артерио-венозная разница давления, увеличивается диаметр капилляров, посткапилляров, венул, замедляется отток крови, образуются микротромбы. При полном прекращении тока крови по венам наблюдают маятникообразные движения крови. Во время систолы сердца кровь толчкообразно продвигается по сосудам, при диастоле кровь перемещается в обратном направлении, отталкиваясь от препятствия — эмбола, тромба, сдавленных стенок сосудов.
Высокая проницаемость гистогематических барьеров сопровождается выходом жидкой части крови — транссудата, содержащего небольшое количество белка, в отличие от экссудата, образующегося при воспалении.
Маятникообразные движения крови завершаются стазом — полной остановкой кровотока. Если устранить препятствие току крови, то стаз в самом начале его развития обратим: возобновляется проходимость микрососудов и движение эритроцитов. Он становится необратимым при дезорганизации структуры эритроцитов и повреждениях стенок микроциркуляторного русла. Остановка кровотока ингибирует тканевое дыхание, приводит к микронекрозам. Их последствия зависят от функциональной значимости органа. Наиболее чувствительна к капиллярному стазу ткань головного мозга, сердца, почек.
ИШЕМИЯ
Ишемия(от греч. ischein — задерживать, haima — кровь) — ограничение или полное прекращение притока крови к тканям. Синоним термина — «местное малокровие».
Для ишемии характерны следующие признаки:
ü побледнение как результат сниженного или прекращенного притока артериальной крови;
ü уменьшение органа в объеме;
ü снижение температуры поверхностно расположенного ишеми-зированного участка из-за того, что отдача тепла превалирует над его содержанием;
ü извращение чувствительности — парестезия (чувство «онемения», «бегания мурашек»);
ü болевой синдром;
ü нарушение или выпадение функции, дистрофические процессы.
Причины, вызывающие ишемию, разнообразны: она может быть обусловлена спазмом сосудов, частичной или полной закупоркой артерии, сдавливанием артерий извне.
Ангиоспастическая ишемия характерна преобладанием симпатикоадреналового влияния на артерии, прекапилляры над парасимпатическим. Рефлекторный спазм сосудов может быть обусловлен отрицательными эмоциональными воздействиями (психогенный стресс), раздражением болевых рецепторов (механические повреждения, тепло, холод), химическими агентами разного происхождения, в том числе бактериальными токсинами. К спазму артерий может привести прямое воздействие на расположенный в подкорке сосудодвигательный центр механических факторов (опухоли мозга, кровоизлияния, отек, травмы), токсических веществ, содержащихся в циркулирующей крови.
При патологии внутренних органов могут появиться висцеро-висцеральные патологические рефлексы, сопровождающиеся ва-зоконстрикцией. Так, спазм коронарных сосудов может быть результатом воспаления поджелудочной железы, прохождения камней по мочевыводящим или желчным путям. Ангиоспастическая ишемия может быть и условнорефлекторной природы.
Чувствительность мышечных элементов стенок сосудов имеет немаловажное значение в развитии ишемии. Так, аллергизация организма повышает восприятие вазоконстрикторами специфических антигенов и неспецифических раздражителей (тепло, холод, химические соединения).
Обтурационная ишемия развивается как следствие полного или частичного закрытия просвета артерий тромбом или эмболом. У лошадей нередко наблюдают так называемые тромбоэмболические колики. При заболевании делафондиозом личинки паразита локализуются на внутренней стенке передней брыжеечной артерии. Они травмируют ткань, вызывая образование обширного пристеночного тромба. Его частицы отрываются и в виде эмболов закупоривают брыжеечные артерии, что вызывает сильную болевую реакцию — колики. Больные животные ударяют задними конечностями по животу, падают, перекатываются по земле.
Сужение просвета артериальных сосудов, ведущее к обтурационной ишемии, развивается при облитерирующем эндоартериите, атеросклерозе, узелковом периартрите.
В отдельных случаях ишемизация тканей может быть результатом перераспределения крови. Так, прокол рубца при тимпании у крупного рогатого скота и быстрое выведение газов могут привести к коллатеральной ишемии мозга из-за оттока крови к органам брюшной полости. Аналогичную опасность может представлять быстрое освобождение брюшной полости от жидкости при асците у собак и кошек. Одним из ведущих факторов в генезе родильного пареза коров считают коллатеральную ишемию мозга из-за депонирования крови в молочной железе. Широко используемым лечебным приемом при этом заболевании является вытеснение крови из вымени путем нагнетания воздуха в протоки молочной железы.
Компрессионная ишемия является результатом сдавливания артерий извне отечной тканью, рубцом, опухолью, инородным телом, лигатурой. Особенности микроциркуляции при компрессионной ишемии слагаются из:
Ø понижения внутрисосудистого давления ниже места сужения;
Ø уменьшения разности артерио-венозного давления;
Ø сокращения числа функционирующих капилляров, их превращения в плазматические или полного спадения;
Ø уменьшения или прекращения доставки тканям оксигенированной крови, энергетических и пластических материалов, биологически активных веществ;
Ø накапливания в клетках продуктов метаболизма, несмотря на усиленную резорбцию;
Ø замедления или прекращения лимфотока вследствие обезвоживания ткани.
Последствия ишемии зависят от скорости обтурации сосуда. Медленное сужение просвета артерий способствует развитию коллатерального кровообращения. Чем моложе животное, тем эластичнее сосуды; развивающиеся коллатерали могут компенсировать недостаточность кровоснабжения по магистральному сосуду. И, наоборот, чем старше животное, тем меньше вероятность замещения кровоснабжения коллатералями. Диаметр просвета сосуда и величина ишемизированного участка существенно влияют на состояние больного организма. Очень важны чувствительность органа к недостаточности кровоснабжения и его значимость для организма. Головной мозг, сердце, почки более чувствительны к ишемии, чем, например, скелетная мышца. Объясняется это тем, что ткани этих жизненно важных органов снабжаются кровью через концевые артерии, не имеющие анастомозов. Поэтому перекрытие магистральных сосудов не компенсируется кровоснабжением по коллатералям, как это может быть, например, при патологии легких. Кроме того, клетки мозга, сердца, почек, интенсивно функционируя, требуют в достаточном количестве кислород, питательные и биологически активные вещества. Недостаточность кровоснабжения мозга сопровождается неоднозначными последствиями. Они зависят от локализации ишемизированного участка. Ишемия тканей, где локализуются дыхательный и сосудодвигательный центры, может завершиться быстрой смертью животного; ишемизация двигательных зон коры больших полушарий приводит к парезам, параличам и т. д.
Ишемия изначально приводит к гипоксии, аутоинтоксикации, за которыми следуют снижение функциональной активности пораженного органа, развитие гипопластических процессов: дистрофии, гипотрофии, атрофии. Завершающим итогом ишемии могут быть некроз, омертвение ткани.
СТАЗ
Стаз (от греч. stasis — стояние, неподвижность) — прекращение, тока крови (гемостаз) или лимфы (лимфостаз) в сосудах микроциркуляторного русла.
Причинами стаза могут быть:
ξ патологические изменения, возникающие в самих капиллярах и обусловленные нарушениями реологических свойств крови (истинный капиллярный стаз);
ξ ишемия (ишемический стаз);
ξ венозная гиперемия (венозный стаз).
Истинный стаз возникает под воздействием химических (неорганические и органические яды), физических (холод, тепло, высыхание) и биологических (токсины микробиального, паразитарного происхождения) факторов. Под влиянием патогенов клетки сосудов и окружающих тканей выделяют биологически активные вещества (гистамин, серотонин, брадикинин), расширяющие стенки сосудов, повышающие их проницаемость, что ведет к усиленному выходу жидкости, электролитов, низкомолекулярных белков в ткани. Возрастает концентрация высокомолекулярных белков — глобулинов, фибриногена в плазме крови, повышается вязкость, замедляется кровоток. Адсорбция высокомолекулярных белков на поверхности эритроцитов способствует началу их агрегации и агглютинации. Эти процессы потенциируются биологически активными веществами, такими, как агглютинины, катехо-ламины, простагландины F и Е, тромбоксан А2- Эритроциты в просвете капилляров останавливаются, образуя «монетные столбики».
Агрегация эритроцитов является важным фактором, изменяющим реологические свойства крови. Сопротивление току крови в капиллярах возрастает. Поступающие из поврежденных эндотели-оцитов и клеток ткани катионы — ионы калия, кальция, магния, натрия и др. адсорбируются на мембране эритроцитов, нейтрализуют отрицательный заряд или меняют его на положительный. В результате агрегаты эритроцитов адгезируются на интиме сосудов, движение тока крови замедляется, а затем останавливается. Эритроциты деформируются, границы между ними исчезают, развивается капиллярный стаз.
Стаз ишемического происхождения развивается как следствие замедления и прекращения притока артериальной крови. Замедленный приток, возникновение турбулентности в движении крови по артериолам и капиллярам вторичны; вслед за первичной закупоркой, сдавливанием, спазмом артерий ведет к агрегации, агглютинации и адгезии эритроцитов к эндотелиальной стенке сосудов — стазу.
Венозный стаз представляет собой заключительный этап венозной гиперемии, явившейся результатом тромбоза или сдавливания венозных сосудов. Отток крови при венозной гиперемии замедлен. Она сгущается, меняются ее физико-химические и реологические свойства. Выделяемые поврежденными клетками (гипоксия, ацидоз) биологически активные вещества определяют агрегацию, агглютинацию эритроцитов и адгезию к сосудистой стенке.
Признаки стаза легко обнаруживаются при микроскопии. В сосудах микроциркуляторного русла хорошо видны неподвижные агрегаты эритроцитов, других клеточных элементов крови, признаки микрокровотечений, а при гемолизе эритроцитов — окрашивание межклеточной жидкости.
Внешне признаки «вторичного» стаза затушеваны проявлениями ишемии или венозной гиперемии.
Последствия стаза зависят от ряда обстоятельств. При быстром устранении причин агрегированные эритроциты возвращаются в общее русло крови с сохранением своих специализированных функций. Агглютинизированные, адгезированные эритроциты не покидают микроциркуляторное русло. Продолжительный стаз становится причиной дистрофических изменений окружающих клеток. Слияние участков микронекроза как самого тяжелого исхода стаза может привести к инфаркту.
ИНФАРКТ
Участок ткани, подверженный некрозу в результате прекращения кровоснабжения, адекватного потребностям, носит название инфаркта (от лат. infarcire — начинять). Причины инфарктов — образование в просвете сосуда тромба или закупорка его эмболами, длительный спазм артерий, эндоартерииты, застойная гиперемия. Инфаркты поражают чаще всего паренхиматозные органы, наиболее чувствительные к гипоксии, кровоснабжение которых обеспечивается концевыми артериями. Закрытие просвета такой артерии приводит к омертвению конусообразного участка, обращенного основанием к поверхности органа. Поэтому на разрезе омертвевшая ткань имеет форму клина.
Различают инфаркты белые (анемические, ишемические) и красные (геморрагические).
Белый инфаркт развивается в органах, где коллатерали очень слабо развиты, кровь в ишемизированный участок не поступает. Этому способствует рефлекторный спазм окружающих артерий, препятствующий поступлению туда эритроцитов, сосуды заполнены лишь плазмой. Белые инфаркты чаще обнаруживают у животных в почках, сердце (рис. 7). Встречаются ишемические инфаркты с геморрагическим поясом (венчиком), возникающие в результате быстрой смены рефлекторного спазма коллатералей, окружающих некротизированный участок, на паралитическую вазодилатацию и переполнение их кровью.
Красный инфаркт назван так потому, что в некротизированную ткань поступают эритроциты из окружающих сосудов. Клетки крови через стенки разрушенных капилляров ингибируют, пропитывают некротизированные участки тканей, окрашивая их в темно-красный цвет, они хорошо отграничены.
Геморрагические инфаркты бывают обычно в легких, кишечнике. Застойного происхождения они могут быть в результате быстрого сдавливания или тромбоза венозных сосудов. У сельскохозяйственных животных их наблюдают при перекручиваниях матки, завороте кишок, часто регистрируемом у свиней, инвагинациях, ущемлениях в грыжевом мешке.
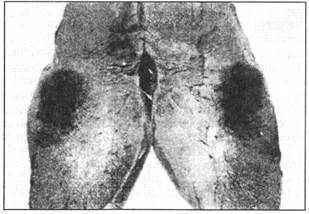
Рис. 7. Инфаркт миокарда у лошади, болевшей инфекционной анемией (Добин, 1968)
Исход инфаркта зависит от его величины локализации, а также от состояния животного.
Существует такое понятие, как микроинфаркт. Он возникает при закупорке тромбами, эмболами мелких артерий или их длительном спазме. Участки микронекрозов могут сливаться, формировать макроинфаркт, различимый невооруженным глазом.
У животных, в частности у лошадей, инфаркты сердца, кишечника заканчиваются летально. При выздоровлении животных вокруг некротической массы развивается воспалительный процесс с последующим замещением мертвой ткани соединительнотканным рубцом. Инфаркты мозга могут осложняться парезами, параличами, заканчиваться летальным исходом. При благоприятном исходе на их месте образуются кисты. Обсеменение некротизированных участков микрофлорой завершается гнойным расплавлением. Инфаркты почек, довольно часто обнаруживаемые у старых животных, не представляют особой опасности для жизни. Они трансформируются в плотную рубцовую ткань, соединенную с капсулой.
КРОВОТЕЧЕНИЕ
Под кровотечением (haemorrhagia, от греч. haema — кровь, rrhagia — течь) понимают выход крови из сосудов или сердца. Покидая кровеносную систему, кровь может изливаться во внешнюю среду, что носит название наружного, или в органы и полости тела — внутреннего кровотечения.
Выход крови во внешнюю среду возникает у животных при ранениях кожных покровов и подлежащих тканей, травмах матки и родовых путей при патологических родах, с рвотными или фекальными массами, из легких и мочевых путей, при ушибах, переломах костей.
Для внутреннего кровотечения характерен выход крови в полости — брюшную (разрыв ткани при гепатозе, селезенки — при гемоспоридиозах), грудную (венозный застой), перикардиальную (разрыв в склерозированной стенке дуги аорты) и ткани.
По виду поврежденных сосудов кровотечение бывает артериальным, венозным, паренхиматозным или капиллярным.
Артериальное кровотечение проявляется алым цветом оксигенированной крови, она изливается сильной пульсирующей струей в такт сокращениям сердца, самопроизвольно останавливается с трудом, что может быть смертельно опасным.
Венозное кровотечение проявляется равномерным, сравнительно медленным током крови темно-красного цвета.
Паренхиматозное кровотечение наблюдают при разрывах внутренних органов (селезенки, печени), мышц, с травмированной поверхности которых через капилляры медленно изливается кровь темно-красного цвета. Оно опасно трудностью прижизненной диагностики и тотальной кровопотерей.
Выход крови за пределы сосудов может быть результатом:
ض разрывов стенок (haemorrhagia per rhexin, от лат. rhexio — разрываю), вызванных механическими повреждениями (ранения) или структурными изменениями (склероз, инфаркт миокарда, аневризмы аорты, других сосудов);
ض изъязвления стенок (haemorrhagia per diabrosin, от греч. diabrosis — аррозия, разъедание) как результат ферментативных процессов. Аррозивные кровотечения наблюдают у животных при язвенной болезни желудка, в очаге гнойного воспаления, при поражениях злокачественными опухолями;
ض диапедеза (haemorrhagia per diapedesis, от греч. dia —через, pedao — скачу) — выхода эритроцитов через стенки артериол, капилляров, венул при резком повышении проницаемости (венозный застой, многие инфекционные и инвазионные болезни, гипоксия, отравления, воспаление). Общее системное повышение проницаемости сосудов микроциркуляторного русла, возникновение геморрагического диатеза (от греч. diatesis — склонность, предрасположенность) обусловлено тромбоцитопенией, гемофилией, повышенной проницаемостью при многих инфекционных болезнях (чума свиней, сибирская язва), авитаминозе С, других патологических состояниях.
Кровотечение может быть первичным, возникающим вслед за ранением, и вторичным, развивающимся спустя несколько часов или суток после остановки первичного. Вторичное кровотечение возможно вследствие инфицирования раны, гнойного расплавления тромба, снятия животным кровоостанавливающей повязки, других причин.
Под кровоизлиянием как одной из форм кровотечений понимают выход крови за пределы сосуда и скопление ее в тканях. По величине кровоизлияния подразделяют на:
· гематому — кровяную опухоль, возникающую преимущественно при разрыве артерий, представляющую собой искусственную полость, заполненную свернувшейся кровью. У животных гематому наиболее часто наблюдают в области подкожной клетчатки, межмышечной соединительной ткани. Если полости не образуется, а ткань пропитана кровью, то говорят о геморрагической инфильтрации;
· кровоподтеки — плоскостные скопления крови в слизистых оболочках, коже;
· петехии и экхимозы — точечные кровоизлияния на коже, слизистых оболочках, серозных поверхностях, обусловленные диапедезом эритроцитов. Они характерны для многих заболеваний животных (петехиальная горячка, пастереллез).
Кровоизлияния следует отличать от эритемы — разлитого или ограниченного покраснения кожи, слизистых оболочек за счет артериальной гиперемии. Например, при роже свиней красные пятна на коже формируются путем расширения артериальных сосудов (эритемы), а при чуме ограниченные пятна на коже свиней обусловлены кровоизлияниями (петехии).
Последствия кровотечений различны. Они зависят от количества потерянной крови, локализации, продолжительности, вида животного, других обстоятельств.
Острая потеря крови в количестве 50—60 % общей массы сопровождается уменьшением ударного и минутного выбросов, артериальной гипотензией, гипоксемией, гипоксией, снижением температуры тела. Чем быстрее организм теряет кровь, тем тяжелее последствия. Ранения крупных сосудов, разрыв аневризмы аорты, селезенки, печени, маточные кровотечения при патологических родах приводят к быстрой, не компенсируемой потере большого количества крови, несовместимой с жизнью. Потеря до 30 % объема циркулирующей крови компенсируется срочными рефлекторными реакциями— тахикардией, одышкой, мобилизацией депонированной крови, межклеточной жидкости, стимуляцией эритро-, тромбо-, лейкопоэза гемопоэтинами. Повторное кровотечение переносится легче. Длительная экстравазация крови, например, при язвенной болезни желудка и двенадцатиперстной кишки у свиней, норок приводит к хронической анемии.
Кровоизлияния не представляют опасности с точки зрения потери крови. Их главная опасность в локализации. Наиболее тяжелым, а часто и смертельным является кровоизлияние в мозг (солнечный удар у неадаптированных к аридным условиям лошадей). Излившаяся кровь подвергает сдавливанию окружающие ткани, затрудняет их кровоснабжение, приводит к гипоксии, некрозу. Излившаяся кровь свертывается, эритроциты разрушаются, гемоглобин трансформируется в кровяной пигмент — гемосидерин; плазма рассасывается. Масса фибрина при гематомах может прорастать соединительной тканью, организовываться, подвергаясь в дальнейшем петрификации. Тромбическая масса может подвергаться инфицированию и превращаться в очаг гнойного воспаления — абсцесс.
Не все животные в равной степени чувствительны к кровопоте-рям. Чувствительность определяется видом животных, возрастом, индивидуальными особенностями. Наиболее тяжело переносят кровопотери свиньи, собаки; сравнительно легче — лошади и крупный рогатый скот. Молодые и старые животные чувствительнее к кровопотерям, чем взрослые. Ожирение животных снижает компенсаторные возможности организма при кровотечениях.
НАРУШЕНИЯ МИКРОЦИРКУЛЯЦИИ
Микроциркуляция (от греч. mikros — мельчайший, лат. circulatio — дуговое движение) представляет собой перемещение крови и лимфы по артериолам, прекапиллярам, капиллярам, посткапиллярам, венулам, артерио-венозным анастомозам (шунтам) и лимфатическим капиллярам.
Кровеносная система замкнутая. Лимфатические капилляры представляют собой слепые коллекторы, по которым лимфа поступает в лимфатическую сеть и направляется в венозную систему через грудной (ductus thoracicus) и другие протоки. В понятие микроциркуляции включают, таким образом, перемещение жидкости между кровеносными и лимфатическими капиллярными сетями, по внутриклеточным системам, трансмембранный обмен газами, субстратами и продуктами метаболизма, сигнальными молекулами.
Расстройства микроциркуляции вызываются многочисленными факторами, к которым можно отнести расстройство кровообращения сердечного и сосудистого происхождения (гипотензию, гипертензию, артериальную и венозную гиперемию, ишемию), нарушение целостности стенок сосудов микроциркуляторного русла и реологических свойств крови.
К типичным нарушениям микроциркуляции относят внутрисо-судистые расстройства, патологические изменения проницаемости сосудов, внесосудистые расстройства.
Внутрисосудистые, или интраваскулярные, расстройства микроциркуляции обусловлены замедлением или прекращением тока крови или лимфы. Суспензионная стабильность клеток крови, обусловленная отрицательным зарядом эритроцитов и тромбоцитов, нарушается в результате выхода альбуминов за пределы сосудов. Абсолютное или относительное увеличение содержания в плазме крови микромолекул фибриногена и глобулинов, заряженных положительно, их адсорбция на поверхности клеток крови приводят к дестабилизации суспензии, агрегации эритроцитов, тромбоцитов, лейкоцитов. Сужение сосудов, увеличение вязкости, расстройство гемо- и лимфодинамики, затрудняя перфузию крови через микрососуды, способствует внутрисосудистой агрегации клеток. Развивается так называемый «сладж-феномен» (от англ, sluge — густая грязь, тина). Внутрисосудистое формирование агрегатов из эритроцитов, тромбоцитов, лейкоцитов наблюдают при многих инфекционных заболеваниях, при отморожениях и ожогах, шоке разного происхождения, острой сосудистой недостаточности (коллапсе), отравлениях, заболеваниях, сопровождающихся альбуминурией, в послеоперационном периоде.
Сладжирование крови складывается последовательно и начинается с агрегации тромбоцитов с хиломикронами (частицы липидов), а в последующем — с эритроцитами. Агрегация сопровождается адгезией (слипанием) клеток между собой и с клетками эндотелия сосудов, агглютинацией (склеиванием) клеток крови и цитолизом.
Различают следующие виды сладжа:
ü классический, с клеточными агрегатами крупных размеров, плотной упаковкой, неровными очертаниями;
ü декстрановый — агрегаты клеток различной величины, с плотной упаковкой и округлыми очертаниями;
ü аморфный, представляющий собой множественные гранулы, состоящие из нескольких эритроцитов.
Агрегация эритроцитов ведет к сужению просвета сосудов, полной или частичной обтурации (закупорке) капилляров, замедлению тока крови, турбулентному характеру кровотока. Закупорка эритроцитарными агрегатами микрососудов приводит к тому, что они становятся только плазменными. Освобождающиеся поврежденными клетками гистамин, серотонин, брадикинин повышают проницаемость гистогематических барьеров; гипоксия и ацидоз повреждают сосудистые стенки, создаются условия для возникновения множественных микротромбов. Тяжесть микроциркуляторных расстройств возрастает. Наступает синдром капиллярно-трофической недост
